
- •Дефекты кристаллической решетки
- •Перемещение атомов в твердых и жидких телах
- •Структура и свойства оксидов железа
- •Термодинамика восстановления оксидов железа
- •Особенности восстановления оксидов при наличии растворов
- •Восстановление оксидов находящихся в растворе
- •Переход продукта восстановления в раствор
- •Кинетика и механизм восстановления оксидов
- •Современные представления о механизме восстановления оксидов
- •Внешняя диффузия газа
- •Диффузия газа в порах кускового материала
Перемещение атомов в твердых и жидких телах
При химических или структурных изменениях в твердой фазе происходит перемещение атомов. Существуют различные механизмы этого явления, один из них — переход атомов из нормальных узлов решетки в расположенную рядом вакансию. Как было отмечено выше, вакансии существуют в каждом кристалле при всех температурах, отличных от абсолютного нуля. Скорость диффузии атомов в этом случае зависит от легкости перемещения атомов из нормального узла в вакантный и от концентрации вакансий. Передвижение атомов в каком-либо направлении эквивалентно блужданию вакансий в противоположном направлении. В связи с этим в подобном случае можно говорить о диффузии вакансий.
Другим возможным механизмом может бьггь движение атомов по междоузлиям. Если атомы переходят из нормального узла решетки в междоузлия, как это происходит при образовании дефектов по Френкелю, то далее они легко перемещаются по кристаллу из одного междоузлия в другое. Одним из вариантов этого процесса является так называемый эстафетный механизм, при котором атом, находящийся в междоузлии, переходит в нормальный узел, выталкивая ранее находившийся там атом в новое междоузлие.
Действительный механизм процесса в данной системе определяется относительной величиной энергии, требующейся для протекания этого процесса. Диффузионные процессы, как правило, во многом определяют скорость химических реакций и спекания. Количественно диффузия характеризуется двумя законами Фика:
I = -D(dc/dx), (2.3)
где / — диффузионный поток (количество вещества в единицу времени на единицу площади); с — концентрация вещества в единице объема; х — расстояние в направлении диффузии; D—коэффициент диффузии, см2/с;
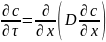 (2.4)
(2.4)
или, если коэффициент диффузии не зависит от концентрации,
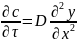 (2.5)
(2.5)
где т — время.
Согласно выражению Нернста—Эйнштейна, Di= BftT,где Bi— подвижность атома (скорость, приобретаемая под действием единицы силы). Это выражение удобно применять при рассмотрении подвижности заряженных частиц и связи между коэффициентом диффузии и электропроводностью.
Атом при перемещении в решетке из одного положения в другое должен пройти через промежуточное положение с высокой энергией. Величина необходимой для этого энергии называется энергией активации процесса, а температурная зависимость коэффициента диффузии может быть представлена в виде:
D = D0exp\-E/(RT)}, (2.6)
где Е — кажущаяся энергия активации диффузии.
Величина коэффициента диффузии и его изменение с ростом температуры зависят, прежде всего, от концентрации дефектов кристаллической решетки (вакансий, ионов в междоузлиях) и энергии активации их перемещения по решетке. Как правило, на кривой зависимости между температурой и коэффициентом диффузии различают два участка: низкотемпературный, во многом определяемый наличием примесей (так называемая примесная область диффузии), и высокотемпературный (собственно область диффузии).
Для нестехиометрических оксидов концентрация дефектов кристаллической решетки велика по сравнению с концентрацией дефектов по Френкелю и Шотпей в решетке стехиометрических оксидов или по сравнению с концентрацией дефектов, обусловленных наличием примесей. Энергия активации диффузии катионов при постоянном составе вюстита соответствует величине энергии активации перемещения вакансий по катионным узлам и составляет 125— 150кДж/моль.
В жидкостях диффузия протекает иначе, так как строение решеток в них другое. В этом случае диффузия характеризуется высокими значениями коэффициентов диффузии и низкими значениями величины энергии активации, так как решетка жидкости обладает высокой степенью неупорядоченности.
Необходимо отметить, что диффузия вдоль границ зерен, где решетка менее упорядочена, должна идти быстрее, чем в объеме кристалла. Точно так же и подвижность атомов на поверхности кристалла должна быть больше, чем внутри кристалла. Таким образом, при низких температурах должна преобладать диффузия по поверхности и границам зерен, а при высоких — объемная диффузия.
