
- •Загальні правила
- •Запобіжні заходи
- •Перша допомога при нещасних випадках
- •Лабораторна робота 1 методи очистки речовин
- •Перекристалізація
- •Перекристалізація речовин із органічних розчинників
- •Перегонка
- •Перегонка при атмосферному тиску
- •Дробна (фракційна) перегонка
- •Дослід 1.1 Перекристалізація бензойної кислоти
- •Дослід 1.2. Перегонка суміші бензолу і ксилолу
- •Контрольні запитання
- •Лабораторна робота 2 визначення основних фізичних констант органічних речовин
- •1. Визначення температури плавлення
- •2. Визначення температури кипіння
- •3. Визначення густини рідкої речовини
- •Маса води в об’ємі пікнометра при 4 с(х) 1
- •Маса 1 мл води при 4с(х) 1
- •4. Визначення показника заломлюваності
- •Дослід 2.1. Визначення температури плавлення
- •Контрольні запитання
- •Лабораторна робота 3 якісний елементний аналіз органічних сполук
- •Дослід 3.1. Визначення вуглецю пробою на обвуглювання
- •Визначення вуглецю і водню спаленням речовини з оксидом міді (II)
- •Дослід 3.2. Визначення азоту сплавленням речовини з металічним натрієм
- •Хімізм процесу:
- •Дослід 3.3. Визначення сірки сплавленням речовини з металічним натрієм
- •Хімізм процесу:
- •Дослід 3.4. Визначення хлору за зеленим забарвленням полум’я (проба Бельштейна)
- •Хімізм процесу:
- •Контрольні запитання
- •Лабораторна робота 4 насичені вуглеводні Будова, ізомерія, номенклатура, властивості
- •Гомологічний ряд
- •Дослід 4.1. Синтез метану та вивчення його властивостей
- •Хімізм процесу:
- •Хімізм процесу:
- •Реакція метану на бромну воду і перманганат калію
- •Дослід 4.2. Бромування насичених вуглеводнів
- •Хімізм процесу:
- •Окислення парафінів
- •Дослід 4.3. Окислення алканів
- •Контрольні запитання
- •Лабораторна робота 5 алкени Будова, ізомерія, номенклатура, властивості
- •Дослід 5.1. Отримання етилену і його горіння
- •Хімізм процесу:
- •Дослiд 5.2. Приєднання до етилену брому
- •Хiмiзм процесу:
- •Дослiд 5.3. Взаємодiя з окислювачами
- •Хiмiзм процесу:
- •Контрольнi запитання
- •Лабораторна робота 6
- •Будова, iзомерiя, номенклатура I властивостi
- •Дослiд 6.1. Отримання ацетилену I його горiння.
- •Хiмiзм процесу:
- •Дослiд 6.2. Приєднання брому до ацетилену
- •Хiмiзм процесу:
- •Дослiд 6.3. Реакцiя ацетилену з окислювачами
- •Дослiд 6.4. Утворення ацетиленiду срiбла
- •Хiмiзм процесу:
- •Дослiд 6.5. Утворення ацетиленiду мiдi
- •Хiмiзм процесу:
- •Контрольнi запитання
- •Лабораторна робота 7 ароматичнi сполуки Будова, iзомерiя, номенклатура I властивостi
- •Дослiд 7.1. Синтез бензолу iз бензойнокислого натрiю
- •Хiмiзм процесу:
- •Дослiд 7.2. Синтез нiтробензолу
- •Хiмiзм процесу:
- •Дослiд 7.3. Дiя бромної води на бензол
- •Дослiд 7.4. Дiя перманганату калiю на бензол
- •Дослiд 7.5. Окислення гомологiв бензолу
- •Контрольнi запитання
- •Лабораторна робота 8 галогенопохiднi вуглеводнi Будова, iзомерiя, номенклатура I властивостi
- •Дослiд 8.1. Синтез хлористого етилу
- •Хiмiзм процесу:
- •Дослiд 8.2. Синтез йодоформу з етилового спирту
- •Дослiд 8.3. Отримання бромбензолу
- •Хiмiзм процесу:
- •Контрольнi запитання
- •Лабораторна робота 9 спирти I простi ефiри Будова, iзомерiя, номенклатура I властивостi
- •Дослiд 9.1. Утворення I гiдролiз алкоголятiв
- •Хiмiзм процесу:
- •Дослiд 9.2. Окислення етилового спирту оксидом мiдi (II)
- •Хiмiзм процесу:
- •Дослiд 9.3. Окислення етилового спирту перманганатом калiю
- •Хiмiзм процесу:
- •Дослiд 9.4. Синтез дiетилового ефiру
- •Хiмiзм процесу:
- •Дослiд 9.5. Взаємодiя глiцерину з гiдроксидом мiдi (II)
- •Хiмiзм процесу:
- •Контрольнi запитання
- •Лабораторна робота 10 феноли Будова, iзомерiя, номенклатура I властивостi
- •Дослiд 10.1. Реакцiя фенолу з хлоридом залiза (III)
- •Дослiд 10.2. Отримання трибромфенолу
- •Хiмiзм процесу:
- •Дослiд 10.3. Сульфування фенолу
- •Хiмiзм процесу:
- •Дослiд 10.4. Кольоровi реакцiї багатоатомних фенолiв
- •Контрольнi запитання
- •Лабораторна робота 11 альдегіди і кетони Будова, iзомерiя, номенклатура I властивостi
Лабораторна робота 7 ароматичнi сполуки Будова, iзомерiя, номенклатура I властивостi
Ароматичними вуглеводнями (аренами) називаються бензол i його похiднi. Останнi можуть мати в молекулi одне або декiлька ядер. Характеризуються при-сутнiстю в циклах спряженої системи iз (4n+2) електронiв, де n=1, 2, 3 i т.д. Роз-ташовуються вуглецевi атоми в циклах в однiй площинi (компланарнiсть), що забез-печує значний ефект спряження в молекулi.
Найпростiший ароматичний вуглеводень - бензол С6Н6, формула його будови зображується по-рiзному:
-

або

або
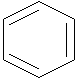
Двi першi формули пiдкреслюють рiвномiрнiсть розподiлу електронної густини в кiльцi бензолу, остання - (формула Кекуле) - зручна для зображення зрушення електронних густин в кiльцi й традицiйно часто використовується. Загальна формула вуглеводнiв ряду бензолу - СnH2n+6.
Гомологи бензолу мають емпiричнi i рацiональнi назви, похiднi вiд бензолу. Похiднi бензолу мають три iзомери, якi називаються орто- або 1,2; мета- або 1,3; пара- або 1,4-iзомер. Тризамiщеннi з однаковими замiщувач мають також три iзомери з такими назвами: рядовий (ряд), несиметричний (несим) i симетричний (s - або сим), наприклад:
|
|
|
|
||
метилбензол, толуол, фенілметан |
1,2-диметилбензол, орто- або о-ксилол |
1,3-диметилбензол, мета- або м-ксилол |
1,4-диметилбензол, пара- або п-ксилол |
||
|
|
|
|||
1,2,3-триметилбензол (ряд-) |
1,2,4-триметилбензол (несим-) |
1,3,5- триметилбензол (сим-) |
|||
Останнiй має також назву мезитилен.
Радикали ароматичних вуглеводнiв (аренiв) мають загальну назву арили (Ar), наприклад:
|
або С6Н5 -; |
|
або С6Н4 -; |
|
або СН3С6Н4 -; |
|
феніл |
о-фенілен |
о-толіл |
бензил |
|||
Для ароматичних вуглеводнiв характернi смуги поглинання в IЧ-спектрах при 1600-1500 см-1 (С-С) i близько 3030 см-1 (С-Н). В УФ-областi присутнi двi смуги поглинання: близько 200 та 260 см-1. Остання найбiльш характерна (“смуга бензиль-ного поглинання”).
Дослiд 7.1. Синтез бензолу iз бензойнокислого натрiю
Реактиви та матеріали: |
бензойнокислий натрiй, натронне вапно, концентро-вана сiрчана кислота (d = 1,84 г/см3) |
Обладнання: |
пробiрки, газовiдвiдна трубка, пальник |
В суху пробiрку кладуть трохи сумiшi iз бензойнокислого натрiю i натронного вапна (1 : 1). Пробiрку закрiплюють в штативi горизонтально i закривають пробкою з газовiдвiдною трубкою, кiнець якої опускають в iншу пробiрку з водою, охолоджену льодом. Реакцiйну пробiрку нагрiвають в полум’ї пальника. Щоб бензол переходив у приймач, спочатку нагрiвають верхню частину пробiрки, а потiм уже реакцiйну сумiш. Через деякий час у приймачi на поверхнi води з’являється масляниста пляма бен-золу. Пiсля того, як реакцiйна пробiрка охолоне, її вiдкривають. Відчувається запах бензолу.











