
- •1. Введение
- •2. Цель лабораторной работы
- •3. Описание ректификационной установки и режимов ее работы
- •4. Изображение изменения концентраций на тарелке в диаграмме y-X. Кинетическая линия процесса. Коэффициент массопередачи
- •5. Порядок проведения эксперимента и обработка опытных данных
- •5. Содержание отчета о лабораторной работе
- •Вопросы для самоконтроля
4. Изображение изменения концентраций на тарелке в диаграмме y-X. Кинетическая линия процесса. Коэффициент массопередачи
Выделим одну тарелку ректификационной колонны (см. рис. 3.2). На этой тарелке, с организованным сливом жидкости, паровая фаза барботирует через отверстия тарелки в жидкую фазу с изменением концентрации компонента от ун до ук.
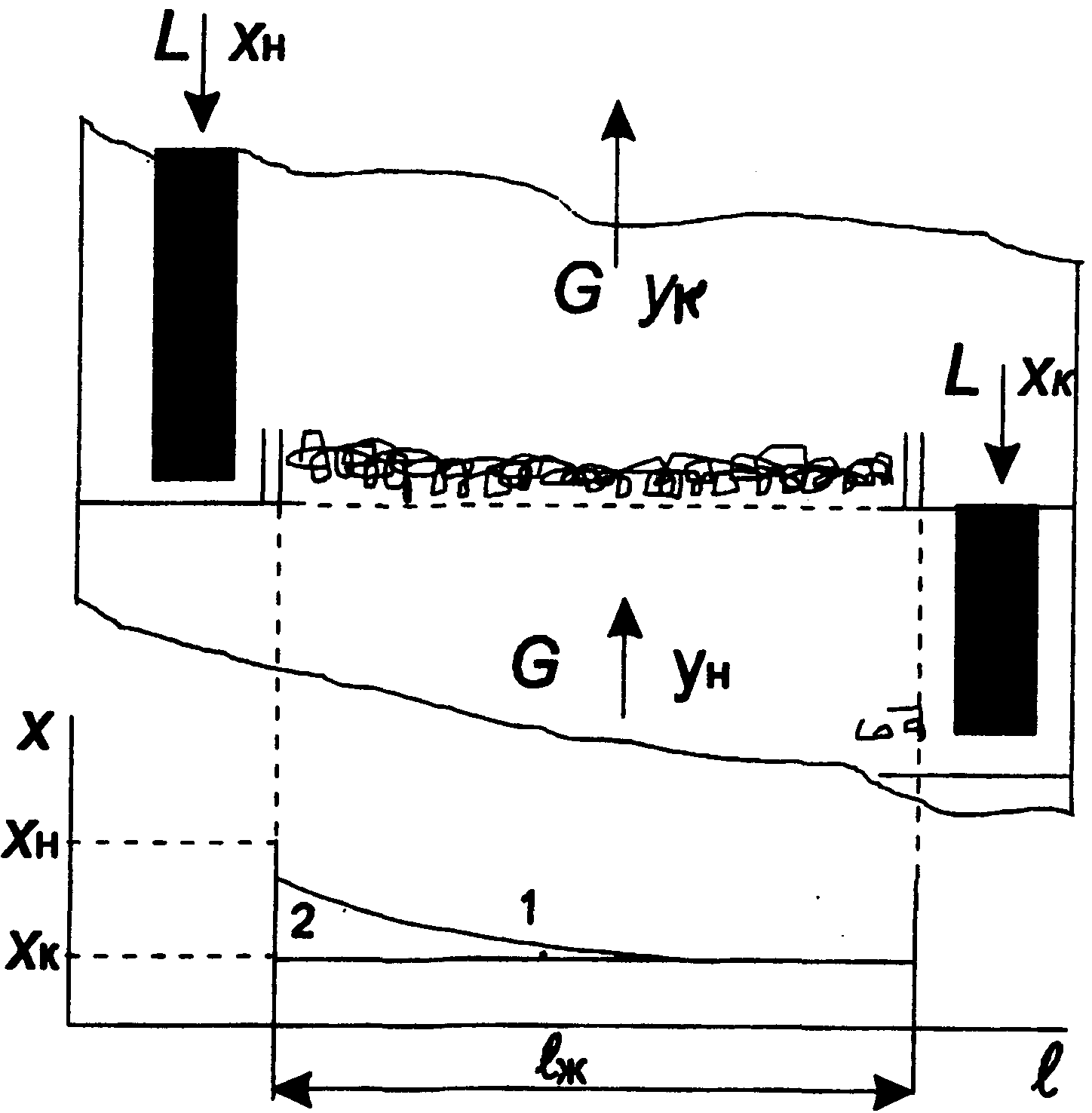
Рис. 3.2. Расчетная схема сетчатой тарелки ректификационной колонны
В свою очередь, жидкая фаза в процессе массообмена изменяет концентрацию от хн до хк Если компонент является легколетучим, то ун < ук, а хк < хн. Принимают, что паровая фаза идеально вытесняется, а концентрация легколетучего компонента в ней монотонно увеличивается от ун до ук. На тарелках промышленных размеров существует градиент концентраций компонента в жидкой фазе вдоль пути ее движения от приемного кармана к сливному (кривая 1, рис. 3.2). Однако в целях упрощения расчета принимают, что жидкая фаза идеально перемешана на тарелке, концентрация легколетучего компонента скачком меняется на входе от хн до хк и на всем пути Lж движения жидкости хк не меняется (линия 2, рис. 3.2).
При взаимодействии фазы на тарелке не достигают равновесное состояние. Изменение концентраций фаз на тарелке может быть представлено графически для бинарной смеси (ступень "Т", рис. 3.3). Соответственно изменение концентраций на верхней тарелке выразится как ступень "В", а нижней - "Н". Кривая, соединяющая точки В, В' В" называется кинетической линией процесса, показывает степень недостижения равновесия и отвечает уравнению связи ук и хк для каждой тарелки. На рис. 3.3 нанесены также линии связи равновесных концентраций у = f(x) и рабочая у = Ax + В, отвечающая условию материального баланса и связывающая на любой тарелке ун и хк.
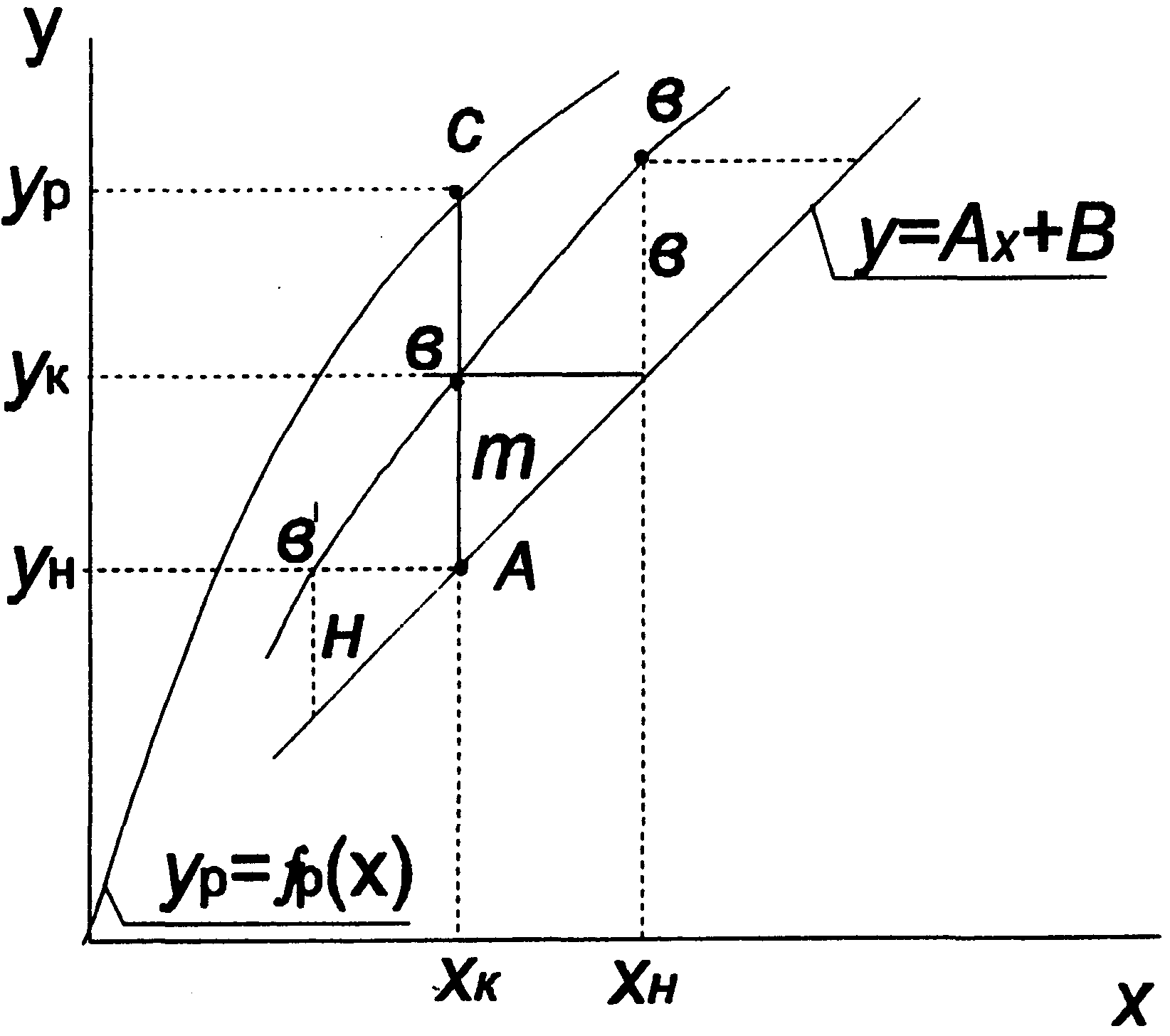
Рис. 3.3. К расчету концентраций фаз на тарелке ректификационной колонны
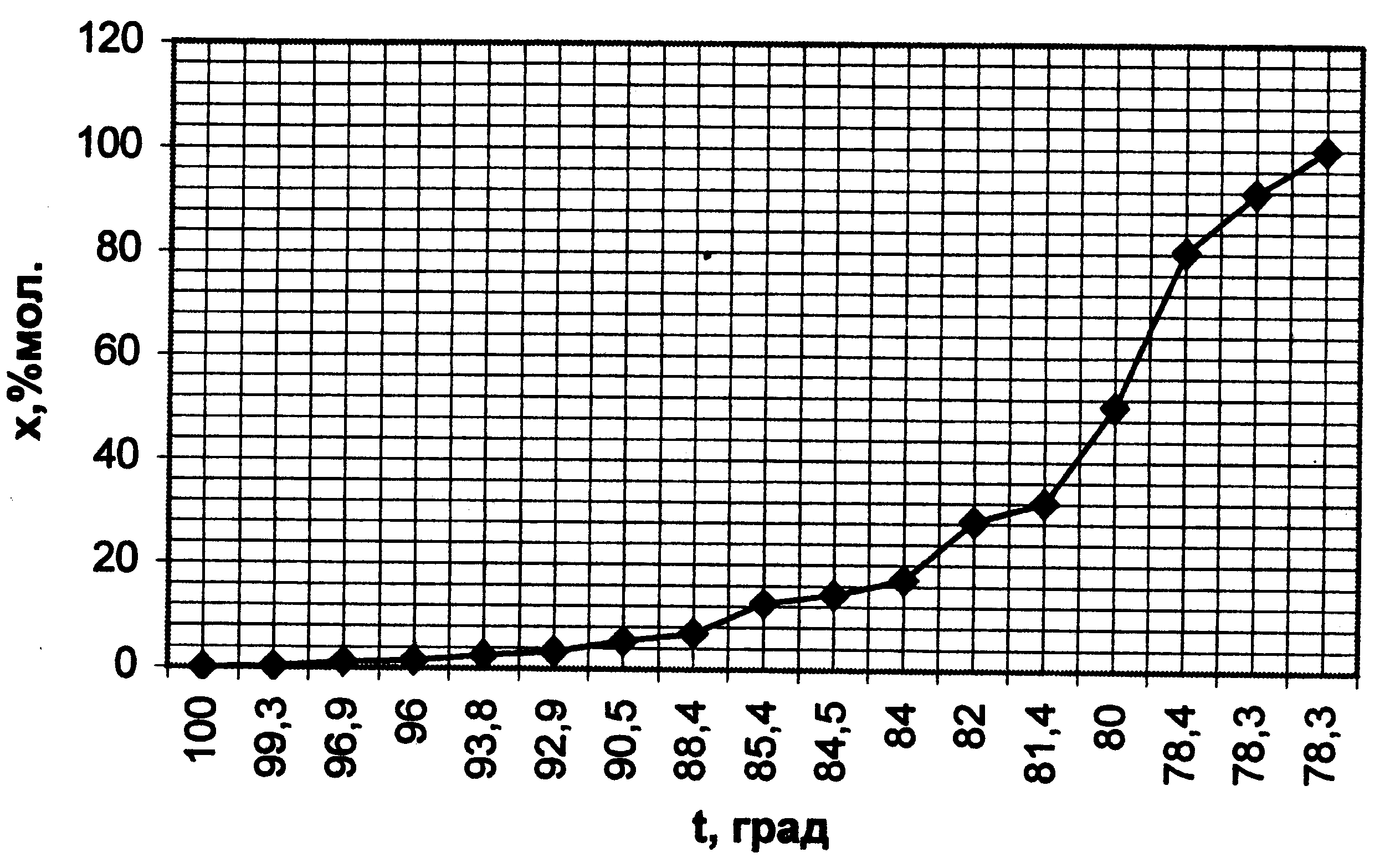
Рис. 3.4. Зависимость температуры кипения смеси от концентрации в ней легкокипящего компонента
При R = ∞ для обогащающей части ректификационной колонны мольный расход паровой фазы G (кг-моль)/ч равен мольному расходу жидкой фазы L (кгмоль)/ч. Из уравнения материального баланса тарелки Т (рис. 3.2)
(ук-ун)=(хн-хк), (3.1)
следует равенство (3.1), которое действительно в случае, когда рабочая линия у = Ax + В лежит на диагонали квадрата диаграммы Y-X. Таким образом в режиме R = ∞ ун = хк, а ук = хн.
Положение кинетической линии процесса ректификации определяется кинетическим коэффициентом процесса - коэффициентом массопередачи ку (кх).
![]()
(3.2)
где Gм - мольный расход паровой фазы, (кг моль)/ч; ук, ун - конечная и начальная концентрации легколетучего компонента в паровой фазе на тарелке, мол.доля; Fб - площадь барботажа тарелки, м2; kу - коэффициент массопередачи (кг моль)/(м2 ч).
Средняя движущая сила для тарелки Т составляет
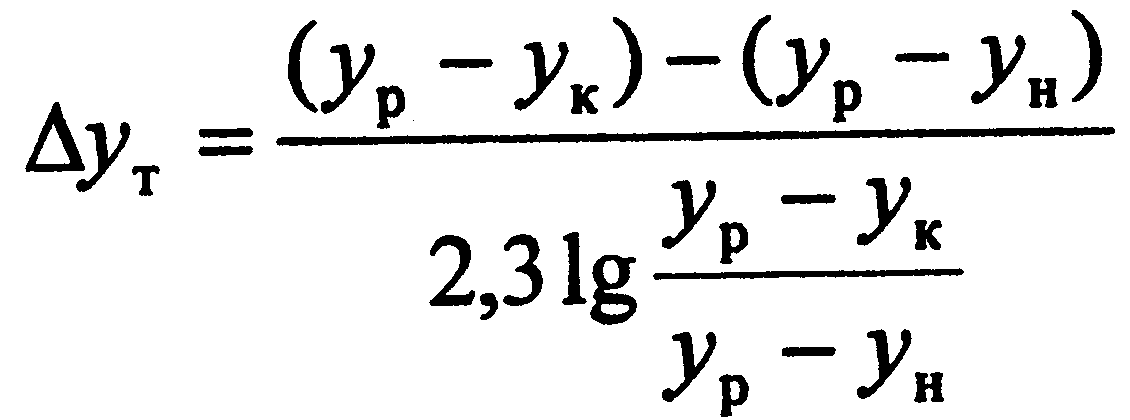
(3.3)
где ур - концентрация легколетучего компонента в паровой фазе, находящейся в равновесии с жидкой фазой состава хк, мол. доли (рис. 3.2). Данные парожидкостного равновесия для смеси этанол-вода приведены в табл. 3.
