
- •Часть I
- •Часть I
- •Оглавление
- •Введение
- •Лабораторно-практическое занятие № 1 Введение в фармацевтическую химию. Понятие о нормативной документации в фармации.
- •Знакомство с правилами безопасной работы в химической лаборатории.
- •Вопросы для обсуждения на семинаре.
- •3. Лабораторная работа Сравнительный анализ фс фармакопей различных стран
- •Лабораторно-практическое занятие № 2 Общие реакции подлинности лекарственных средств различных химических классов
- •1. Вопросы для обсуждения на семинаре.
- •2. Образцы тестовых вопросов:
- •3. Лабораторная работа – 45 мин Общие фармакопейные реакции подлинности
- •Лабораторно-практическое занятие № 3 Оценка качества лекарственных средств по показателю «чистота». Часть 1.
- •Оценка чистоты лекарственных средств: определение допустимых и недопустимых примесей
- •Лабораторно-практическое занятие № 4 Оценка качества лекарственных средств по показателю «чистота». Часть 2.
- •1. Вопросы для обсуждения на семинаре:
- •Решить ситуационные задачи
- •3. Лабораторная работа – 45 мин Оценка качества лекарственных средств по показателю «чистота»
- •Растворимость левомицетина
- •4. Защита лабораторной работы – 30 мин
- •Лабораторно-практическое занятие № 5 Оценка качества лекарственных средств по показателю «количественное определение»
- •Вопросы для обсуждения на семинаре:
- •Решить ситуационные задачи Задача № 1
- •Задача № 2
- •Задача № 3
- •Задача № 4
- •Задача № 5
- •Задача № 6
- •2. Образцы тестовых вопросов:
- •3. Лабораторная работа – 45 мин Количественное определение действующего вещества в лекарственной субстанции титриметрическим методом
- •Лабораторно-практическое занятие № 6 Контрольная работа №1 «Общие вопросы фармацевтической химии»
- •Защита контрольной работы – 90 мин.
- •Лабораторно-практическая работа № 7 Фармацевтический анализ лекарственных средств p-элементов VII группы периодической системы элементов
- •Препараты галогенов
- •Абсорбционный комплекс синего цвета
- •Препараты галогенидов
- •1. Реакции на натрий.
- •Светло-желтый
- •2. Реакции на калий
- •Светло-желтый
- •Семинар - 90 мин
- •Контрольный тест - 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементов VII группы псэ
- •Лабораторно-практическая работа № 8 Фармацевтический анализ лекарственных средств р-элементов
- •VI группы периодической системы элементов
- •Тиосульфат натрия/Natrii thiosulfas
- •1. Семинар - 90 мин
- •Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств р-элементов VI группы
- •Лабораторно-практическое занятие № 9 Фармацевтический анализ лекарственных средств p-элементов V группы периодической системы элементов
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементами V группы периодической системы элементов
- •Лабораторно-практическое занятие № 10 Фармацевтический анализ лекарственных средств р-элементов III-IV групп периодической системы элементов
- •(Бура/ Borax)
- •Семинар - 90 мин
- •Контрольный тест - 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементов III-IV групп
- •Лабораторно-практическое занятие № 11 Контрольная работа № 2 Фармацевтический анализ лекарственных средств p-элементов VII, VI, V, IV, III групп периодической системы элементов
- •1. Контрольный тест - 45 мин
- •2. Подготовка ответа на вопросы билета – 45 мин
- •Решите задачи:
- •3. Защита контрольных работ – 90 мин.
- •Лабораторно - практическое занятие №12 Фармацевтический анализ лекарственных средств s-элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе магния
- •Лекарственные средства на основе кальция
- •Лекарственные средства на основе бария
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс s-элементов I-II групп псэ
- •Лабораторно-практическое занятие № 13 Фармацевтический анализ лекарственных средств d-элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе серебра
- •Коллоидные препараты серебра
- •Лекарственные средства на основе цинка
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс d- элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе железа
- •Лекарственные средства на основе платины
- •Радиофармацевтические препараты
- •Гомеопатические лекарственные средства
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс d-элементов VIII группы псэ
- •Лабораторно-практическое занятие № 16 Фармацевтический анализ лекарственных средств – галогенпроизводных углеводородов, спиртов, простых и сложных эфиров
- •Лекарственные средства – галогенопроизводные ациклических алканов
- •Лекарственные средства на основе спиртов
- •Лекарственные средства на основе эфиров
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств на основе спиртов
- •Лабораторно-практическое занятие № 17 Фармацевтический анализ лекарственных средств альдегидов и углеводов
- •Лекарственные средства альдегидов
- •Лекарственные средства на основе углеводов
- •1. Семинар - 90 мин
- •2.Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лс альдегидов и углеводов
- •Лабораторно-практическое занятие № 18 Итоговое занятие
- •Приложение 1 Правила безопасной работы в лаборатории
- •Частные фармакопейные статьи к лабораторно-практическому занятию№1
- •Приложение 2 Общие фармакопейные статьи (Государственная фармакопея XI) определение температуры плавления
- •Определение температурных пределов перегонки
- •Определение плотности
- •Растворимость
- •Определение показателя преломления (рефрактометрия)
- •Определение оптического вращения (поляриметрия)
- •Определения, основанные на измерении поглощения электромагнитного излучения
- •Спектрофотометрия
- •Спектрофотометрия в ультрафиолетовой и видимой областях
- •Определение степени белизны порошкообразных лекарственных средств
- •Определение рН
- •Определение окраски жидкостей
- •Определение прозрачности и степени мутности жидкостей
- •Приложение 3 Оценка качества лс по показателю «чистота», «количественное определение».
- •В лекарственных препаратах
- •Приложение 4 Частные фармакопейные статьи для лс р-элементов VII группы псэ (ер, перевод с английского)
- •Калия бромид (Kalii Bromidum)
- •Калия йодид (Kalii iodidum)
- •Натрия бромид ( Natrii Bromidum)
- •Натрия йодид ( Natrii iodidum)
- •Натрия фторид (Natrii fluoridum)
- •Натрия хлорид (Natrii chloridum)
- •Вода очищенная в резервуарах
- •Вода для инъекций (Aqua pro injectionibus)
- •Стерильная вода для инъекций
- •Раствор водорода пероксида (3%) (Solutio Hydrogenii peroxydi 3%)
- •Магния пероксид (Magnesii peroxydum)
- •Натрия тиосульфат (Natrii thiosulfas)
- •Натрия тетраборат (Natrii tetraboras) (Бура Borax)
- •Алюминия гидроксид (Aluminii hydroxidum)
- •Алюминия фосфат (Aluminii рhosphaS)
- •Натрия гидрокарбонат (Natrii hydrocarbonas)
- •Лития карбонат (Lithii carbonas)
- •Кальция хлорид (Сalcii chloridum)
- •Бария сульфат для рентгеноскопии (barii sulfas pro roentgeno)
- •Магния сульфат (Magnesii sulfas)
- •Магния оксид (Magnesii oxidum)
- •Серебра нитрат (Argenti nitras)
- •Цинка оксид (Zinci oxydum)
- •Цинка сульфат (Zinci sulfas)
- •Железа глюконат
- •Железа фумарат
- •Цисплатин (Cisplatinum)
- •Йодированный [I 125] альбумин для инъекций, меченный.
- •Натрия йодида [i131] раствор
- •Приложение 12 Частные фармакопейные статьи для лс галогенпроизводных углеводородов, спиртов, простых и сложных эфиров
- •Приложение 13 Частные фармакопейные статьи для лс альдегидов и углеводов
1. Семинар - 90 мин
Вопросы для обсуждения:
Методы получения и характеристика физических свойств ЛС галогенопроизводных углеводородов, спиртов, простых и сложных эфиров.
Обсуждение фармакопейных и нефармакопейных реакций подлинности ЛС галогенопроизводных углеводородов, спиртов, простых и сложных эфиров.
Оценка чистоты и определение примесей ЛС галогенопроизводных углеводородов, спиртов, простых и сложных эфиров.
Методики количественного определения ЛС галогенопроизводных углеводородов, спиртов, простых и сложных эфиров.
Применение ЛС галогенопроизводных углеводородов, спиртов, простых и сложных эфиров.
2. Контрольный тест – 15 мин
Образцы тестовых вопросов:
Какие реакции определения подлинности ЛС «Спирт этиловый» используют в фармакопейном анализе?
Какие реакции определения подлинности ЛС «Глицерин» используют в фармакопейном анализе?
Что является недопустимой примесью в ЛС «Глицерин»?
Каким методом проводят количественное определение ЛС «Глицерин»?
Применение ЛС «Глицерин».
Применение ЛС «Спирт этиловый».
По каким физическим константам устанавливают подлинность ЛС «Эфир медицинский»?
С помощью какой реакции определяют примесь пероксидов в ЛС «Эфир медицинский»?
Что является причиной взрывоопасности диэтилового эфира?
При каких условиях следует хранить ЛС «Эфир для наркоза»?
Какие реакции определения подлинности ЛС «Нитроглицерин» используют в фармакопейном анализе?
Применение ЛС «Нитроглицерин»?
Каким методом проводят перевод ковалентно связанных хлоридов в ионное состояние, при анализе ЛС «Хлористый этил»?
Как осуществляют определение подлинности галотана?
Испытания на чистоту ЛС «Хлористый этил».
Дайте описание фторотана согласно ФС.
Дайте описание хлористого этила согласно ФС.
Какие испытания на чистоту ЛС «Галотан» надо проводить?
Что наблюдается при добавлении фторотана к концентрированной серной кислоте?
Примегнение ЛС «Хлористый этил».
Применение ЛС «Фторотан».
Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств на основе спиртов
Задание 1.
Провести фармацевтический анализ этилового спирта по показателям:
Описание
Подлинность
А. Проведите реакцию образования этилацетата.
В пробирку поместите 4 капли этанола и 5 капель уксусной кислоты. Добавьте 3 капли концентрированной серной кислоты и осторожно нагрейте смесь до кипения. Через несколько секунд появляется характерный приятный запах этилацетата.
Б. Проведите реакцию образования йодоформа.
В пробирку поместите 1 каплю раствора препарата, добавьте 3 капли 10 % раствора гидроксида натрия и 3 капли водного раствора иода в иодиде калия. Через несколько минут образуется желтоватый осадок йодоформа, обладающий стойким характерным запахом.
В. Проведите реакцию окисления этанола дихроматом калия (ЕР).
В пробирку поместите 2 капли этанола, 2 капли 5 % раствора дихромата калия и 1 каплю 10% раствора серной кислоты. Полученный оранжевый раствор слегка нагрейте над пламенем горелки до начала изменения цвета. Обычно уже через несколько секунд появляется зеленоватая окраска, характерная для растворов, содержащих фиолетовый иона хрома (Ш) и оранжевый дихромат-анион. Одновременно ощущается запах ацетальдегида (запах прелых антоновских яблок).
Чистота
А. Примесь альдегидов.
К смеси 1,0 мл препарата, 1,0 мл воды и 0,1 мл раствора нитрата серебра прибавляют по каплям раствор аммиака до исчезновения образующегося вначале осадка. Смесь должна оставаться бесцветной и прозрачной при стоянии в темном месте в течение 12 часов.
Б. Примесь сивушных.
Полоску фильтровальной бумаги смачивают смесью, состоящей из 1,0 мл препарата, 0,5 мл воды и 0,1 мл глицерина. После испарения жидкости не должен ощущаться посторонний запах.
В. Примесь дубильных и других экстрактивных веществ
К 0,4 мл препарата прибавляют 0,08 мл раствора аммиака: не должна появляться окраска.
Г. Примесь метилового спирта (Описать теоретически)
К 0,5 мл препарата, отмеренным пипеткой и помещенным в коническую колбу емкостью 50 мл. прибавляют из пипетки 4,5 мл воды, встряхивают и через 5 минут добавляют 2 мл раствора перманганат калия в фосфорной кислоте. Через 10 минут добавляют по каплям насыщенный раствор бисульфита натрия до обесцвечивания раствора и 1 мл свежеприготовленного 2% раствора динатриевой соли хромотроповой кислоты. Затем постепенно добавляют 10 мл концентрированной серной кислоты (порциями по 1 мл с интервалом в 1 минуту) и перемешивают; не должно быть фиолетового окрашивания.
Задание 2.
Определите неизвестную концентрацию этилового спирта рефрактометрическим способом, используя таблицу 1 и пример определения концентрации спирта, приведенные в конце лабораторной работы.
Задание 3.
Провести фармацевтический анализ глицерина по показателям:
Описание
Подлинность
А. Смешайте 1 мл глицерина с 0,5 мл азотной кислоты и добавьте 0,5 мл 10,6% (масс.) раствора дихромата калия. На границе раздела фаз должно наблюдаться голубое кольцо, а затем появляется голубое окрашивание, сохраняющееся в течение 10 минут.
Б. Нефармакопейная реакция подлинности: в пробирку поместите 2 капли 2 % раствора сульфата меди и 5 капель 10 % раствора гидроксида натрия. Образуется голубой студенистый осадок гидроксида меди (II). Добавьте 3 капли глицерина и встряхните содержимое пробирки. Осадок гидроксида меди переходит в раствор, который приобретает интенсивный синий цвет.
Результаты оформите в виде таблицы:
Лабораторная работа №16 Фармацевтический анализ лекарственных средств на основе спиртов |
|
«__»______201.. г
|
|
Русское название ЛС в соответствии с требованиями IUPAС, синонимы |
|
Латинское название ЛС |
|
Химическая формула |
|
Физические свойства (агрегатное состояние, цвет, растворимость) |
|
Реакции подлинности (условия проведения, наблюдаемый эффект, уравнения) |
|
Определение примесей (условия проведения, наблюдаемый эффект, уравнения) |
|
Количественное определение (условия проведения, наблюдаемый эффект, уравнения) |
|
Выводы |
|
Оценка и подпись руководителя |
|
Таблица 16-4.
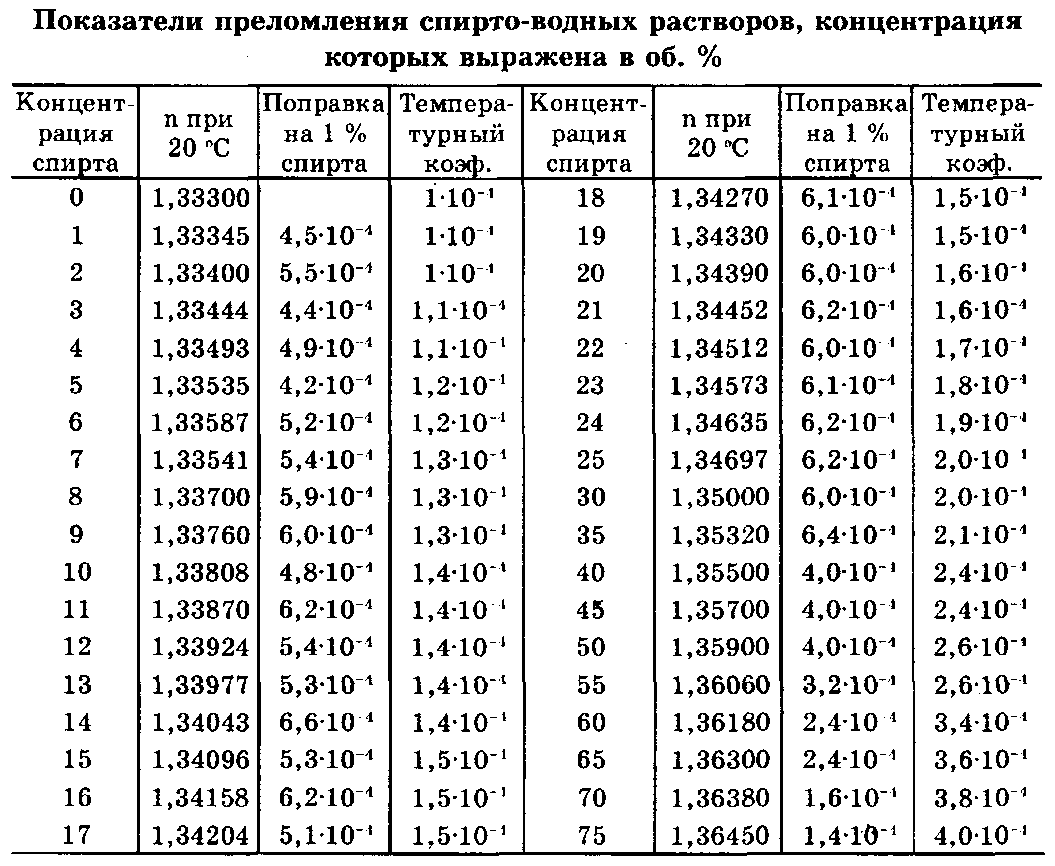
Пример. Анализу подвергался 40 % -ный раствор спирта. Определение показателя преломления проводили при 23 °С. Показание рефрактометра — 1,3541. Согласно табл. 1 поправка на 1 °С для показателя преломления, близкого по величине к полученному (1,35500), равна 2,4•10-4 (т. е. 0,00024). Поскольку исследование проводилось при 23 °С, то поправка будет составлять 0,00024 • 3 = 0,00072. Показатель преломления, приведенный к 20 °С, равен 1,3541 + 0,00072 = 1,35482.
По табл. 1 определяют соответствующую данному показателю преломления концентрацию спирта. Найденной величины показателя преломления (1,35482) в таблице нет; близкому по величине показателю преломления 1,35500 соответствует 40 % спирта. Необходимо определить, какая концентрация спирта соответствует разности показателей преломления: 1,35500 - 1,35482 = 0,00018. Поправка на 1 % спирта равна 4,0 •10 -4. Следовательно, 0,00018/0,0004 = 0,45%. Таким образом, истинное содержание спирта в исследуемом растворе 39,55 % (40 - 0,45).
4. Защита лабораторной работы – 30 мин.
Домашнее задание для подготовки к лабораторно-практическому занятию №17 «Фармацевтический анализ лекарственных средств на основе альдегидов и углеводов»:
Учебное пособие по фармацевтической химии под редакцией проф. Арзамасцева А. П.: Москва «ГЭОТАР-Медиа» 2006. - С:54-56, 58-63, 66-72, 75-84.
Беликов В. Г. Фармацевтическая химия - Пятигорск – 2003. – С.:167-182.
Конспект лекций.
