
- •Часть I
- •Часть I
- •Оглавление
- •Введение
- •Лабораторно-практическое занятие № 1 Введение в фармацевтическую химию. Понятие о нормативной документации в фармации.
- •Знакомство с правилами безопасной работы в химической лаборатории.
- •Вопросы для обсуждения на семинаре.
- •3. Лабораторная работа Сравнительный анализ фс фармакопей различных стран
- •Лабораторно-практическое занятие № 2 Общие реакции подлинности лекарственных средств различных химических классов
- •1. Вопросы для обсуждения на семинаре.
- •2. Образцы тестовых вопросов:
- •3. Лабораторная работа – 45 мин Общие фармакопейные реакции подлинности
- •Лабораторно-практическое занятие № 3 Оценка качества лекарственных средств по показателю «чистота». Часть 1.
- •Оценка чистоты лекарственных средств: определение допустимых и недопустимых примесей
- •Лабораторно-практическое занятие № 4 Оценка качества лекарственных средств по показателю «чистота». Часть 2.
- •1. Вопросы для обсуждения на семинаре:
- •Решить ситуационные задачи
- •3. Лабораторная работа – 45 мин Оценка качества лекарственных средств по показателю «чистота»
- •Растворимость левомицетина
- •4. Защита лабораторной работы – 30 мин
- •Лабораторно-практическое занятие № 5 Оценка качества лекарственных средств по показателю «количественное определение»
- •Вопросы для обсуждения на семинаре:
- •Решить ситуационные задачи Задача № 1
- •Задача № 2
- •Задача № 3
- •Задача № 4
- •Задача № 5
- •Задача № 6
- •2. Образцы тестовых вопросов:
- •3. Лабораторная работа – 45 мин Количественное определение действующего вещества в лекарственной субстанции титриметрическим методом
- •Лабораторно-практическое занятие № 6 Контрольная работа №1 «Общие вопросы фармацевтической химии»
- •Защита контрольной работы – 90 мин.
- •Лабораторно-практическая работа № 7 Фармацевтический анализ лекарственных средств p-элементов VII группы периодической системы элементов
- •Препараты галогенов
- •Абсорбционный комплекс синего цвета
- •Препараты галогенидов
- •1. Реакции на натрий.
- •Светло-желтый
- •2. Реакции на калий
- •Светло-желтый
- •Семинар - 90 мин
- •Контрольный тест - 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементов VII группы псэ
- •Лабораторно-практическая работа № 8 Фармацевтический анализ лекарственных средств р-элементов
- •VI группы периодической системы элементов
- •Тиосульфат натрия/Natrii thiosulfas
- •1. Семинар - 90 мин
- •Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств р-элементов VI группы
- •Лабораторно-практическое занятие № 9 Фармацевтический анализ лекарственных средств p-элементов V группы периодической системы элементов
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементами V группы периодической системы элементов
- •Лабораторно-практическое занятие № 10 Фармацевтический анализ лекарственных средств р-элементов III-IV групп периодической системы элементов
- •(Бура/ Borax)
- •Семинар - 90 мин
- •Контрольный тест - 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс р-элементов III-IV групп
- •Лабораторно-практическое занятие № 11 Контрольная работа № 2 Фармацевтический анализ лекарственных средств p-элементов VII, VI, V, IV, III групп периодической системы элементов
- •1. Контрольный тест - 45 мин
- •2. Подготовка ответа на вопросы билета – 45 мин
- •Решите задачи:
- •3. Защита контрольных работ – 90 мин.
- •Лабораторно - практическое занятие №12 Фармацевтический анализ лекарственных средств s-элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе магния
- •Лекарственные средства на основе кальция
- •Лекарственные средства на основе бария
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс s-элементов I-II групп псэ
- •Лабораторно-практическое занятие № 13 Фармацевтический анализ лекарственных средств d-элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе серебра
- •Коллоидные препараты серебра
- •Лекарственные средства на основе цинка
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс d- элементов I-II групп периодической системы элементов
- •Лекарственные средства на основе железа
- •Лекарственные средства на основе платины
- •Радиофармацевтические препараты
- •Гомеопатические лекарственные средства
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лс d-элементов VIII группы псэ
- •Лабораторно-практическое занятие № 16 Фармацевтический анализ лекарственных средств – галогенпроизводных углеводородов, спиртов, простых и сложных эфиров
- •Лекарственные средства – галогенопроизводные ациклических алканов
- •Лекарственные средства на основе спиртов
- •Лекарственные средства на основе эфиров
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств на основе спиртов
- •Лабораторно-практическое занятие № 17 Фармацевтический анализ лекарственных средств альдегидов и углеводов
- •Лекарственные средства альдегидов
- •Лекарственные средства на основе углеводов
- •1. Семинар - 90 мин
- •2.Контрольный тест – 15 мин
- •Лабораторная работа – 45 мин Фармацевтический анализ лс альдегидов и углеводов
- •Лабораторно-практическое занятие № 18 Итоговое занятие
- •Приложение 1 Правила безопасной работы в лаборатории
- •Частные фармакопейные статьи к лабораторно-практическому занятию№1
- •Приложение 2 Общие фармакопейные статьи (Государственная фармакопея XI) определение температуры плавления
- •Определение температурных пределов перегонки
- •Определение плотности
- •Растворимость
- •Определение показателя преломления (рефрактометрия)
- •Определение оптического вращения (поляриметрия)
- •Определения, основанные на измерении поглощения электромагнитного излучения
- •Спектрофотометрия
- •Спектрофотометрия в ультрафиолетовой и видимой областях
- •Определение степени белизны порошкообразных лекарственных средств
- •Определение рН
- •Определение окраски жидкостей
- •Определение прозрачности и степени мутности жидкостей
- •Приложение 3 Оценка качества лс по показателю «чистота», «количественное определение».
- •В лекарственных препаратах
- •Приложение 4 Частные фармакопейные статьи для лс р-элементов VII группы псэ (ер, перевод с английского)
- •Калия бромид (Kalii Bromidum)
- •Калия йодид (Kalii iodidum)
- •Натрия бромид ( Natrii Bromidum)
- •Натрия йодид ( Natrii iodidum)
- •Натрия фторид (Natrii fluoridum)
- •Натрия хлорид (Natrii chloridum)
- •Вода очищенная в резервуарах
- •Вода для инъекций (Aqua pro injectionibus)
- •Стерильная вода для инъекций
- •Раствор водорода пероксида (3%) (Solutio Hydrogenii peroxydi 3%)
- •Магния пероксид (Magnesii peroxydum)
- •Натрия тиосульфат (Natrii thiosulfas)
- •Натрия тетраборат (Natrii tetraboras) (Бура Borax)
- •Алюминия гидроксид (Aluminii hydroxidum)
- •Алюминия фосфат (Aluminii рhosphaS)
- •Натрия гидрокарбонат (Natrii hydrocarbonas)
- •Лития карбонат (Lithii carbonas)
- •Кальция хлорид (Сalcii chloridum)
- •Бария сульфат для рентгеноскопии (barii sulfas pro roentgeno)
- •Магния сульфат (Magnesii sulfas)
- •Магния оксид (Magnesii oxidum)
- •Серебра нитрат (Argenti nitras)
- •Цинка оксид (Zinci oxydum)
- •Цинка сульфат (Zinci sulfas)
- •Железа глюконат
- •Железа фумарат
- •Цисплатин (Cisplatinum)
- •Йодированный [I 125] альбумин для инъекций, меченный.
- •Натрия йодида [i131] раствор
- •Приложение 12 Частные фармакопейные статьи для лс галогенпроизводных углеводородов, спиртов, простых и сложных эфиров
- •Приложение 13 Частные фармакопейные статьи для лс альдегидов и углеводов
Лекарственные средства на основе цинка
Цинк является эссенциальным микроэлементом. Его содержание в организме человека в среднем составляет 1,5-3,0 г.
Ион цинка прочно связывается с большинством органических лигандов металлоферментов. Ионы цинка необходимы для функционирования различных ферментов, таких как термолизин, дипептидазы, щелочная фосфатаза, РНК-полимераза, ДНК-полимераза, супероксиддисмутаза. Цинк является незаменимым компонентом активного центра фермента карбоангидразы. При удалении цинка фермент теряет каталитическую активность. Именно благодаря цинку, содержание которого в ферменте очень небольшое – 0,33%, образующийся в тканях диоксид углерода превращается в угольную кислоту. Затем в легких идет процесс дегидратации угольной кислоты. Таким образом, эта обратимая реакция влияет на процесс дыхания.
Применение соединений цинка в медицине основано на том, что цинк образует соединения с белками — альбуминаты, которые, в зависимости от концентрации цинка, обладают слабовяжущим или резко прижигающим действием.
Цинка оксид / Zinci oxydum
ZnO Mr 81,4
Содержание действующего вещества в субстанции должно составлять не менее 99,0% и не более 100,5%.
Определение подлинности
При прокаливании порошок ZnO приобретает жёлтую окраску, охлаждении - белую.
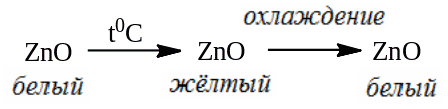
0,1 г субстанции растворяют в 1,5 мл разведенной HCl, и добавляют 5 мл воды. Раствор даёт характерные реакции на ионы Zn2+:
к полученному раствору добавляют 0,2 мл концентрированного раствора NaOH, образуется белый осадок.
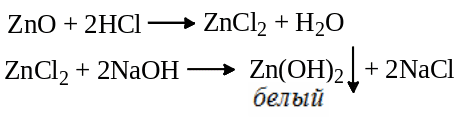
Далее добавляют 2 мл концентрированного раствора NaOH – осадок растворяется.
![]()
Затем добавляют 10 мл раствора аммония хлорида – раствор остаётся прозрачным, образуется комплексный аммиакат цинка.
![]()
Далее добавляют 0,1 мл раствора натрия сульфида, образуется белый осадок.

при взаимодействии с раствором калия гексационоферратом (II) растворы солей цинка образуют белый осадок, нерастворимый в кислотах, но растворимый в щелочах:
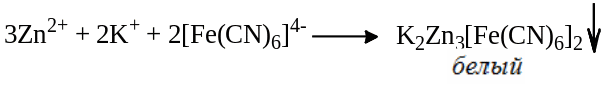
Оценка чистоты
Щелочность определяют индикаторным методом: 1,0 г субстанции взбалтывают с 10 мл кипящей воды. Добавляют 0,1 мл фенолфталеина и фильтруют. Если фильтрат окрашен в красный цвет, то при добавлении не более чем 0,3 мл 0,1 моль/л раствора HCl цвет индикатора должен измениться.
Контролируют содержание карбонатов и примесей нерастворимых в кислотах:1,0 г субстанции растворяют в 15 мл разведенной HCl - не должно наблюдаться выделения пузырьков газа, полученный раствор должен быть бесцветным и его опалесценция не должна быть интенсивнее опалесценции эталона сравнения.
Допустимыми примесями являются мышьяк, кадмий железо, свинец.
Мышьяк определяют методом Гутцайта, его содержание не должно превышать 5 ppm в навеску массой 0,2 г.
Содержание кадмия (не более 10,0 ppm) и свинца (не более 50,0 ppm) определяют методом атомно-адсорбционной спектрофотометрии.
Для обнаружения примесей ионов железа (не более 200 ppm) 50 мг субстанции растворяют в 1 мл разведенной HCl и добавляют 9 мл воды. К полученному раствору добавляют 2 мл 200 г/л раствора лимонной кислоты и 0,5 мл раствора тиогликолевой кислоты. Перемешивают, подщелачивают раствором аммиака, и доводят объём смеси водой до 20 мл. При наличии примесей ионов железа появляется розовое окрашивание.
Потеря в массе при прокаливании до постоянной массы при 500±500С не должна быть более 1,0% для навески 1,00 г.
Количественное определение проводят методом комплексонометрии.
Субстанцию массой 0,150 г растворяют в 10 мл разбавленной CH2COOH, и доводят водой до 200 мл. Добавляют 50 мг ксиленового оранжевого и раствор гексаметилентетрамина, раствор становится красно-фиолетового цвета.
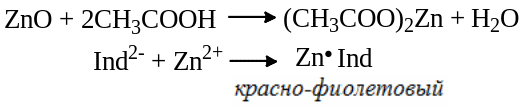
Титруют 0,1 моль/л раствором ЭДТА (динатриевая соль этилендиаминтетрауксусной кислоты, трилон Б).
![]()
В точке эквивалентности протекает конкурирующая реакция образования более прочного координационного соединения иона металла с этилендиаминтетраацетат-ионом и переход окраски в желтую.
![]()
1 мл 0,1 моль/л ЭДТА эквивалентен 8,14 мг ZnO.
Цинка сульфат гептагидрат / Zinci sulfas heptahydricus
ZnSO4∙7H2O Mr 287,5
Содержание действующего вещества в субстанции должно составлять не менее 99,0% и не более 104,0%.
Определение подлинности
5% водный раствор субстанции даёт характерные реакции на сульфат ионы и ионы цинка.
Оценка чистоты
5% водный раствор субстанции должен быть прозрачным и бесцветным, и его рН должен находиться в пределах от 4,4 до 5,6.
Допустимыми примесями являются хлориды (не более 300 ppm) и железо (не более 100 ppm).
Количественное определение проводят методом комплексонометрии.
Титрант – 0,1 моль/л раствор ЭДТА. Индикатор – ксиленоловый оранжевый в присутствии гексаметилентетрамина.
1 мл 0,1 моль/л ЭДТА эквивалентен 28,75 мг ZnSO4∙7H2O.
