
- •Перелік умовних скорочень
- •Зв’язок роботи з науковими програмами, планами, темами:
- •Мета дослідження:
- •Завдання дослідження:
- •Практичне значення отриманих результатів:
- •Впровадження результатів досліджень:
- •Особистий внесок пошукача:
- •Апробація результатів роботи:
- •Розділ 1
- •1.1. Етіологічний чинник varicella zoster інфекції
- •1.2. Епідеміологія та контроль за вітряною віспою
- •1.3. Сучасні уявлення про патогенез вітряної віспи
- •1.4. Імунопатогенетичні особливості вітряної віспи
- •1.5. Питання адаптації військовослужбовців
- •1.6. Клінічні прояви вітряної віспи
- •1.7. Сучасна діагностика varicella zoster інфекції
- •1.8. Лікування вітряної віспи у дорослих
- •1.9. Профілактика вітряної віспи
- •Висновки до розділу 1.
- •Розділ 2
- •2.1. Дизайн дослідження та характеристика обстежених хворих
- •2.1.1. Дизайн дослідження, критерії включення / виключення
- •2.1.2. Характеристика обстежених хворих
- •2.2. Характеристика та схеми застосування досліджуваних препаратів
- •2.3. Методи дослідження
- •2.3.1. Клінічна діагностика
- •2.3.2. Лабораторна діагностика
- •Загальний аналіз крові
- •Визначення деяких імунологічних показників
- •Визначення фенотипу лімфоїдних клітин непрямим імунофлуоресцентним методом на проточному цитофлуориметрі
- •Визначення цитокінів методом кількісного імуноферментного аналізу
- •Молекулярно-біологічний метод
- •2.4. Методи статистичного аналізу
- •Висновки до розділу 2.
- •Розділ 3
- •3.1. Епідемічна ситуація з вітряної віспи у Збройних силах України
- •3.2. Клінічні прояви вітряної віспи у військовослужбовців
- •Динаміка захворюваності на вітряну віспу за 5 років
- •Розподіл хворих за ступенем тяжкості перебігу та формою вітряної віспи
- •Динаміка змін загального рівня лейкоцитів та лейкоформули, % (m±m)
- •3.3 Вірусний профіль при вітряній віспі у дорослих хворих
- •3.4. Імунопатогенетичні зміни при вітряній віспі у військовослужбовців
- •3.4.1. Стан клітинної та гуморальної ланки імунної відповіді
- •Динаміка деяких показників гуморальної ланки імунної відповіді (m±m)
- •Динаміка змін показників гуморальної ланки імунної відповіді
- •3.4.2. Стан цитокінової ланки імунітету
- •Показники досліджуваних цитокінів по групам (m±m)
- •Динаміка змін досліджуваних цитокінів по групах
- •3.5. Ускладнення вітряної віспи у дорослих хворих
- •Динаміка виявлення ускладнених форм вітряної віспи за 5 років
- •Взаємозв’язок тривалості висипу та наявності пустулізації*
- •Висновки до розділу 3.
- •Розділ 4
- •4.1. Застосування аміксину у дорослих хворих на вітряну віспу
- •4.1.1 Клінічна ефективність аміксину та особливості вірусного профілю
- •Частота клінічних ознак у хворих на вітряну віспу
- •Динаміка змін лейкограми крові під впливом аміксину (м±m)
- •4.1.2. Імуномодулююча активність аміксину
- •4.1.2.1. Вплив аміксину на основні компоненти клітинного та гуморального імунітету
- •Динаміка імунологічних показників клітинної ланки* при застосуванні аміксину (м±m)
- •Динаміка деяких імунологічних показників гуморальної ланки* при застосуванні аміксину (м±m)
- •4.1.2.2. Вплив аміксину на цитокінову регуляцію імунної відповіді
- •4.1.3. Небажані явища лікування аміксином
- •4.2. Застосування лімфоміозоту з енгістолом у хворих на вітряну віспу
- •4.2.1. Клінічна ефективність лімфоміозоту з енгістолом та особливості вірусного профілю
- •Динаміка змін лейкограми крові
- •4.2.2. Імуномодулююча активність лімфоміозоту та енгістолу
- •4.2.2.1. Вплив лімфоміозоту з енгістолом на основні компоненти клітинного та гуморального імунітету
- •Динаміка деяких імунологічних показників клітинної ланки* при застосуванні антигомотоксичних препаратів (м±m)
- •4.2.2.2. Вплив лімфоміозоту з енгістолом цитокінову регуляцію імунної відповіді
- •Динаміка змін цитокінового профілю, залежно від схеми лікування (м±m)
- •4.2.3. Небажані явища антигомотоксичної терапії
- •Висновки до розділу 4.
- •Розділ 5
- •Нозологічна структура інфекційної захворюваності
- •Аналіз і узагальнення результатів дослідження
- •Висновки
- •Практичні рекомендації
- •Додаток а
- •Додаток б
- •Д одаток в
- •Референтні значення деяких імунологічних показників крові
- •Додаток г
- •Референтні значення деяких цитокінів крові*
- •Додаток д
- •Додаток е Етапи дискримінантного аналізу (скорочено)
- •Список використаних джерел
Динаміка змін загального рівня лейкоцитів та лейкоформули, % (m±m)
Показник |
Показники лейкограми |
|||
М |
m |
Min |
Max |
|
До лікуваня |
||||
Лейкоцити, абс., 109/л |
5,45 |
0,12 |
2,7 |
8,9 |
Лімфоцити, % |
23,68 |
0,89 |
6,3 |
49,9 |
Моноцити, % |
11,24 |
0,31 |
4,1 |
21,6 |
Гранулоцити, % |
65,08 |
0,94 |
35,2 |
87,5 |
Після лікування |
||||
Лейкоцити, абс., 109/л |
6,03 |
0,09 |
4,5 |
8,8 |
Лімфоцити, % |
29,82 |
0,66 |
16,4 |
51,7 |
Моноцити, % |
11,42 |
0,22 |
4,8 |
17,0 |
Гранулоцити, % |
58,83 |
0,65 |
37,4 |
77,5 |
Примітка. М – середня арифметична, m – похибка середньої арифметичної, Min – мінімальне та Max – максимальне значення (тут і надалі – авт.)
Аналіз даних табл. 3.5 показав, що до та після лікування спостерігалась нормальна кількість лейкоцитів (нормоцитоз). Середні значення лімфоцитів (%) відповідали межам лабораторної норми, проте в окремих випадках спостерігалась зниження лімфоцитів (лімфопенія) незалежно від періоду хвороби. Водночас, звертає увагу наявність підвищенних середніх показників моноцитів периферійної крові (моноцитоз) як у хворих з початковими проявами ВВ, так і у реконвалесцентів, що відповідає даним літератури [29, 30].
При дослідженні рівня тромбоцитів виявлено, що до лікування тромбоцитопенія (у середньому 155,98±1,68 х 109/л) відмічалась у 59 зі 135 хворих, що склало 43,70%. Решта 75 (56,30%) хворих мали середній рівень тромбоцитів 224,32±4,56 х 109/л, що відповідало показникам лабораторної норми. Дане свідчить про те, що частина хворих мають підвищений ризик геморагічних ускладнень.
3.3 Вірусний профіль при вітряній віспі у дорослих хворих
Спираючись на загальновизнані дані про схильність ГВІ та власне VZV-інфекції до латентного перебігу, ми припустили, що дорослі хворі з клінічними проявами ВВ можуть мати певні особливості молекулярного патогенезу, які вивчені недостатньо. Останнє втілилось в одну з поставлених задач дослідження, згідно якої ми вивчали вірусний профіль у хворих на ВВ за допомогою ПЛР.
При початковому обстеженні методом ПЛР крові, слини та вмісту везикул (в середньому на 2,0±0,1 добу) та при повторному обстеженні крові й слини (в середньому на 9,8±0,2 добу) у дорослих, хворих на ВВ виявлено ДНК VZV, що лабораторно підтвердило клінічний діагноз (табл. 3.6).
Так, до лікування вміст везикул та слини характеризувався 100-відсотковою навністю ДНК патогену. Водночас, VZV ДНК-емія спостерігалась лише 97 (71,85%) хворих, що було обумовлено особливостями імунопатогенезу інфекції – непостійним рівнем віремії, що збігається з поштовхоподібним розвитком екзантеми. У той же час, за даними аналізу повторного дослідження крові у періоді реконвалесценції ДНК VZV була в 3 (2,22%) хворих.
Таблиця 3.6
Частота вивлення ДНК VZV у різних біологічних рідинах
Досліджувана рідина |
Кількість спостережень (n) |
Кількість позитивних відповідей (n) |
Частота виявлення реплікації, % |
До лікування |
|||
Кров |
135 |
97 |
71,85 |
Слина |
135 |
135 |
100 |
Везикула |
135 |
135 |
100 |
Після лікування |
|||
Кров |
135 |
3 |
2,22 |
Слина |
135 |
89 |
65,93 |
Показники VZV ДНК-емії відрізнялись в дослідних групах (рис. 3.2).

Рис. 3.2. Частота детекції ДНК VZV в крові у % (по групам)
Рис. 3.2 демонструє присутність ДНК VZV в крові, що свідчить про активну реплікацію вірусу та віремію. Високий рівень детекції генетичного матеріалу вірусу від 60,0 до 83,33% на початку лікування відповідає періоду розпалу хвороби (різниця відсотків між І групою та КГ значима, р=0,018). Після лікування також виявлена ДНК VZV в крові, за виключенням хворих КГ, що носило несистемний характер. На нашу думку, різний рівень детекції ДНК VZV в крові при первинному обстеженні може бути пов’язаний з хвилеподібністю віремії або корелювати зі ступінем тяжкості перебігу, що потребує подальшого детального вивчення.
Вірусний профіль до та після лікування за результатами обстеження слини представлений на рис. 3.3.
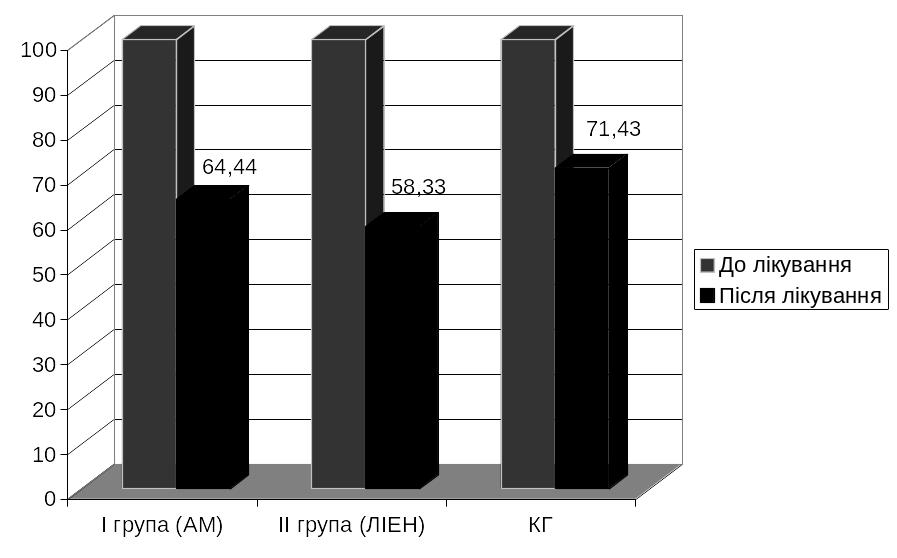
Рис. 3.3. Частота детекції ДНК VZV в слині у % (по групам)
Раніше зазначалось, що до лікування вірусний профіль для слини та вмісту везикул характеризувався наявністю ДНК патогену у 100% хворих з ВВ. При цьому, наявність власне вірусу у вмісті везикул було доведено давно, проте активно дискутується заразність слини та наяв щодо ураження слинних залоз інформації бракувало. На рис. 3.7 показано, що при повторному дослідженні слини хворих з різних груп також визначали ДНК VZV з різною частотою, а найбільший показник був у КГ. Сумарно в 89 (65,92%) хворих на момент виписки зберігалась екскреція ДНК VZV в слині (табл. 3.7), що не доводить виділення вірулентного вірусу, проте теоретично сприяє формуванню резервуару збудника в організованому колективі.
Таблиця 3.7
Зведені частоти вірусологічного результату лікування (по групам)
Результат |
І група (АМ) Абс.(%) |
ІІ група (ЛІЕН) Абс. (%) |
ІІІ група (КГ) Абс. (%) |
Всього по групам |
«-» кров та слина |
15 (33,33) |
18 (37,5) |
12 (28,57) |
45 (33,33) |
«-» кров, «+»слина |
29 (64,44) |
28 (58,33) |
30 (71,43) |
87 (64,44) |
«+» кров, «-»слина |
1 (2,23) |
- |
- |
1 (0,75) |
«+» кров та слина |
- |
2 (4,17) |
- |
2 (1,48) |
Всього |
45 (100%) |
48 (100%) |
42 (100%) |
135 (100%) |
Примітка: різниця відсотків не достовірна (р>0,1).
В результаті аналізу даних табл. 3.7, варто зауважити, що у цілому відсутність ДНК VZV в крові та слині при повторному обстеженні, становила лише у третини всіх хворих. У той же час, дві третини всіх хворих мали уповільнене звільнення біологічних рідин від збудника ВВ – продовження детекції ДНК VZV у слинних залозах було в 64,44%, а VZV ДНК-емія в 2,23% випадків відповідно, що характеризує перебіг основного захворювання у дорослих хворих.
