
- •1 Вопрос:
- •2 Вид: Классы органических соединений
- •2 Вопрос:
- •3 Вопрос:
- •4 Вопрос:
- •5 Вопрос:
- •6 Вопрос:
- •7 Вопрос:
- •8 Вопрос:
- •Получение гликолей.
- •Химические свойства гликолей.
- •1. С галогенводородными кислотами
- •Применение.
- •Тринитрат Глицерина (Тринитроглицерин).
- •Сложные эфиры высших карбоновых кислот (жиры и масла).
- •10 Вопрос:
- •Вопрос 11. Карбонильные соединения. Реакции альдегидов и кетонов, обусловленные активностью атомов водорода при α-углеродном атоме. Альдольная конденсация.
- •12 Вопрос:
- •13 Вопрос:
- •1.Теоретическая часть.
- •1.2. Физические свойства.
- •1.4. Химические свойства карбоновых кислот.
- •1.4.1. Кислотность
- •1.4.2. Превращение карбоновых кислот в функциональные производные
- •1.4.2.1. Галогенангидриды кислот
- •1.4.2.2. Сложные эфиры карбоновых кислот.
- •1.4.2.3. Ангидриды кислот.
- •1.4.2.4. Амиды кислот.
- •1.4.2.5. Нитрилы карбоновых кислот
- •14 Вопрос:
- •15 Вопрос:
- •16 Вопрос:
- •17 Вопрос:
- •18 Вопрос:
- •19 Вопрос:
- •20 Вопрос:
- •21 Вопрос:
- •22 Вопрос:
- •23 Вопрос:
- •26 Вопрос:
- •27 Вопрос:
- •28 Вопрос:
- •29 Вопрос:
- •Кетонное
- •Кислотное
- •30 Вопрос:
- •31 Вопрос:
- •1. Методы получения
Получение гликолей.
Двухатомные спирты можно получать всеми способами получения одноатомных спиртов. Так, например, двухатомные спирты можно получать:
1. Гидролизом дигалогенопроизводных:
СH2Br — CH2 — CH2Br + NaOH (Вод. Среда) = CH2OH —CH2OH + 2HBr
2. Окислением этиленовых углеводородов:
Н2С==СН2 + Н2О + [O] = HOCH2—CH2OH
этилен этиленгликоль
Н2С—СН2 + KMnO4 + H2O = CH2OH — CH2OH + MnO2 + KOH (Реакция Вагнера)
3. Гидратацией оксида этилена:
Н2С==CH2 +Н2О = НОСН2—СН2ОН
4. Через сложные эфиры с их последующим омылением:
СН2Br — CH2Br + 2AgOOCCH3 = CH3COO —CH2 —CH2 —OOCCH3 + 2AgBr
CH3COO — CH2 —CH2 —OOCCH3 +2H2O = CH2OH — CH2OH + 2CH3COOH
5. CH2=CH2 + O2 (Ag) = CH2 — CH2 + H2O = CH2OH — CH2OH
\ /
O
Химические свойства гликолей.
1. С активными металлами:
HO-CH2-CH2-OH + 2Na → H2↑+ NaO-CH2-CH2-ONa
(гликолят натрия)
2. С гидроксидом меди(II) – качественная реакция!
CH2OH — CH2OH +Cu(OH)2 = CH2 – CH2
| |
CH2 CH2
\ /
O
1. С галогенводородными кислотами
HO-CH2-CH2-OH + 2HCl H+↔ Cl-CH2-CH2-Cl + 2H2O
Образование простых эфиров:
СH2OH — CH2OH + C2H5OH [H+] = CH2OH — CH2 - OC2H5 + CH3 — CH2 — OH = C2H5O - CH2 — CH2 – OC2H5 (Диэтиловый эфир этиленгликоля)


Кислотные свойства многоатомных спиртов выше, чем у одноатомных
CH2 – CH2 Стабилизирован засчет индукционного эффекта устойчивость | | повышается, так как он оттягивает себя.
OH O-
Применение
Этиленгликоль производства лавсана, пластмасс, и для приготовления антифризов — водных растворов, замерзающих значительно ниже 0°С (использование их для охлаждения двигателей позволяет автомобилям работать в зимнее время); сырьё в органическом синтезе.
Глицерин.
Глицерин (1,2,3-триоксипентан, пропантриол-1,2,3) - простейший представитель трёхатомныхспиртов. Представляет собой вязкую прозрачную жидкость.
Получение глицерина.
Получение из пропена (2 Метода):
1)
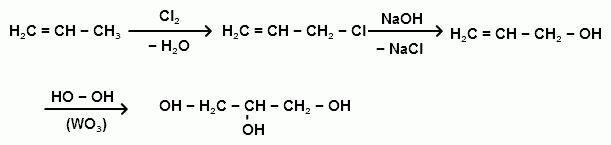
2)
CH2=CH-CH3 + Cl2 -(t=450)-> CH2=CH-CH2-Cl CH2=CH-CH2-Cl + H2O -( в щелочной среде)- > CH2(OH)-CH(Cl)-CH2(OH) + CH2(Cl)-CH(OH)-CH2(OH) CH2(OH)-CH(Cl)-CH2(OH) + H2O -( в щелочной среде)- > CH2(OH)-CH(OH)-CH2(OH)
Получение
гидролизом жиров:
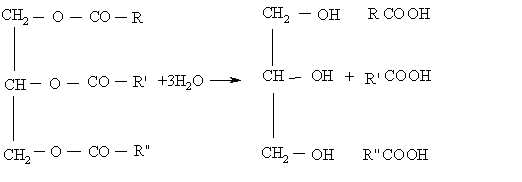
Химические свойства.
С гидроксидом меди(II) – качественная реакция!
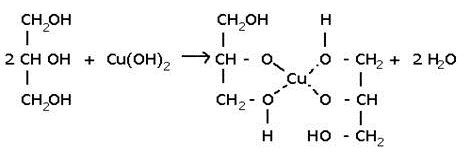
Упрощённая схема
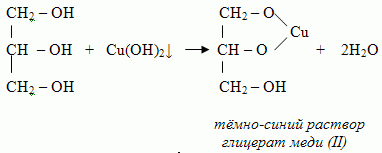
С азотной кислотой
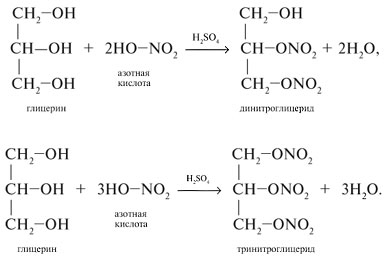
Тринитроглицерид – основа динамита.
Реакция с активными металлами:
CH2-OH CH2-ONa | |
2 CH-OH + 6Na → 2 CH - ONa + 3H2 | | CH2-OH CH2-ONa
Реакция с галогеноводородами.
CH2OH-CHOH-CH2OH + HCl → CH2OH-CHOH-CH2Cl + H2O
