
- •А.Н.Геннадиев, м.А. Глазовская География почв с основами почвоведения
- •Введение почвоведение как отрасль естествознания: история, предмет и задачи
- •Часть I факторы и сущность почвообразования
- •Глава 1
- •Компоненты географической среды как факторы почвообразования
- •Главные горные породы магматического происхождения
- •Основные функции биологического фактора в почвообразовании
- •Лучистая энергия Солнца, атмосферные осадки и воздух как составляющие климатического фактора почвообразования
- •Температура почв на глубине 0,2 м и приземного слоя воздуха в различных областях (по в.Н, Димо)
- •Рельеф — перераспределитель тепла, влаги и твердых масс. Особенности почв и ландшафтов в зависимости от положения в рельефе
- •Локальные и антропогенные факторы почвообразования
- •Глава 2 значение географических факторов в энергетике почвообразования
- •Количество солнечной энергии, участвующей в почвообразовании
- •Глава 3 вклад географических факторов в материальную основу почвообразования
- •Средний химический состав горных пород в долях массы (по а.П. Виноградову)
- •Средний химический состав живых организмов (по а.П. Виноградову)
- •Средний химический состав приземной атмосферы в долях массы на сухой воздух (по ф. Панету и в. Миртову)
- •Глава 4 участие географических факторов в динамике почвообразования
- •Глава 5 почва - многокомпонентная полифакторная открытая биокосная система
- •Морфологические признаки почв
- •Аналитические исследования почв
- •Часть II состав и свойства твердой, жидкой и газовой фаз почвы
- •Глава 6 происхождение и состав минеральной части почвообразующих пород и почв
- •Минеральный и химический состав магматических и метаморфических пород
- •Средний химический состав главных типов изверженных пород, % (по р.А. Дэли)
- •Минеральный и химический состав осадочных пород
- •Главные типы осадочных пород
- •Устойчивость минералов к процессам выветривания
- •Остаточные коры выветривания и коррелятивные им типы аккумулятивных отложений
- •Глава 7 гранулометрический (механический) состав почвообразующих пород и почв Гранулометрические фракции и методы их определения
- •Классификация гранулометрических элементов почвенной массы (по н.А. Качинскому)
- •Классификация почв и пород по гранулометрическому составу (по н.А. Качинскому)
- •Гранулометрический состав почвы
- •Разделение почв по степени дифференциации профиля
- •Минеральные почвенные горизонты
- •Глава 8 органические и органо-минеральные вещества почв Источники органических веществ в почвах и их химический состав
- •Процессы гумификации
- •Гумус почвы. Состав и свойства
- •Влияние факторов почвообразования на образование и накопление гумуса
- •Органо-минеральные соединения и комплексы в почвах
- •Гумусово-аккумулятивные и гумусово-иллювиальные горизонты почв
- •Глава 9 почвенные коллоиды и поглотительная способность почв
- •Физическая адсорбция
- •Физико-химическая поглотительная способность. Строение почвенных коллоидов
- •Физическое состояние коллоидов и его зависимость от состава дисперсионной среды и поглощенных оснований
- •Почвенный поглощающий комплекс
- •Величина емкости обмена глинистых минералов
- •Физическое состояние почвенного поглощающего комплекса в зависимости от состава поглощенных оснований
- •Глава 10 жидкая фаза почв, почвенные растворы
- •Категории, формы и виды почвенной влаги
- •Глава 11 газовая фаза почв. Состав почвенного воздуха
- •Глава 12 окислительно-восстановительные процессы в почвах
- •Глава 13 структурное состояние и физические свойства почв как трехфазного тела
- •Факторы структурообразования
- •Объемная масса, удельная масса и пористость почв
- •Объемная масса суглинистых и глинистых почв (по н.А. Каминскому)
- •Физико-механические свойства почв
- •Часть III классификация почв и почвенно-географическое районирование. Свойства, генезис и география основных типов почв мира
- •Глава 14
- •Принципы генетической классификации почв, картография почв и почвенно- географическое районирование
- •Таксономические единицы и критерии выделения почв
- •Глава 15 почвы полярных и субполярных областей Выветривание и почвообразование в полярных пустынях
- •Дерновые арктотундровые почвы
- •Тундровые глеевые почвы
- •Дерновые субарктические почвы
- •Болотные почвы
- •Глава 16 почвы бореальных и суббореальных лесных областей
- •Подбуры
- •Подзолы
- •Подзолистые почвы
- •Буроземы (или бурые лесные почвы)
- •Поверхностно-глеево-элювиальные почвы
- •Грунтово-глеево-элювиальные почвы
- •Дерново-карбонатные почвы
- •Глава 17 почвы лесо-лугово-степных и степных суббореальных областей
- •Серые лесные почвы
- •Черноземы
- •Каштановые почвы
- •Глава 18 солончаки, солонцы и солоди
- •Солончаки
- •Типы засоления почв по соотношению ионов
- •Солонцы
- •Глава 19 почвы полупустынь и пустынь
- •Бурые пустынно-степные и серо-бурые пустынные почвы
- •Сероземы
- •Годовое поступление органических остатков и зольных элементов в почвы эфемерово-злаково- кустарничковых пустынных степей (по л.Е. Родину и н.И. Базилевич)
- •Такыры и такыровидные почвы
- •Глава 20 почвы переменно-влажных ксерофитно-лесных и саванновых субтропических и тропических областей
- •Коричневые и красно-коричневые почвы
- •Серо-коричневые почвы
- •Слитоземы (вертисоли)
- •Красные и красно-бурые почвы саванн (ферроземы)
- •Глава 21 почвы влажных лесных субтропических, тропических и экваториальных областей
- •Часть IV общие закономерности географии почв и региональная организация почвенного покрова
- •Глава 22 факторы, определяющие общие закономерности географии почв
- •Биоклиматическая зональность почв
- •Литогенная дифференциация почвенного покрова
- •Топогенно - геохимическая сопряженность почв
- •Миграционная способность химических элементов и их соединений (по б.Б. Полынову)
- •Историко-хронологическое разнообразие почвенного покрова
- •Глава 23 структуры почвенного покрова
- •Микроструктуры и мезоструктуры почвенного покрова
- •Основные морфологические типы мезоструктур почвенного покрова (счетания и мозаики)
- •Региональные особенности горизонтальной биоклиматогенной зональности почв
- •Региональные типы вертикальной (горной) биоклиматогенной зональности почв
- •Глава 24 почвенный покров материков и континентов: основные факторы и особенности его организации Почвенный покров Евразии
- •Почвенный покров Северной Америки
- •Почвенный покров Центральной Америки
- •Почвенный покров Южной Америки
- •Почвенный покров Африки
- •Почвенный покров Австралии
- •Часть V современное состояние, мелиорация и охрана почвенных ресурсов
- •Глава 25
- •Функциональная ценность и структура использования почвенных ресурсов
- •Глава 26 состояние почвенных ресурсов и факторы его изменения
- •Увеличение пахотных земель и урожайности в период 1964—1985 гг. (World resourses)
- •Глава 27 социально-экономические факторы охраны почв и почвоохранная политика в россии
- •Литература
- •Оглавление
Устойчивость минералов к процессам выветривания
Степень устойчивости |
Минералы первичные |
Минералы вторичные |
Очень неустойчивые |
Оливин, апатит, анортит |
Галит, мирабилит, гипс и органические соли |
Неустойчивые |
Авгит, роговая обманка, Лабрадор |
Кальцит, арагонит, доломит |
Сред неустойчивые |
Биотит, андезин, гранат, эпидот |
Хлорит, нонтронит, иллит, серицит |
Устойчивые |
Ортоклаз, микроклин, альбит, олигоклаз |
Вермикулит, монтмориллонит, бейделлит |
Наиболее устойчивые |
Кварц, мусковит, циркон, турмалин, рутил, ильменит, анатаз, кианит, титанит, магнетит |
Каолинит, галлуазит, бемит, гиббент, гематит, гетит, лимонит |
ных пустынь. Процессам биохимического выветривания пород и минералов способствуют высокие температуры и влажность, а также обилие органических остатков. Наиболее быстро породы и минералы химически изменяются во влажных субтропиках и тропиках, к умеренным и полярным областям скорость биохимического процесса выветривания уменьшается.
Более быстрому протеканию процессов биохимического выветривания способствует удаление подвижных продуктов распада из выветривающихся пород и почвенной толщи. Поэтому в условиях хорошо дренированного рельефа при обилии осадков выветривание идет быстрее, чем в условиях затрудненного дренажа или аридного климата.
Физическое выветривание горных пород и минералов. Термин «выветривание» не совсем удачен; можно подумать, что в разрушении пород повинен только ветер.
Действительно, местами его роль велика. В пустынях ветром поднимаются и несутся мелкие песчинки, с силой ударяясь о поверхность скал и высверливая в камне маленькие, а затем все более расширяющиеся ячейки; стенки ячеек постепенно истончаются и разрушаются, идет так называемый процесс коррозии. Но наряду с ветром повсеместно действуют и другие мощные агенты физического выветривания. Первый из них связан со свойствами самой породы и проявляется как следствие суточных и сезонных колебаний температуры. Наибольшие амплитуды температур создаются на поверхности породы, с глубиной они уменьшаются: суточные колебания сказываются до глубины нескольких дециметров, а годичные — до 10 и даже 20 м. В местностях с морским климатом суточные и сезонные колебания температур невелики; в местностях, лежащих внутри континентов; вдали от моря они наибольшие и достигают десятков градусов.
Горные породы, как и все тела, при нагревании расширяются, а при охлаждении сжимаются; их теплопроводность невелика, поэтому верхние слои прогреваются, а следовательно, и расширяются сильнее, чем более глубокие; в результате создаются механические напряжения, появляются трещины между поверхностными и более глубокими слоями; скалы начинают «шелушиться». Кроме того, действует и еще один фактор — горные породы состоят из зерен различных минералов (гранит, например, состоит из прочно скрепленных друг с другом кристаллов кварца, полевого шпата, слюды и других минеральных зерен), которые при нагревании расширяются неодинаково (например, коэффициент теплового расширения ортоклаза почти в три раза больше, чем кварца). Кристаллы многих минералов расширяются неодинаково по разным кристаллическим направлениям. Если минеральные зерна с неодинаковыми коэффициентами теплового расширения и сжатия оказываются рядом, это приводит к возникновению напряжения между ними, при частых колебаниях температур приводит к «расшатыванию», нарушению целостности породы и появлению сети тонких трещин. Эти трещинки играют большую роль в дальнейшем разрушении горной породы. Попадающая в них вода оказывает на стенки давление, достаточное для разрушения даже самых твердых пород. Так, согласно данным Ребиндера, при обычной температуре в трещинках толщиной в 1 мк капиллярное давление воды составляет около 1,5 кг/см2; в трещинках с диаметром в 1 мкм — до 1500 кг/см2.
При понижении температуры ниже нуля вода в трещинах замерзает, лед занимает больший объем, чем жидкая влага, он давит на стенки трещин и еще более расширяет их. В трещины проникают корни растений, которые при росте также оказывают давление на стенки.
В жарких пустынных областях действие, аналогичное замерзающей воде, производят соли. Они попадают в трещины горной породы в растворенном виде с проникающей влагой. При нагревании поверхности скал влага испаряется, соли кристаллизуются. При росте кристаллов их объем увеличивается, они оказывают давление на стенки трещин и расширяют последние.
Физическое разрушение пород приводит к образованию обломочной, хрящевато-щебневатой коры выветривания. Полярные пустыни и вершины гор, если они не покрыты снегом и льдом, представляют собой «каменные моря», где вся поверхность покрыта крупными, беспорядочно нагроможденными остроугольными камнями — продуктами разрушения массивных пород.
Ярким примером господства процессов физического выветривания являются выровненные поверхности гольцов на Северном Урале, в горах Таймыра, Средней и Восточной Сибири, где среди каменных россыпей возвышаются лишь отдельные скалы — «свидетели» былого состояния вершинной поверхности. Другой пример господства физического выветривания — «каменные моря» — скопления крупных обломков скал, щебня и гравия, в которых «тонут» горные сооружения в жарких пустынях мира.
Физическое разрушение пород и минералов замедляется по мере уменьшения размеров образующихся частиц и практически останавливается по достижении ими состояния крупной пыли — частиц, диаметр которых лежит в пределах 0,05—0,01 мм. Еще более дисперсного состояния выветривающиеся минералы достигают в результате химического и биохимического выветривания.
Химическое и биохимическое выветривание минералов. Одновременно с физическим разрушением горных пород начинается и их химическое изменение. Атмосферная вода, насыщенная кислородом, соприкасаясь с породой, производит гидратацию, окисление и растворение ряда минералов.
Попадающая вместе с водой на поверхность породы и в ее трещины разнообразная микрофлора (синезеленые и диатомовые водоросли, грибы, бактерии), а также поселяющаяся на поверхности породы литофильная растительность (лишайники, мхи) также весьма активно участвуют в химическом изменении минералов.
В процессе жизнедеятельности организмы выделяют углекислый газ СО2 В больших количествах СО2 образуется и при разложении органических остатков. Поэтому вода, циркулирующая в мельчайших трещинах породы, всегда насыщена углекислотой. При растворении СО2 в воде образуется Н2СО3, которая при диссоциации дает ионы Н+ и НСО3-. Увеличение концентрации ионов водорода в воде за счет растворения С02 сильно повышает растворяющее и разлагающее действие на минералы.
Живые организмы выделяют различные органические соединения, способствующие разложению минералов: лишайники — особые органические кислоты; силикатные бактерии — разъедающую минералы слизь; диатомовые водоросли — слизь, разлагающую даже такой устойчивый минерал, как каолин. Наконец, при разложении органических остатков образуются специфические органические кислоты, близкие к кислотам, характерным для органического вещества почв, которые также участвуют в биохимическом выветривании.
Таким образом, агентами химического выветривания минералов являются: вода, кислород, углекислота и различные органические соединения преимущественно кислотного типа.
При воздействии воды, кислорода, углекислоты и органических кислот в поверхностных горизонтах литосферы и в почвах идут реакции растворения, окисления, гидратации и гидролиза минералов. Одновременно происходит синтез вторичных минералов. Некоторые из них, как, например, многие глинистые минералы, диаметр частиц которых <0,001 мм, устойчивы и сохраняются в выветривающейся толще пород; другие, как, например, простые соли (хлориды, сульфаты, карбонаты), малоустойчивы, растворяются и выносятся с грунтовыми и поверхностными водами.
Растворение. Все минералы, и первичные и вторичные, подвержены в той или иной мере процессам растворения, что проявляется в химическом составе природных вод. Наибольшей растворимостью обладают хлориды, сульфаты и карбонаты щелочных металлов, менее растворимы карбонаты кальция и магния. Их растворение и выщелачивание из толщ карбонатных, гипсоносных и засоленных пород приводит к формированию карста — солевого, гипсового и карбонатного. Растворение и выщелачивание солей из почв сопровождается образованием особого просадочного микрорельефа.
Значительно меньшей растворимостью обладают фосфаты кальция и кремнезем, освобождающийся при выветривании первичных минералов или осадочных кремнистых пород. Первичные алюмосиликаты и кварц в чистой дистиллированной воде малорастворимы. Однако в природных водах, насыщенных углекислотой или содержащих органическое вещество, или имеющих высокую щелочность, растворение усиливается, но здесь этот процесс идет параллельно с разложением минералов.
Гидратация. Процесс гидратации заключается в присоединении молекул воды к безводным минералам, что приводит к трансформации их кристаллической решетки и образованию новых минералов. Так, присоединение молекул воды к безводному минералу гематиту дает серию минералов-гидроксидов различной степени гидратиро- ванности:
Fe2О3 + Н2О -> FeO(OH)+ Н2О -> FeO(OH), + иН2О -> Fe(OH), • nН2О
гематит гетит гадрогетит лимонит
Окисление химических элементов с переменной зарядностью идет в присутствии кислорода и воды. Оно касается прежде всего такого распространенного элемента, как железо. В первичных силикатах и алюмосиликатах присутствует преимущественно двухзарядное железо. Если при дроблении минералов, содержащих двухзарядное железо, отдельные ионы его оказываются на поверхности, начинаются процессы окисления и гидратации. На поверхности обломков пород и минеральных зерен появляются охристые, оранжевые пятна и пленки гидроксидов железа Fe2О3 • nН2О. Они особенно обильны при большом содержании в породах темноцветных минералов: оливина, пироксенов и биотита. В случае наличия в породах минералов двухзарядного марганца при его окислении и гидратации образуются гидроксиды трех- и четырехзарядного марганца — манганит МпО(ОН), пиролюзит МпO2 и др. Гидроксиды марганца выделяются в форме черных, сажистых скоплений, иссиня-черных пленок на поверхности пород и минеральных зерен.
Окисление двухзарядных железа и серы сульфидов (пирита, марказита и др.) сопровождается образованием наряду с сульфатами и гидроксидами железа свободной серной кислоты:
2FeS2+7O2+2H2O = 2FeSO4 +2H2SO4
2FeSO4+0+5H2P = 2Fe(OH)3+2H2SO4
Образующаяся серная кислота активно разрушает минералы; водород вытесняет основания из кристаллических решеток, в результате образуются сульфаты кальция CaSO4, магния MgSO4, натрия Na2SO4 и калия K2SO4. Наиболее легкорастворимые из них в условиях свободного дренажа выщелачиваются; менее растворимые, как, например, гипс CaSO4- • 2Н2O,в определенных условиях могут накапливаться; происходит загипсование выветривающейся породы.
Гидролиз. Постоянно присутствующая в большинстве природных вод растворенная углекислота, а также продуцируемые организмами органические кислоты являются источниками водородного иона Н+ (протона) — активного реагента, способного вытеснять основания из кристаллических решеток минералов (Са2+, Mg2+, Na+, К+). Процесс замещения оснований на водородный ион в кристаллической решетке силикатов и алюмосиликатов и их гидратации называется гидролизом. С процессами гидролиза и вторичного синтеза минералов из продуктов распада связано образование обширной группы глинистых минералов, диаметр кристаллов которых измеряется микронами и долями микронов. Высокая степень дисперсности обусловливает появление у глинистых минералов свойств коллоидов: они имеют на поверхности заряд, преимущественно отрицательный, обладают сорбционными свойствами по отношению к катионам, могут переходить, подобно коллоидам, в состояние золя и коагулировать; некоторые из них при увлажнении сильно набухают как истинные коллоиды. Все они принадлежат к группе слоистых силикатов (двух-, трех- и четырехслойных) с варьирующим отношением SiО2/Al2О3 от 2 до 5; все глинистые минералы в той или иной степени гидратированы.
В двухслойных глинистых минералах элементарный слой кристаллической решетки состоит из одного тетраэдрического кремне- кислородного слоя и одного октаэдрического алюмогидроксильного (рис. 6.3, а). Молекулярное отношение SiО2/Al2О3 = 2.
В трехслойных глинистых минералах на один октаэдрический алюмогидроксильный слой приходится два тетраэдрических крем- некислородных (рис. 6.3, б, в). Между трехслойными пакетами располагаются ионы калия, кальция, магния и гидроксония. Молекулярные отношения SiО2/Al2О3 варьируют от 3 до 4, так как в части тетраэдров кремний может быть замещен алюминием.
К двухслойным глинистым минералам относятся каолинит, гал- луазит, дикит и накрит. В кристаллической решетке этих минералов почти все основания замещены водородом. Наиболее распространенные среди них — каолинит и галлуазит — образуются при условии быстрого удаления оснований, вытесняемых из кристаллических решеток первичных минералов (см. рис. 6.3, а).
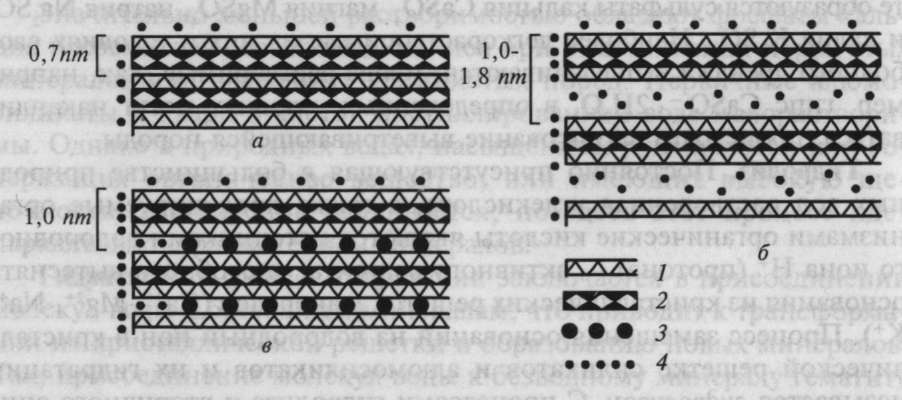
Рис. 6.3. Строение глинистых минералов и обменные катионы. Минералы:
а — каолинит (двухслойный); б — монтмориллонит (трехслойный с расширяющейся решеткой); в — иллит (трехслойный со стабильной решеткой); 1 — кремнекислородные тетраэдры; 2 — алюмогидроксильные октаэдры; 3 — необменные катионы; 4 — обменные катионы.
В гидротермических условиях поверхности земли это достаточно устойчивые минералы. Они накапливаются наряду с гидрокси- дами алюминия и железа в качестве остаточных продуктов в древних корах выветривания и сформированных на этих корах почвах.
Трехслойные глинистые минералы представлены группой монтмориллонита, включающей монтмориллонит, нонтронит и бейделит (см. рис. 6.3, б). Эти минералы образуются в нейтральной или щелочной среде, где присутствуют кальций и магний. Монтмориллонит часто образуется при выветривании основных пород, богатых щелочноземельными основаниями. Кристаллическая решетка монтмориллонита при увлажнении способна расширяться, вода проникает в межплоскостные промежутки и минерал сильно разбухает, что облегчает проникновение различных оснований в межслоевое пространство, увеличивая сорбционную способность этой группы минералов. В кислой среде монтмориллонит неустойчив.
К группе трехслойных глинистых минералов, но со стабильной решеткой относятся иллит и гидрослюды (рис. 6.3, в). Иллит — калийная гидрослюда — образуется на первых стадиях выветривания полевых шпатов. Внешне это проявляется в образовании на поверхности минеральных зерен и по трещинам спайности мелких слюдоподобных светлых чешуек.
При длительном течении процесса выветривания происходит полное метосоматическое (без изменения первоначальной формы минералов) замещение гидрослюдами зерен первичных полевых шпатов. Дальнейший гидролиз гидрослюд и полное замещение калия водородным ионом преобразует иллит в каолинит или галлуазит.
При выветривании слюд и хлорита образующиеся на первых стадиях выветривания гидромусковит, гидробиотит, гидрохлорит при дальнейшем выветривании переходят в вермикулит, железисто-магнезиальный алюмосиликат, подобно монтмориллониту имеющий подвижную кристаллическую решетку.
В процессе преобразования первичных и синтеза вторичных алюмосиликатов образуется большая группа промежуточных смешан- нослойных минералов — смектитов. Это трех- и четырехслойные глинистые минералы, в кристаллической решетке которых в качестве элементарных структурных элементов выступают кристаллические решетки различных глинистых минералов, например, монт- мориллонит-иллита, монтмориллонита-вермикулита-хлорита и др.
Наряду с глинистыми алюмосиликатами при выветривании и разрушении кристаллических решеток как первичных, так и вторичных минералов освобождаются оксиды кремния (кремнезем SiО2) и алюминия (глинозем А12О3). Гидроксиды кремнезема частично растворяются и выносятся с подземными и поверхностными водами в речной сток, а частично осаждаются в виде аморфных сильно гидратированных осадков SiО2 • nН2О, которые при высыхании и некоторой потере воды превращаются в опал, а по мере частичной кристаллизации переходят в халцедон.
Белые порошковидные новообразования аморфного кремнезема на поверхности минералов и структурных отдельностей в вывет- релых породах и почвах получили название «кремнеземистой присыпки».
Гидроксиды алюминия менее растворимы, чем гидроксид кремнезема. В нейтральной и слабокислой среде они накапливаются как остаточные продукты выветривания. При кристаллизации гидрокси- дов алюминия образуются минералы: боксит А12О3 • nН2О, гидраргил- лит, или гиббсит А1(ОН)3, бёмит АlO(ОН). Это типичные минералы коры выветривания и почв влажных субтропиков и тропиков.
При выветривании железосодержащих силикатов — авгитов, роговых обманок, оливина — освобождаются гидроксиды железа. По мере кристаллизации и потери воды они превращаются в лимонит, гидрогетит, гетит и вторичный гематит. Все эти минералы ярко окрашены, они имеют охристый, оранжевый или кирпично- красный цвет и присутствие их хорошо заметно.
Первичные минералы, содержащие марганец, при выветривании являются источником в коре выветривания и почвах оксидов марганца — пиролюзита Мп02 и псиломелана mМпО • МпO2 •nН2O.
При быстром течении процессов выветривания и полном разложении алюмосиликатов на составляющие оксиды кремния и алюминия происходит их совместное осаждение в виде аморфных гидратированных осадков — аллофанов с варьирующим отношением SiO2/Al2O3.
По мере старения и кристаллизации они переходят в глинистые слоистые алюмосиликаты: каолинит, а в присутствии Са и Mg — в
монтмориллон ит.
Освобождающиеся при выветривании первичных минералов кальций, магний, калий, натрий соединяются с анионом угольной кислоты и образуют углекислые соли — карбонаты. Например:
CaAl2Si2O8+ Н2СO3 + Н2O -> H,Al2Si2O8- 2Н2O + CaCO3
анортит каолинит кальцит
При выветривании калиевых полевых шпатов и кислых плагиоклазов образуется много соды Na2CO3 • 10Н2O, выделяется поташ К,СО Н2O, при выветривании кальций- и магнийсодержащих минералов - доломит (Са, Mg)CO3.
