
- •1. Основные положения мкт. Идеальный газ.
- •Основные определения (давление, плотность количество вещества, константы и размерность)
- •2) Число молекул в вещества;
- •3) Число молекул в вещества;
- •Количество вещества можно найти по формуле
- •2. Основное уравнение мкт, температура, среднеквадратичная скорость
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Температура снизилась с до . Как изменилась при этом среднеквадратичная скорость молекул?
- •1) Уменьшилась в 2 раза;
- •3. Уравнение Менделеева-Клапейрона, газовые законы
- •Уравнение Менделеева–Клапейрона имеет вид
- •Уравнение Менделеева–Клапейрона имеет вид
- •Уравнение изобары имеет вид
- •4. Сложные задачи на газовые законы
- •5.Основные определения статистики Максвелла
- •6. Знание формул для статистики Максвелла, среднеквадратичная скорость
- •7.Распределение Больцмана (не везде знание формулы)
- •1) ; 2) ; 3)Обе формулы верны.
- •8. Длина свободного пробега
- •9. Термодинамика. Определения. 1-е начало. Простые вопросы.
- •10.Первое начало термодинамики для изопроцессов. Сложные формулы. Задачи.
- •11.Теплоёмкость, адиабатный процесс
- •12. Тепловые машины
- •13. Второе начало термодинамики. Энтропия
- •3. Обе формулы верны.
- •3. Обе формулы верны.
6. Знание формул для статистики Максвелла, среднеквадратичная скорость
Распределение Максвелла имеет вид
1)
![]() ;
;
2)
![]() ;
;
3)
![]() .
.
Распределение Максвелла имеет вид
1)
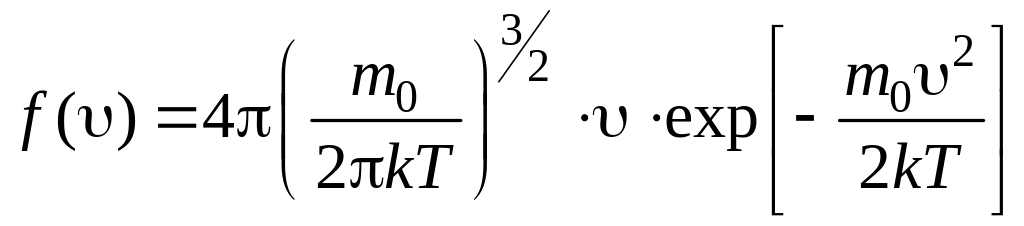 ;
;
2)
![]() ;
;
3) .
Распределение Максвелла имеет вид
1)
![]() ;
;
2) ;
3) .
Средняя скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Наиболее вероятная скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Среднеквадратичная скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Средняя скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Наиболее вероятная скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Среднеквадратичная скорость молекул определяется формулой
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Среднеквадратичная скорость молекул зависит от температуры как
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Среднеквадратичная скорость молекул некоторого газа при температуре 500 К была 500 м/с. Чему стала равна среднеквадратичная скорость молекул этого газа при температуре 900 К?
1) 670 м/с 2) 740 м/с; 3) 800 м/с.
Средняя скорость молекул некоторого газа при температуре 300 К была 1000 м/с. Чему стала равна средняя скорость молекул этого газа при температуре 800 К?
1) 1,6 км/с 2) 2 км/с; 3) 2,4 км/с.
Наиболее вероятная скорость молекул некоторого газа при температуре 400 К была 400 м/с. Чему стала равна наиболее вероятная скорость молекул этого газа при температуре 1200 К?
1) 571 м/с 2) 692 м/с; 3) 813 м/с.
Среднеквадратичная скорость молекул кислорода (молярная масса ) при температуре 23 0С равна
1) 267 м/с 2) 320 м/с; 3) 483 м/с.
Среднеквадратичная скорость молекул кислорода (молярная масса ) при температуре 500 0С равна
1) 644 м/с 2) 776 м/с; 3) 915 м/с.
Средняя скорость молекул водорода при температуре 23 0С равна
1) 1,21 км/с 2) 1,782 км/с; 3) 2,156 км/с.
Средняя скорость молекул водорода при температуре 500 0С равна
1) 2,86 км/с 2) 3,07 км/с; 3) 5,72 км/с.
При какой температуре среднеквадратичная скорость молекул водорода равна 500 м/с
1) 80 К 2) 140 К 3) 210 К.
Чему равна среднеквадратичная скорость молекул водорода при температуре 100 К?
1) 513 м/с 2) 883 м/с; 3) 1116 м/с.
Между величинами средней скорости
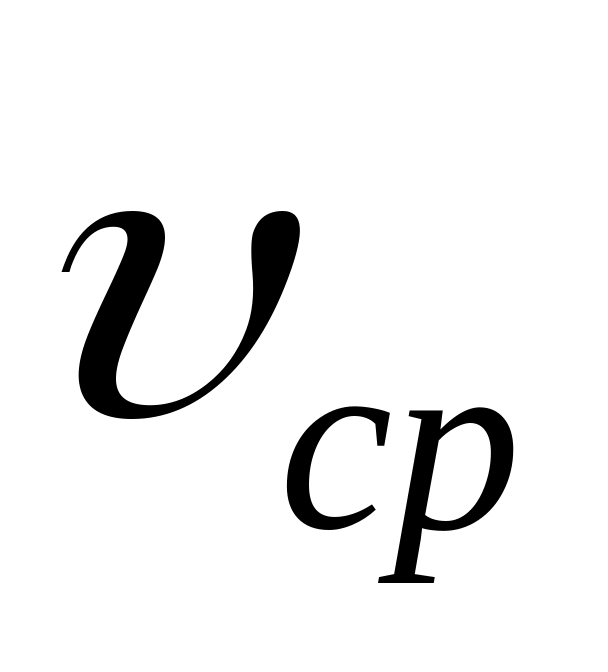 ,
среднеквадратичной скорости
,
среднеквадратичной скорости
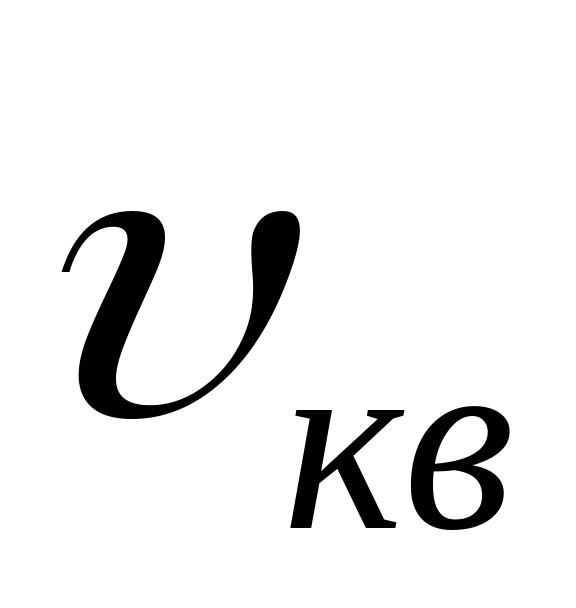 и наиболее вероятной скорости
и наиболее вероятной скорости
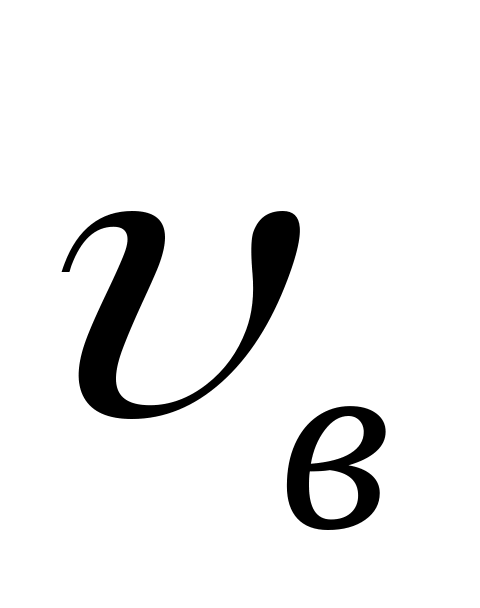 справедливо соотношение
справедливо соотношение
1);![]() 2);
2);
![]() 3)
3)
![]() .
.
7.Распределение Больцмана (не везде знание формулы)
Распределение Больцмана – это распределение частиц по
1) потенциальной энергии;
2) высоте;
3) оба утверждения верны.
Распределение Больцмана справедливо
1) для молекул идеального газа;
2) для микроскопических частиц в поле тяжести;
3) оба утверждения верны.
Распределение Больцмана – это распределение частиц по
1) потенциальной энергии;
2) кинетической энергии;
3) энергии хаотического движения.
Распределение Больцмана имеет вид
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Распределение Больцмана имеет вид
1)
; 2)
![]() ; 3)
; 3)
![]() .
.
Барометрическая формула имеет вид
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Барометрическая формула имеет вид
