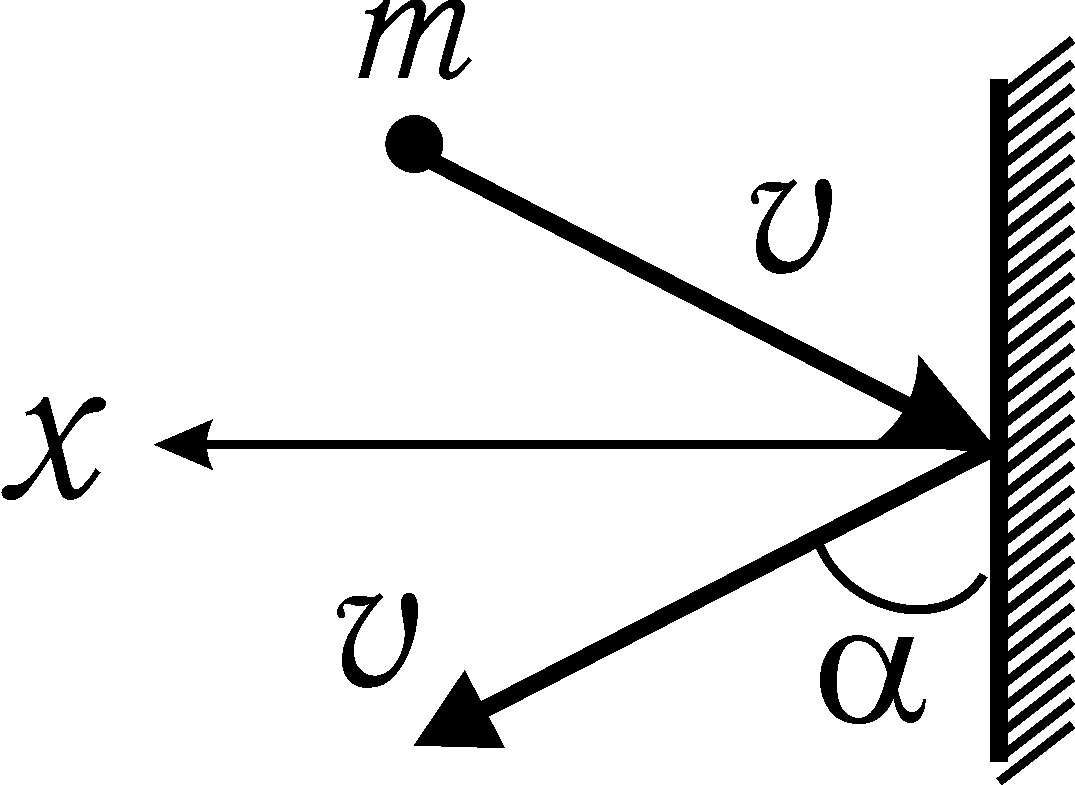- •1. Основные положения мкт. Идеальный газ.
- •Основные определения (давление, плотность количество вещества, константы и размерность)
- •2) Число молекул в вещества;
- •3) Число молекул в вещества;
- •Количество вещества можно найти по формуле
- •2. Основное уравнение мкт, температура, среднеквадратичная скорость
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Основное уравнение молекулярно–кинетической теории записывается так:
- •Температура снизилась с до . Как изменилась при этом среднеквадратичная скорость молекул?
- •1) Уменьшилась в 2 раза;
- •3. Уравнение Менделеева-Клапейрона, газовые законы
- •Уравнение Менделеева–Клапейрона имеет вид
- •Уравнение Менделеева–Клапейрона имеет вид
- •Уравнение изобары имеет вид
- •4. Сложные задачи на газовые законы
- •5.Основные определения статистики Максвелла
- •6. Знание формул для статистики Максвелла, среднеквадратичная скорость
- •7.Распределение Больцмана (не везде знание формулы)
- •1) ; 2) ; 3)Обе формулы верны.
- •8. Длина свободного пробега
- •9. Термодинамика. Определения. 1-е начало. Простые вопросы.
- •10.Первое начало термодинамики для изопроцессов. Сложные формулы. Задачи.
- •11.Теплоёмкость, адиабатный процесс
- •12. Тепловые машины
- •13. Второе начало термодинамики. Энтропия
- •3. Обе формулы верны.
- •3. Обе формулы верны.
1. Основные положения мкт. Идеальный газ.
К одному из основных положений молекулярно–кинетической теории следует отнести следующее высказывание:
1) молекулы вещества могут находиться только в поступательном и вращательном движениях;
2) молекулы вещества взаимодействуют между собой;
3) размерами молекул можно пренебречь.
Между молекулами действуют
1) силы притяжения;
2) силы отталкивания;
3) силы притяжения и отталкивания
Идеальным называется газ, для которого можно пренебречь
1) размерами молекул;
2) взаимодействием молекул;
3) и размерами и взаимодействием.
Какой газ ближе к идеальному?
1) с большим давлением и малой температурой;
2) с малым давлением и малой температурой;
3) с малым давлением и большой температурой.
Молекулы газов участвуют
1) только в поступательном движении;
2) в поступательном и вращательном движении;
3) в поступательном, вращательном и колебательном движении.
Молекулы газов при столкновениях
1) обмениваются энергией между собой;
2) обмениваются ускорениями движений;
3) подчиняются закону абсолютно неупругого удара.
При столкновении со стенкой сосуда, молекула передаёт стенке импульс, равный ( в проекции на ось х)
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
При ударе о стенку сосуда молекула изменяет свой импульс на величину
 ,
равную
,
равную
|
1)
2)
3) 0. |
Основные определения (давление, плотность количество вещества, константы и размерность)
1 моль вещества имеет столько же молекул, сколько их в
1) 1 г водорода; 2) 1 г углерода; 3) 12 г углерода.
Давление газа это
1) сила тяжести молекул, действующая на единицу площади поверхности сосуда;
2) сила давления молекул, действующая на единицу площади поверхности сосуда;
3) оба варианта верны.
Один паскаль – это давление, которое
1) создаётся силою в 1 ньютон, которая действует нормально на площадку площадью в 1 см2;
2) создаётся силою в 1 ньютон, которая действует нормально на площадку площадью в 1 м2;
3) создаётся силою в 1 Кг, которая действует нормально на площадку площадью в 1 см2.
Концентрация молекул это
1) число молекул в
![]() вещества;
вещества;
2) Число молекул в вещества;
3) Число молекул в вещества;
Число Авогадро определяет
1) число молекул в вещества;
2) число молекул в вещества;
3) число молекул в
![]() вещества;
вещества;
Число Авогадро равно
1)
![]() ; 2)
; 2)
![]() ; 3).
; 3).
![]()
Масса одной молекулы кислорода равна (относительная атомная масса кислорода равна 16)
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Универсальная газовая постоянная равна
1)
![]() 2)
2)
![]() 3)
3)
![]()
Количество вещества можно найти по формуле
1)
 2)
2)
![]() ; 3)
обе формулы верны.
; 3)
обе формулы верны.
Количество вещества можно найти по формуле
1)
2)
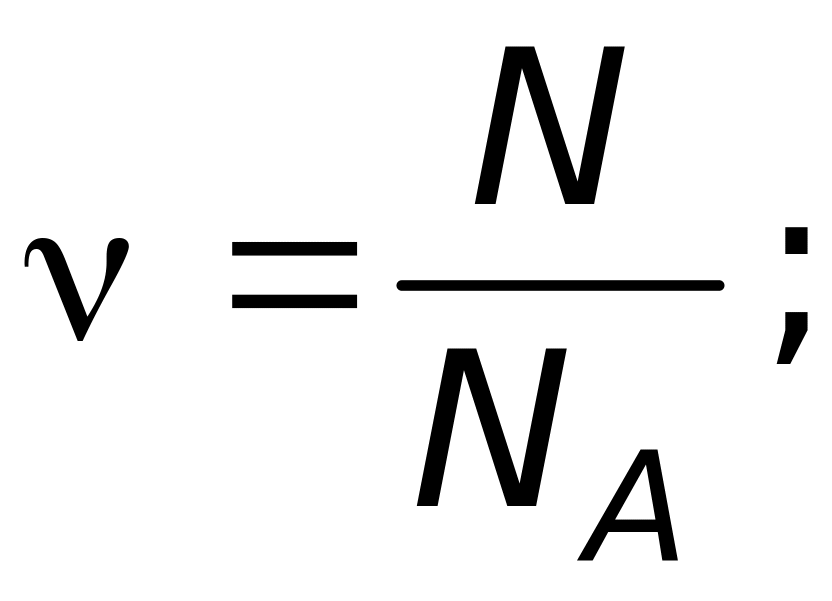 3)
обе формулы верны.
3)
обе формулы верны.
Сколько моль содержится в 5 граммах кислорода? (Относительная атомная масса кислорода 16).
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Сколько моль содержится в 96 граммах кислорода? (Относительная атомная масса кислорода 16).
1)
![]() ; 2)
; 2)
![]() ; 3)
.
; 3)
.
Молярная масса смеси газов находится по формуле
1)
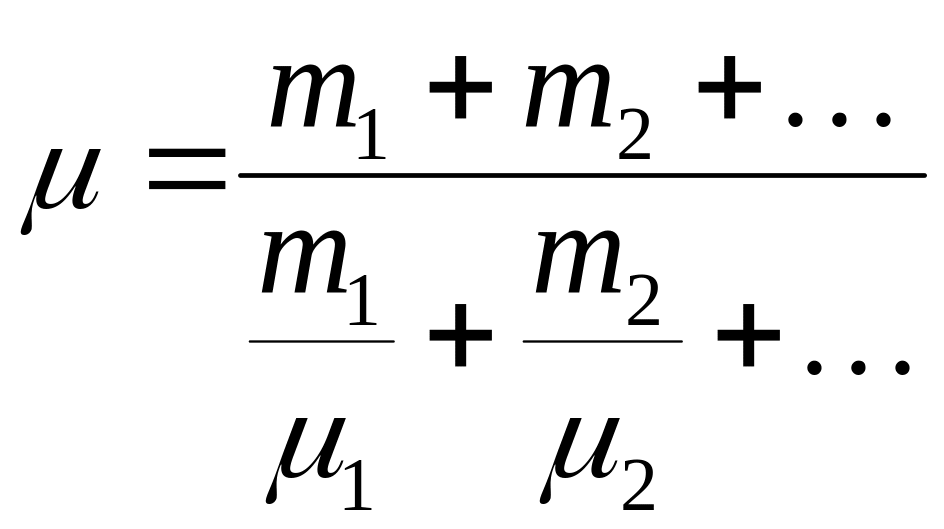 ; 2)
; 2)
 ; 3)
; 3)
![]() .
.
Какова молярная масса смеси, состоящей из 5 молей гелия и 2 молей водорода? (Молярная масса гелия
 ,
а водорода
,
а водорода
 )
)
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.
Найти молярную массу смеси, состоящей из 9 г водяных паров и 11 г углекислого газа? (Молярная масса воды
 ,
а углекислого газа
,
а углекислого газа
 )
)
1)
![]() ; 2)
; 2)
![]() ; 3)
; 3)
![]() .
.