
- •В.П. Дмитриков, о.Г. Близнюченко, с.М. Кривонос конспект лекцій
- •Перелік скорочень
- •Лекція 1
- •1.1. Корисні і токсичні речовини в продукції апк
- •1.2. Визначення якості продукції
- •1.3. Завдання моніторингу якості сільгосппродукції
- •1.4. Мета і задача дисципліни
- •Контрольні питання
- •Лекція 2
- •2.1. Головні забруднення і забруднювачі
- •2.2. Азотовмісні сполуки
- •2.3. Пестициди і антибактеріальні речовини
- •2.4. Важкі метали і радіаційне забруднення
- •Контрольні питання
- •Лекція 3
- •3.1. Класифікація токсикантів
- •3.2. Ендогенні та екзогенні забруднення
- •3.3. Токсикологічні забруднення продуктів
- •Контрольні питання
- •Лекція 4
- •4.1. Фактори ризику від генетично модифікованої продукції
- •4.2. Проведення досліджень гмп на якість та біобезпечність
- •4.3. Методи виявлення генетично модифікованої продукції
- •Контрольні питання
- •Лекція 5
- •5.1. Фактори, що впливають на якість та зберігання продукції
- •5.2. Контроль якості плодів і овочів під час зберігання
- •5.3. Нормування якості продукції. Завдання нормування
- •5.4. Основні кондиції сільгосппродукції
- •Контрольні питання
- •Лекція 6
- •6.1. Основні положення стандартизації
- •6.2. Розробка і типи стандартів
- •6.3. Класифікація і структура державних стандартів
- •Контрольні питання
- •Лекція 7
- •7.1. Види контролю якості
- •7.2. Традиційні методи контролю якості
- •7.3. Забезпечення якості результатів аналізу
- •Кожну контрольну пробу аналізують кілька разів.
- •Контрольні питання
- •Лекція 8
- •8.1. Типи моніторингового контролю
- •8.2. Предмети й об'єкти моніторингу
- •8.3. Головні методи моніторингу
- •8.4. Контактні і неконтактні методи виміру
- •Контрольні питання
- •Лекція 9
- •9.1. Системи автоматичного контролю параметрів
- •9.2. Основні і допоміжні функції сак
- •9.3. Структурна схема сак
- •Контрольні питання
- •Лекція 10
- •10.1. Загальні відомості про датчики
- •10.2. Класифікація датчиків
- •10.3. Характеристики датчиків
- •Контрольні питання
- •Лекція 11
- •11.1. Фізичні методи
- •11.2. Електрохімічні методи. Потенціометрія
- •11.3. Іонселективні електроди в потенціометрії
- •Контрольні питання
- •Лекція 12
- •12.1. Види випромінювання, радіонукліди
- •12.2. Взаємодія ядерного випромінювання з речовиною
- •12.3. Принцип дії іонізаційного детектора
- •Контрольні питання
- •Лекція 13
- •13.1. Загальні принципи спектроскопії
- •13.2. Основний закон поглинання
- •13.3. Спектроскопія видимої й ультрафіолетової області
- •13.4. Загальна схема оптичних спектрофотометрів
- •13.5. Спектроскопія інфрачервоної області
- •Контрольні питання
- •Лекція 14
- •14.1. Хроматографія і сорбційні процеси
- •14.2. Параметри хроматограми
- •14.3. Ефективність хроматографічного розподілу
- •Контрольні питання
- •Лекція 15
- •15.1. Принципи управління якістю
- •15.2. Ефективність системи управління якістю продукції
- •15.3. Діагноз, прогноз і управління в моніторингу якості
- •15.4. Особливості локального і регіонального агроекологічного моніторингу
- •Контрольні питання
- •Лекція 16
- •16.1. Державне регулювання продовольчої безпеки
- •16.2. Міжнародне регулювання безпеки харчових продуктів
- •16.2.1. Стандарт іфс
- •16.2.2. Система хассп
- •Склад й послідовність дій для впровадження вимог iso 22000 (хассп):
- •Контрольні питання
- •Додатки
- •Література
14.2. Параметри хроматограми
Якщо на виході із шару сорбенту реєструвати зміну в часі (або об’ємі рухомої фази) якої-небудь властивості потоку рухомої фази, то на стрічці реєстратора запишеться вихідна хроматографічна крива– хроматограма (рис. 11). Параметри вихідної кривої – параметри утримання – можуть служити засобом вираження результатів хроматографічного розподілу суміші речовин.
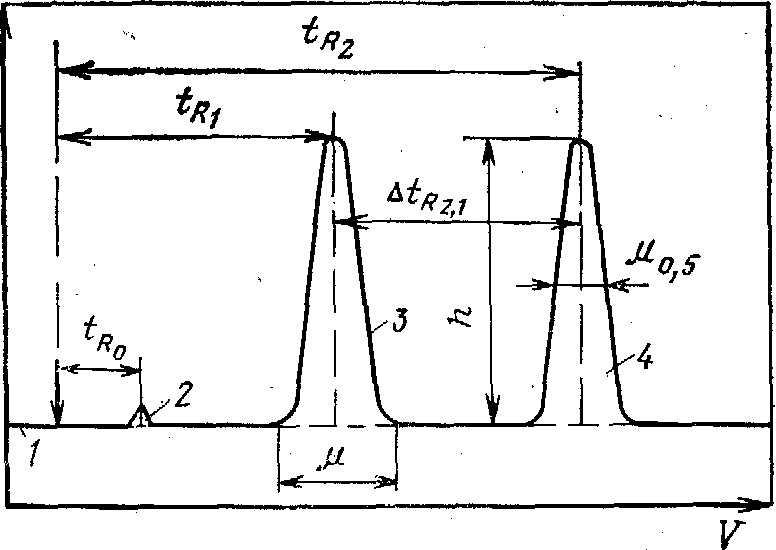
Рис. 11. Диференціальна хроматограма двох компонентів:
1 – нульова лінія; 2 – пік не сорбуємого компонента; 3 і 4 – піки цільових компонентів
Сорбційна здатність нерухомої фази стосовно поділюваних речовин характеризується часом утримання t. Це – відстань на хроматограмі від моменту введення речовини в шар сорбенту до моменту появи речовини в максимальній концентрації в потоці рухомої фази на вході із шару сорбенту .
Об’єм рухомої фази, що пройшов через шар сорбенту, називають об’ємом утримання VR:
VR = t∙ v,
де v – об'ємна швидкість рухомої фази,
VR,t – обсяг (час) утримання компоненту.
Висота вихідної кривої (піка) h – це перпендикуляр, опущений з максимуму піка на нульову лінію. Нульова лінія – частина хроматограми, отримана при реєстрації сигналу детектора під час виходу зі стовпчика чистої рухомої фази. Ширина піка μ – відрізок, що відтинається на нульовій лінії дотичними до кривої в крапках перегину, його половина – відстань між точками контуру піка на середині висоти μ0,5.
14.3. Ефективність хроматографічного розподілу
В хроматографічному процесі речовина, що переміщається уздовж шару сорбенту, розподіляється між рухомою і нерухомою фазами і зона речовини розмивається. Чим більше розмивання зон двох сусідніх компонентів, тим складніше їх розділити. Мірою розмивання хроматографічної зони є висота, еквівалентна теоретичній тарілці (ВЕТТ або Н).
Для колоночної хроматографії кількість теоретичних тарілок N розраховують за формулою:
N = 5,54 (t / μ0,5 )2
ВЕТТ розраховують за формулою ВЕTT = L / N, де L – довжина колонки, мм.
Чим менше ВЕТТ, тим ефективніше працює колонка, тим більш вузькими стають піки на хроматограмі.
Для кількісної оцінки хроматографічного розподілу використовують критерії, що характеризують якість розподілу в залежності від параметрів і умов виміру – природи сорбенту, температури, особливостей фаз тощо. До них відносять ступінь розподілу α, критерій селективності КC, критерій розподілу R.
Ступінь розподілу α змінюється від 1 до ∞ і характеризує відносне утримання компонентів суміші і селективність нерухомої фази. Величину α розраховують за формулою через VR або t
α = ( tR2 – tR0) / ( tR1 – tR0) = K2 / K1
Критерій селективності Кс змінюється від 0 до 1 і характеризує вибірковість сорбенту. Його розраховують через VR або t за формулою:
КС = ( tR2 – tR1) / ( tR1 + tR2)
При Кс = 0,4 компоненти розділяються цілком.
Критерій розподілу R враховує дію на повноту поділу ефективності колонки і селективності сорбенту. Його розраховують за формулою
R = 2ΔtR2,1 / (μ1 + μ2)
Критерій розподілу R має значення від 0 до ∞, однак уже з наближенням R до 1 компоненти суміші розділяються цілком.
Схема газового хроматографа містить чимало елементів, але головними є хроматографічна колонка та детектор (рис. 12).
 2 3 4
5 9 6 7 10 11 15 16
2 3 4
5 9 6 7 10 11 15 16
1 8 12 скидання 13 14
8 12 скидання 13 14
Рис. 12. Схема газового хроматографа:
1 – балон зі стиснутим газом; 2,4 – регулятори витрати газу; 3 – вимірник витрати газу; 5 – фільтр; 6 – дозатор-випарник; 7 – хроматографічна колонка; 8 – термостат; 9 – мікрошприц; 10 – терморегулятор; 11 – пристрій для програмування температури; 12 – детектор; 13 – блок живлення детектора; 14 – підсилювач; 15 – дисплей; 16 – комп'ютер
У практиці газової хроматографії широко застосовують детектор, заснований на вимірі теплопровідності газу (ДТП) і полум'яно-іонізаційний детектор (ПІД). Принцип роботи детектора по теплопровідності заснований на зміні електричного опору провідника в залежності від теплопровідності НС.
Газова хроматографія на капілярних колонках (довжина 20–50 м) характеризується високою розподільною здатністю (рис. 13).
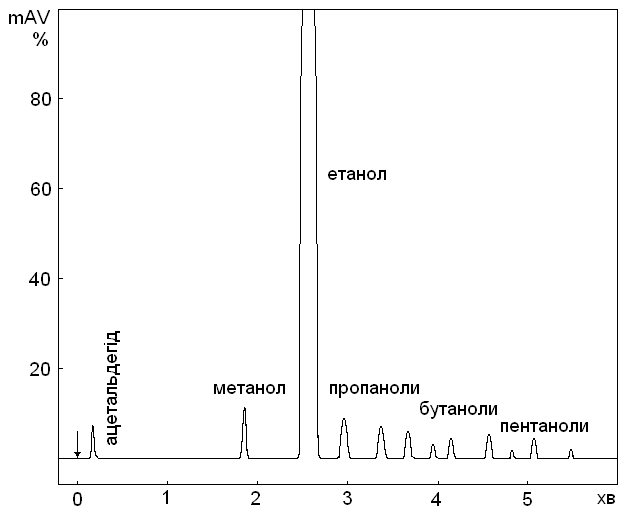
Рис. 13. Газохроматографічний аналіз спирту-сирцю на капілярній колонці
Найбільш поширений з детекторів полуменево-іонізаційний, оскільки він
є універсальним. Для визначення галогеновуглеводнів застосовують детектор електронного захоплення, а склад фосфор- і азотовмісних агрохімічних препаратів визначають за допомогою N/Р -детектора.
