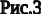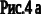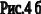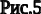Материальные балансы в этом случае будут
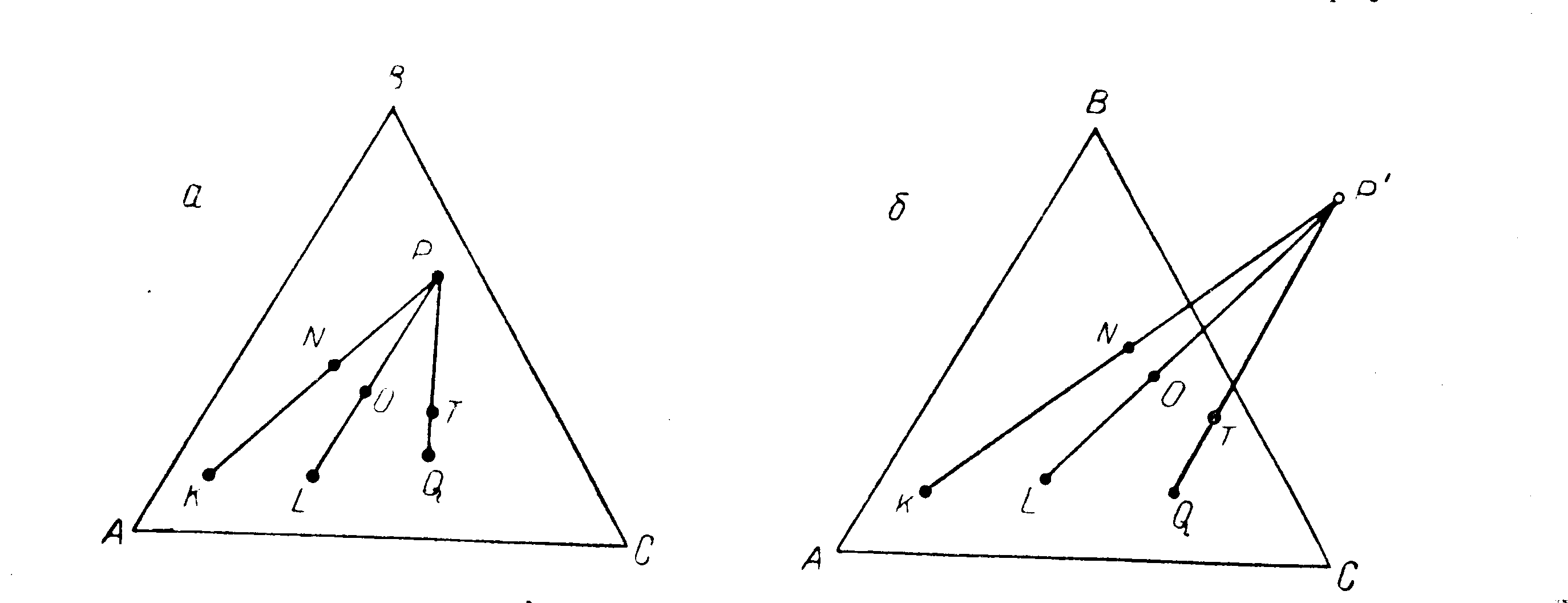
N = K +P; О = L + Р; T = Q + P откуда N - K = O – L = T – Q = P
Отсюда выводится имеющее большое применение свойство треугольной диаграммы: если разность количеств любых двух смесей компонентов А, В и С есть величина постоянная, то на треугольной диаграмме прямые, соединяющие точки, выражающие составы этих смесей (на рис. 4, а точки К и N, L и О, Q и Т), пересекутся в одной точке (Р), называемой полюсом экстрагирования.
Полюс экстрагирования может оказаться вне диаграммы (например, точка Р' на рис. 4, б). В этом случае состав, выражаемый этой точкой, является гипотетическим, так как лежит вне реальных пределов.
Кривые равновесия фаз в треугольных диаграммах
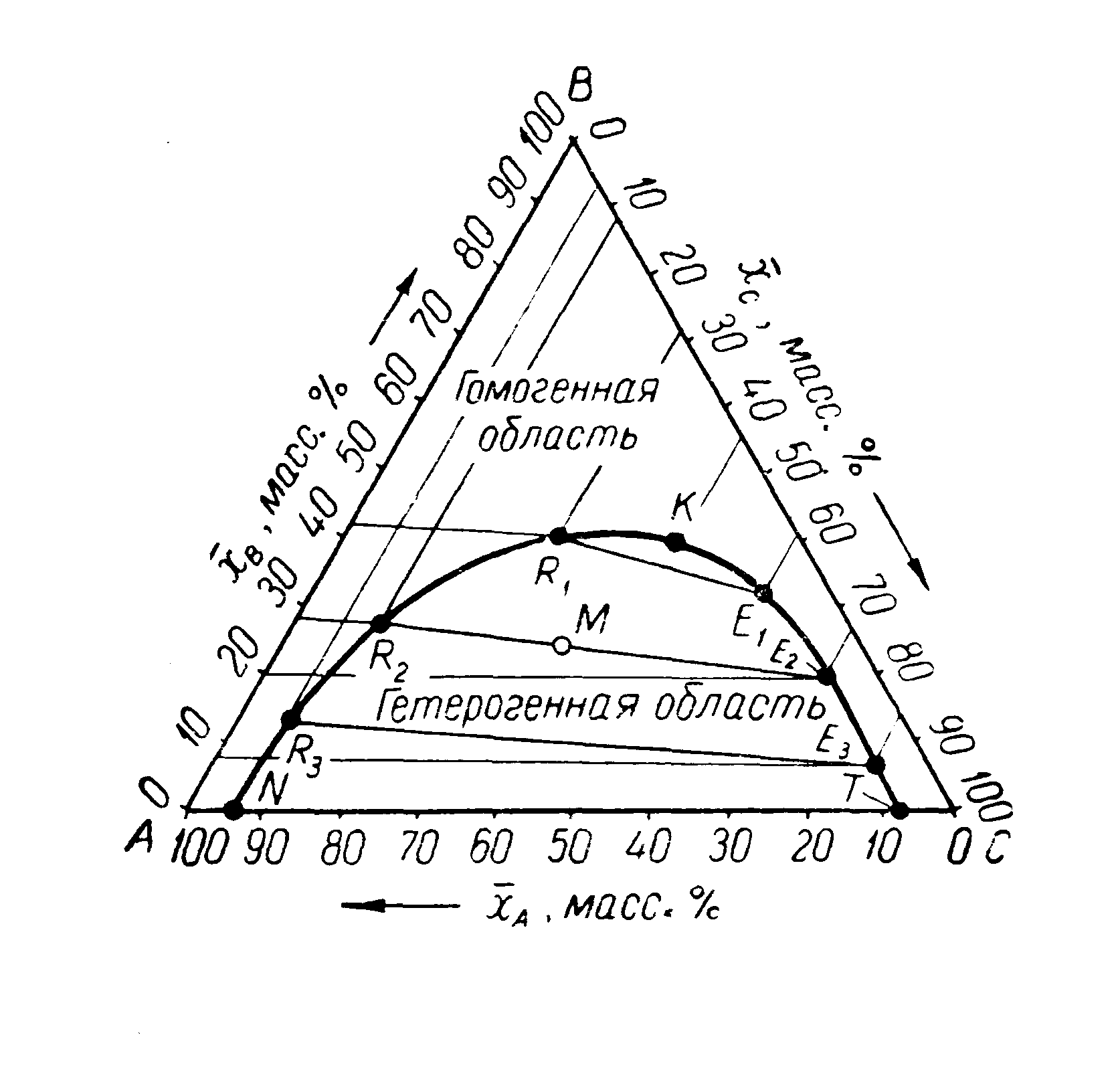
На рис. 5 представлена типовая тройная система, причем компоненты А и В, а также В и С неограниченно растворимы друг в друге, а компоненты А и С ограниченно растворимы и в определенных соотношениях образуют двухфазную жидкую смесь. На рис. 5 кривая равновесия NKT — пограничная (бинодальная*- т.к. охватывает значение концентрации двух сосуществующих растворов). Каждая бинодальная кривая для данной системы соответствует определенной температуре, так как при изменении температуры изменяется растворимость и кривая меняет свое положение, которое определяется экспериментально. Обычно при повышении температуры область существования гетерогенной (расслаивающейся) системы уменьшается и, при так называемой критической температуре растворения, фазы рафината и экстракта сливаются в одну общую фазу.
Изменение давления в пределах 1—20 ат не оказывает заметного влияния на растворимость. Точки, лежащие внутри области, ограниченной бинодальной кривой, характеризуют двухфазную расслаивающуюся систему. Точка К — критическая точка, характеризующая состав, при котором расслоение растворов прекращается и образуется гомогенный раствор.
Область вне бинодальной кривой — область гомогенных (нерасслаивающихся) растворов.
Ветвь бинодальной кривой NK, характеризует составы рафината, а вегвь
КТ — составы экстрактов В области гетерогенных растворов каждому составу рафината R соответствует вполне определенный состав экстракта Е.
Прямые, соединяющие составы двух сосуществующих слоев рафината н экстракта (например, R1E1, R2E2, R3E3), называются линиями сопряжения *
Линии сопряжения не параллельны друг другу, так как компонент В, добавленный к какой-либо гетерогенной системе, неравномерно распределяется между рафинатом и экстрактом.
Процессы экстрагирования осуществляются только в области гетерогенных смесей. Так, если гетерогенная смесь общего состава характеризуется точкой М (рис. 5), то такая система образует две равновесные фазы, состав которых после расслаивания определится сопряженными точками R2 и Е2, лежащими на пересечении линии сопряжения, проходящей через точку М, с ветвями бинодальной кривой.
Количество образовавшихся при расслоении фаз рафината и экстракта можно определить, измерив в одинаковом масштабе отрезки прямой МЕ2 и МR2 из соотношения
R2/Е2 =МЕ2/МR2
С учетом приведенного соотношения, можно оценивать количества распределяющегося вещества в рафинате и экстракте.
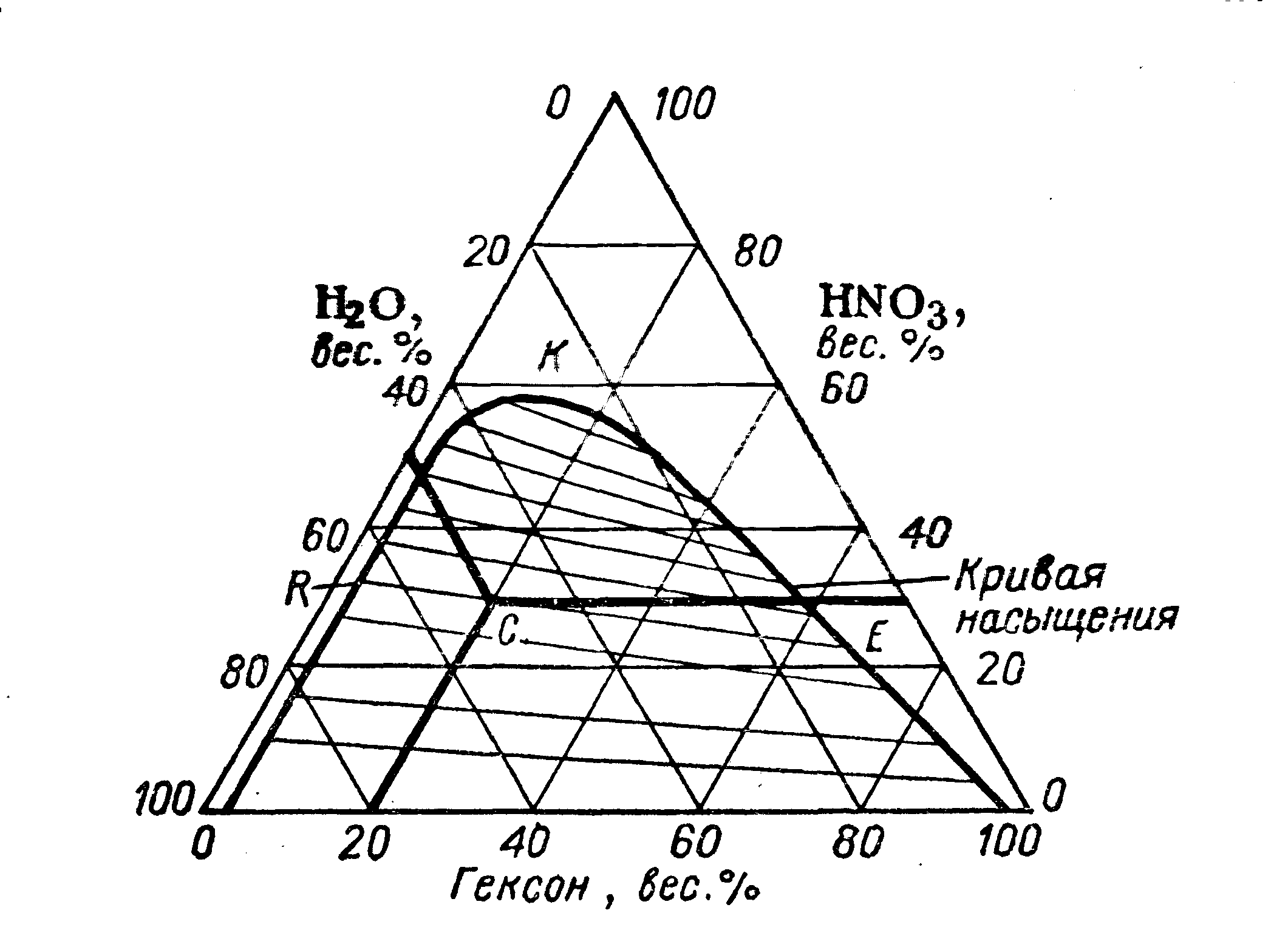
На рис.6 в качестве примера показана треугольная даграмма растворимости в системе СН3СОСН2СН(СН3)2 (гексон)-HNO3-Н2О при 25о. Вершины этого треугольника соответствуют чистым компонентам. Каждая точка внутри треугольника соответствует определенному соотношению концентрация этих компонентов: например точка С соответствует соотношению –гексон: Н2О: HNO3= 20:50:30. Пространство треугольника ограниченное кривой насыщения представляет собой гетерогенную область системы, расслаивающуюся при отстаивании на двефазы: фазу рафината(или остатка)R и фазу экстракта (или растворителя) Е. Количество этих фаз пропорционально длине отрезков RС и СЕ. Наклон линии сопряжения RЕ зависит от величины коэффициента распределения; при приближении к критической точке К этот коэффициент стремится к единице.
Пользуясь треугольными диаграммами, удобно рассчитывать состав фаз. Эффективность экстрагирования выражается обsчно коэффициентом извлечения Е, равным отношению количества компонента в фазе экстракта QE к количеству его в фазе рафината QR.
Коэффициент извлечения при достижении равновесия связан с коэффициентом распределения следующим равенством:
VE
E= K -----
VR
где VE- объем фазы экстракта; VR - объем фазы рафината; K- коэффициент распределения, равный отношению концентраций СЕ /СR. (см. формулу 1).
Очевидно, чем больше взято растворителя для экстракции, тем больше коэффициент извлечения.
На (Э) влияют: состав органического растворителя, валентность экстрагируемого иона, концентрация всех веществ, участвующих в образовании экстрагируемого соединения, рН раствора, наличие комплексообразователей, вещество мишени (если необходимо выделить изотоп без носителя), наличие высаливателей, температура среды, продукты радиолиза, возможность адсорбции.