
- •Глава II. Элементы зонной теории твердых тел.
- •§1. Энергетический спектр изолированных атомов.
- •§2. Адиабатическое приближение в квантовой теории твердых тел.
- •§3. Одноэлектронное приближение в квантовой теории твердых тел.
- •§4. Квантовая теория свободных электронов кристалла.
- •§5. Волновая функция связанных электронов кристалла.
- •§6. Волновые вектора связанных электронов кристалла.
- •§7. Образование энергетических зон электронов в периодическом поле кристалла.
- •§8. Инверсионная симметрия энергетических зон и приведенная зона Бриллюэна.
- •§9. Металлы, диэлектрики и полупроводники с точки зрения зонной теории твердых тел.
- •§10. Эффективная масса электронов в кристаллах.
- •§11. О состояниях между эффективными массами связанных и свободных электронов кристалла.
- •§12. Собственные полупроводники, понятие о дырках.
- •§13. Примесно – дефектные состояния в полупроводниках. Полупроводники n и p типов проводимости.
- •§14. Элементарная теория мелких примесных состояний полупроводника.
- •§15. Зонная структура полупроводника в пространстве.
Глава II. Элементы зонной теории твердых тел.
§1. Энергетический спектр изолированных атомов.
Изолированные
атомы представляют собой динамическую
систему, состоящую из неподвижного ядра
и вращающихся вокруг него электронов.
Ирншоу доказал, что система точечных
неподвижных зарядов находящихся, на
конечных расстояниях друг от друга не
является устойчивой системой, т.е. их
потенциальная энергия не может иметь
минимум, а атомы представляют собой
устойчивую систему, следовательно,
согласно теоремы Ирншоу они являются
динамическими системами. Полная энергия
атома равна
![]() ,
T – кинетическая энергия
электронов, U – потенциальная
энергия взаимодействия электронов с
ядром и друг с другом. Для определенности
рассмотрим атом с простейшей архитектурой
– атом водорода (H), у него
вокруг протона +1e вращается
электрон –1e.
,
T – кинетическая энергия
электронов, U – потенциальная
энергия взаимодействия электронов с
ядром и друг с другом. Для определенности
рассмотрим атом с простейшей архитектурой
– атом водорода (H), у него
вокруг протона +1e вращается
электрон –1e.
![]() ,
,
![]() ;
r – расстояние от электрона
до центра ядра, U – имеет
сферическую симметрию. Если
;
r – расстояние от электрона
до центра ядра, U – имеет
сферическую симметрию. Если
![]() ,
,
![]() ,
то движение электрона e
является связанным. Если
,
то движение электрона e
является связанным. Если
![]() ,
,
![]() ,
то движение электрона e
является свободным. Видно, что
,
то движение электрона e
является свободным. Видно, что
![]() ,
,
![]() .
.
Т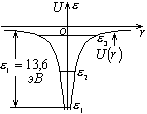 очную
характеристику о состояниях электронов
в атомах можно получить с помощью
квантовой механики, учитывающую волновые
свойства частиц. Состояния электронов
в атомах можно описывать с помощью
волновой функции, удовлетворяющей
уравнению Шредингера
очную
характеристику о состояниях электронов
в атомах можно получить с помощью
квантовой механики, учитывающую волновые
свойства частиц. Состояния электронов
в атомах можно описывать с помощью
волновой функции, удовлетворяющей
уравнению Шредингера
![]() .
Однако в общем случае решение уравнения
Шредингера это сложная задача, она легче
решается для стационарных условиях
электрона. Стационарная задача не
описывает процессы, она описывает
структуру системы в которой могут
протекать процессы.
.
Однако в общем случае решение уравнения
Шредингера это сложная задача, она легче
решается для стационарных условиях
электрона. Стационарная задача не
описывает процессы, она описывает
структуру системы в которой могут
протекать процессы.
Полную волновую функцию электрона атома водорода в стационарном состоянии можно представить в виде произведения:
![]() (1)
(1)
![]() - полная энергия электрона в n
состоянии.
- полная энергия электрона в n
состоянии.
Амплитудная
часть волновой функции
![]() должна удовлетворять стационарному
уравнению Шредингера:
должна удовлетворять стационарному
уравнению Шредингера:
![]() (2)
(2)
![]() (3)
(3)
![]() (4)
(4)
![]() ,
n = 1,2,3… (5)
,
n = 1,2,3… (5)
Из (4) следует, что атом водорода имеет дискретный спектр энергий, промежуточное состояние электрон принимать не может.
![]() .
Состояние с такой энергией называется
основным состоянием. В этом состоянии
атом имеет максимальную устойчивость.
А состояния с энергиями
.
Состояние с такой энергией называется
основным состоянием. В этом состоянии
атом имеет максимальную устойчивость.
А состояния с энергиями
![]() ,
,
![]() называются возбужденными.
называются возбужденными.
![]() - энергия ионизации водорода.
- энергия ионизации водорода.
Соотношение (5)
определяет энергию электрона в связанном
состоянии, как видно эта энергия
квантуется. Дискретность энергии
связанного электрона является следствием
проявления его волновых свойств. Движения
такого электрона схожи со стоячей
волной. Стоячая волна – это волна,
получающаяся в результате интерференций
двух одинаковых волн распространяющихся
в противоположных направлениях. В
связанном состоянии электронная волна
распространяется в ограниченном объеме
(в объеме атома). Как известно в этом
случае стоячие волны могут иметь только
определенное значение длин волн
![]() ,
,
![]() .
.
Из последнего соотношения следует, что λ стоячих электромагнитных волн принимает ряд дискретных значений и следовательно, и энергия связанного электрона принимает ряд дискретных значений.
Движение свободного электрона можно описывать бегущей волной, распространяющейся в неограниченном пространстве, а бегущая волна может принимать любое значение λ, следовательно, энергия свободного электрона не квантуется.
Если электрон
переходит из основного состояния
![]() в возбужденное
в возбужденное
![]() ,
то он поглощает энергию:
,
то он поглощает энергию:
![]() .
Если электрон переходит из возбужденного
состояния в основное, он испускает квант
энергии
.
Если электрон переходит из возбужденного
состояния в основное, он испускает квант
энергии
![]() .
.
Состояние
электрона в атоме водорода с энергией
![]() имеет кратность вырождения равной 2n2,
n – основное квантовое
число. Под кратностью вырождения следует
понимать число различных состояний при
данном значении энергии
.
Для электрона атома водорода, энергия
зависит только от основного квантового
числа n, следовательно,
вырождение будет определяться числом
различных значений орбитального (l),
магнитного (m) и спинового
(s) квантовых чисел.
имеет кратность вырождения равной 2n2,
n – основное квантовое
число. Под кратностью вырождения следует
понимать число различных состояний при
данном значении энергии
.
Для электрона атома водорода, энергия
зависит только от основного квантового
числа n, следовательно,
вырождение будет определяться числом
различных значений орбитального (l),
магнитного (m) и спинового
(s) квантовых чисел.
В многоэлектронном
атоме потенциальная энергия атома
определяется не только взаимодействием
электронов с ядром, но и взаимодействием
друг с другом. В связи с этим энергия
электронов зависит от дух квантовых
чисел (n, l).
Кратность вырождения состояния
![]() будет определяться числом различных
квантовых чисел m и s.
При данном квантовом числе l,
кратность вырождения 2(2l+1).
будет определяться числом различных
квантовых чисел m и s.
При данном квантовом числе l,
кратность вырождения 2(2l+1).
