
- •Сутек энергиясында жүретін «AlMobile» автокөлігінің жобасы
- •Абстракт
- •Абстракт
- •Теориялық бөлім
- •Сутек өндірісі
- •1.1 Қазіргі заманғы сутек энергетикасының ұғымы
- •Сутекті зерттеу тарихы
- •1.3 Сутекті өндіру тәсілдері
- •6 Сурет. Сірке қышқылы (этан қышқылы) - ch3cooh формуладағы органикалық зат
- •7 Сурет. Силикагель көмірқышқылды газды, сутекті, оттекті, азотты, хлорды және басқа да өнеркәсіптік газдарды кептіруге пайдаланады.
- •8 Сурет. Тікелей метанолды отын элементі
- •9 Сурет. Отын элементінің ішкі түрі.
- •2.2 Автомобильді басқару құрылғылары
- •Қорытынды
- •Қолданылған әдебиеттер тізімі:
- •Мазмұны
Сутекті зерттеу тарихы
Миллиард жылдар бұрын сутектің негізі – бір электрон және бір протон – барлық атомдардың 92%-на жуығын құрастырды, сол уақытта қалған заттар гелий элементінен тұрды. Бүгінде 15 миллиард жыл кейін әлемдегі барлық бөлшектердің 90%-на жуығы сутектің атомдарынан тұрады, ал осы бөлшектердің 9% ғана гелий атомдарынан құралады.
Сутек барлық жерде бар. Американың физигі Джон Риджен дәлелдегендей, «сутек – барлық атомдар мен молекулардың бастауы.»[3]
Сутегінің тұңғыш ғылыми ашылуын көбінесе Парацельс лақап атымен танымал, Ренессанс дәуірінің физигы және алхимигы Теофраст Бомбаст фон Гогенгейм есімімен байланыстырады. Ол қышқылдар металлдармен әрекеттескенде отқауіпті газ бөлінетініне тәжірибе өткізіп, ғылыми бақылау жүргізді. Ағылшын ғалымы Генри Кавендиш (1731-1810) 1766 жылы сутекті бөлек зат ретінде ашқаны үшін және оның түрлі қасиеттерін сипаттап жазғаны үшін марапаттауларға иеленді. Ол сутекті «жанатын ауа» деп атады және де сутек пен оттек реакциясынан су құраған ең бірінші химик болды. Ал француз ғалымы Антуан Лавуазье (1743-1794) 1793 жылы Кавендиштің еңбегін зерттей келе, өзінің тәжірибелерінде сутекті зерттеуді қайталады әрі бақылауларын ұлғайтты. Лавуазье ашқан элементін «су» және «құрау» деген екі сөзден тұратын гректің hydrogene сөзімен атады.
Сутектің абсолютті жанатындығы, сарқылмас қоры және қуаттылығы жайлы алғашқы ойлар 19-шы ғасыр әдеби жазушыларының туындыларында орын алды. Сәуегей жазушы Жюль Верн өзінің романдарында суды сарқылмас отын ретінде тұжырымдайтын кейіпкерлерді сипаттап жазды. «Жұмбақ арал» кітабындағы инженер Сайрус Смиттің айтуынша: «Су – келешектің көмірі».[4]
1.3 Сутекті өндіру тәсілдері
Сутек өндірісі – бастауын өткен ғасырлардан алатын коммерциялық жүйесі бар, өте үлкен, заманауи өнеркәсіп. Ғаламда сутек екі түрлі әдіспен өндіріледі. Біріншісі – нитроген мен сутекті қосу арқылы аммонийді (NH₃) синтездеу. Екіншісі – мұнай өңдейтін зауыттардағы мұнайды жоғарғы қысымда гидро-өңдеу немесе гидро-тазалау. Бұл процессте ауыр дымқыл мұнай транспорт отынына айналу немесе өңделген жанармайды тазарту жұмыстары жүргізіледі.
Жаһандық жылдық өндіру шамамен 45 миллиард килограмм немесе нормадағы 500 миллиард м³ (норма: 1 атм. қысым мен 0ºС-дағы кубтық метр) құрайды. Сутекті төменде талқыланатын дәстүрлі отын түрлерінен әр түрлі процесстер арқылы өндіреді[5]:
Шығу тегі |
Саны (млд. Нм³/г) |
Пайызы ( %) |
Табиғи газ |
240 |
48 |
Мұнай |
150 |
30 |
Көмір |
90 |
18 |
Электролиз |
20 |
4 |
Жалпы |
500 |
100 |
Табиға газ (метан, СН₄) – бүгінгі күндегі сутектің ең көп таралған қоры[6]. Метан әлемнің жартысынан жуық және АҚШ-тың 90 пайыз сутек мөлшерін өндіреді[7]. Метаннан сутекті бөлу процессі өзі екі процесстен тұратын метанның бу конверсиясы деп аталады. Бірінші процессте (әдетте никельмен) катализаторлармен толтырылған, жоғарғы қысым (15-тен 25 атм. қысым) мен жоғарғы температурадағы (750ºС-1000ºС) құбырлардың ішінде табиғи газ (метан) су буымен (Н₂О) реакцияға түсіп, көміртек моноксиді (СО) мен сутек құрайды:
СН₄ + Н₂О → СО + 3Н₂
Су-газ конверсиясы деп аталатын екінші реакцияда СО су буымен әрекеттесіп, СО₂ және сутек жасайды:
СО + Н₂О → СО₂ + Н₂
Бұл реакция 200ºС-тан 475ºС-қа дейінгі температурада бір немесе екі кезеңде жүзеге асады.
Реактордан ұшып шыққан газ түтіндерінде СО₂, СН₄, су буы мен СО-дан басқа шамамен 70-тен 80%-ға дейін сутек болады. Кейін сутек түпкілікті тұтынуы үшін әр текті, араласқан газдардан бөлініп шығарылады. Сутекті толық тазарту үшін әдетте адсорбция қысымын пайдаланады.
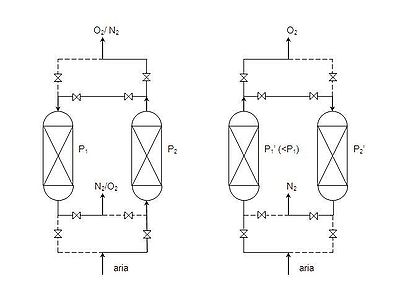
Сурет 1. Адсорбционды генераторлар газ буын гидро-тазарту кезінде қолданылады
С О₂
қалдықтары дағдыда атмосфераға
шығарылады. Жаһандық жылудың күшеуіне
және экологиялық жағдайларға байланысты
метанның бу конверсиясы және адсорбция
процесстері біздің қоршаған ортамызға
өте зиянды болып келеді.
О₂
қалдықтары дағдыда атмосфераға
шығарылады. Жаһандық жылудың күшеуіне
және экологиялық жағдайларға байланысты
метанның бу конверсиясы және адсорбция
процесстері біздің қоршаған ортамызға
өте зиянды болып келеді.
:
Метан

Күкірт арқылы тазарту

Бу конверсиясы
CH₄ + H₂O → CO + 3H₂
температура 880ºС
Бу
CO₂ + H₂O → CO₂ + H₂
Бу
СО
СО СН₄
СН₄
Бөліну және тазарту
Н₂ сығу
С
Кеңейту немесе сақтау
урет 2. Метанның бу конверсиясыБұл екеуі өндірістегі дамыған коммерциялық процесстер болып саналады. Метанның бу конверсиясы үшін энерго-өнімділік (өндірілген сутек энергиясының берілген отын энергиясына қатысты арасалмағы) шамамен 70%-ды құрайлы.
Су – бұл сутек өндіруде кеңінен қолданылатын ресурс. Суды сутек пен оттекке бөлу үшін сырттан электрэнергиясын қажет ететін элекролиз процессі – қоспасыз таза сутекті өндіру үшін қолданылатын дүниежүзінін дамыған технологиясы.
Дегенмен, бұл өте энергокөлемді процесс, және де бір килограмм сутекті шапшаңырақ өндіру үшін қуат көбірек қажет етіледі. Қарапайым коммерциялық электролиздер 50 кВт қуатты қажет етеді, бұл энергияның 70 % тиімділігін көрсетеді, яғни сутектегі энергияның 1 бірлігін өндіруге өзге энергияның 1,4 бірлігі жұмсалуы қажетті. Өйткені электроэнергияның басым бөлігі қазбалы отындардан өндіріледі және орташа органикалық отында 30% энергияның тиімділігіне жуығы бар, жалпы ПӘК-і 20% шамаланады – энергияның 4 бірлігі сутекті энергияның әрбір бірілігінде сутекті өндіру кезінде тасталынады. Осы жағдайда қуаттың өте көп жұмсалуы жүреді.
Бірақ табиғи газдың булы конверсиясымен салыстырғанда электролиздің үлкен қондырғаларын қондыру арзанырақ – олардың жергілікті қалалық ЖҚС-лардағы дәл осындай, бірақ аумағы кішкентай қондырғыларымен (тек сутек энергиясы өте қажетті жерлерде орналасатындығынан кейде «аула қондырғылары» деп аталады) салыстырғанда электроэнергия бағасы көп есе арзанырақ түседі.

Сурет 3. Электролизёр — судан сутегі өндіретін қондырғы
Жаһандық жылымықтың болашағына қарай отырып, электролиз процессінің келешекте мағынасы шамалы, себебі, электролиз бен орталық станциялардан электр энергиясын өндіру тиімді емес процесстер болып келеді және дүниежүзі елдерінің көбі электр энергияны көбінесе қазбалы кендерден өндіреді. Алайда, 1 галлон жанармайдың жануы ауаға шамамен 9 кг қос оксидті көміртек газын таратады. Электролиз процессі арқылы өндірілген 1 кг сутектен ауаға орташа 70 фунт (шамамен 31 кг) көміртек қышқылын босатады. Жанармай галлоны килограмм сутектің энергиясына тең. Электролиз процессінің көмегімен сутек өндіретін отын элементтері орналастырылған автомобильдерде, оның потенциалды екі еселенген пайдалы әсерін есептегенмен де, бүкіл планетада жаһандық жылымықтың күшеюіне әсер етпей қоймайды.
Бұдан басқа сутек жаңартылмалы электр қуаттарынан өндіріледі, бірақ қазіргі уақыттың жергілікті өндіріске ең қолайлы жаңартылмалы жүйесі – күн энергиясының фотоэлектрикалық қондырғысы – сутек өндірісінде қымбатшылықты тудырып отыр, ал әлемнің ең арзан жаңартылмалы энергиясының – жел күшінің саны – жел қондырғыларының жылдам қадаммен дамуына қарамастан, бүкіл дүниеде энергияның шағын үлесін ғана қамтып отыр.

Сурет 4. Күннен энергия өндіретін фотоэлектрикалық қондырғылар
Көмір де – сутегі өндірісінде басты қорлардың бірі. Сутекті өндіру үшін әуелі көмірді газ түріне келтіреді, бөгде заттардан тазартады, сосын ғана одан сутек газын бөлу процессін жүргізеді. Бұл процессте СО₂ газының ауаға таралуы аумақты түрде өтеді, сондықтан, жаһандық жылыну проблемасына байланысты, көмірді заманауи газ түріне айналдыру технологиясы сутек экономикасының негізі бола алмайды. Көмір әлемнің көп елдерінде ең жеткілікті пайдалы қазба ретінде саналады. Мысалы, Қазақстанда көмірдің жалпы қоры 162 млрд тоннадан асады[8].
Биомассалар – сутекті өндірудегі маңызды қорлардың бірі. Биомассалар – өсу айналымына қатысқан әр түрлі материалдар, мысалы: тамақтың, ағаштардың, агромәдениеттің қалдықтары. Энергия егісі ретінде өсірілген өсімдіктер де биомасса құрамына кіреді. Биомассалар да жаһандық жылымықтың күшеюіне әсер тигізетін қаупі бар, себебі, егер биомассалар өртенсе, олардан көмірқышқыл газы бөліне бастайды. Алайда, кейін зиянды газ қайтіп биомассалардың бойына сіңеді, яғни өсу айналымына қатынасады. Сол себепті, биомассалар планетаның жылуына ешбір әсер етпейтін потенциалды шыдамды энергия көздері болып табылады. Биомассаны этанол секілді сұйық отынға айналдырып, жанармай қоспасы ретінде қолдануға болады. Қазіргі заманда жүгері дәндерінен жасалған био-отын – этанол - әлемдегі басты экологиялық таза отын түрі болып есептеледі. Этил спирті, этанол, С2Н5ОН – біратомды қаныққан-алифатты спирт, түссіз, күйдіргіш дәмі және өзіндік исі бар оңай қозғалатын сұйықтық[17]. Келешекте жүгеріден басқа, өсуге және егісті жинап алуға сырттан азғантай энергия көзін қажет ететін тары дәндерінен этанол өндіру жұмыстары көп үміт күттіреді.


Сурет 5. Жүгеріден отын өндіру
Биоэтанолды 2005 жылы 36,3 млрд литр, оның 45% Бразилия және 44,7% АҚШ елдерінде ғана өндірді. Биоэтанолды Бразилияда үлкен көлемде қант таяқшаларынан, ал АҚШ-та жүгеріден жасайды. Этанол бензинге қарағанда аз энергия сақтау көзі болып табылады. 85% этанол мен 15% бензин қоспасында жұмыс істеген машинаның жүрісі стандартты машина жүрісінің көлемдік отынның бірлігіне шамамен 75% құрайды. Ал тек таза этанолда тек «Flex-Fuel» машиналар («жұмсақ отынды» машина) ғана жұмыс істей алады. Бразилия отын ретінде биоэтанол мен қант таяқшаларын өндіру мен қолдануда көш бастап тұр. Қозғалтқышта этанолды жаққанда одан альдегидтер (формальдегид және ацетальдегид) пайда болады. Ал бұлар өз кезегінде ароматты көмірсутекерге қарағанда тірі организмдерге екі есе көп зиянды заттар шығарады.
Биомассының жержаңғақ қабықтары және жом (қант тростнигінің қалдығы) сияқты қалдықтары тиімді ресурс ретінде саналуға мүмкіндіктері мол, бірақ мұндай биомассаларды тасымалдау шектелген.
Әлемде сутекті өндіру жағынан өте көп жаңа стратегиялар бар, мысалы, суды тура жолмен ажырату үшін фотоэлектрикалық қондырғыларды қолдану көмегімен, күн энергиясы арқылы тікелей сутекті өндіру жолы ғылыми мәнділігі жағынан зерттелуде. Сутекті өндіруде белсенді биологиялық процесстердің маңызы зейінсіз қалмайды, мысалға, сутек өніміне арналған фотосинтез процесстерінің бейімделуі және органикалық құрылымдарды сутекке ажырату үшін арналған биоинженерлік бактериялардың қолданылуын айтуға боларлық.
Соңғы уақыттары сутекті өндіруде отын элементтерінің қолданысы көбеюде, мысалы, жоғарғы температуралы отын элементтері бір мезетте электр энергиясын, жылуды және сутекті тудырады. Табиғи газ көмегімен жасалынған отын элементтері энергия өндіруде метан (СН₄) құрамындағы сутектің шамамен ¾ атомдарын қолданады.
Отын элементтері тиімсіз, өте көп айырылуларды тудыратын жану процессінен алшақтап, отынның химиялық энергиясын оңай жолмен электр энергиясына айналдырады. Бұл электрохимиялық қондырғы отынның тиімділігі жоғары «суық» жануы әсерінен тікелей жолмен электр энергиясын өндіреді[9].
Отын элементтерінің түрлері:
Фосфор қышқылынан тұратын отын элементі, аты айтып тұрғандай, электролит ретінде фосфор қышқылын қолданады. Тұңғыш отын элементі электролит есебінде күкіртті қолданды. Дәл осындай отын элементтері қазіргі уақытта ең дамыған технологиялар болып табылады.
Еріген карбонаттан тұратын отын элементі электролит ретінде сұйық карбонатты қолданады. Осындай элементтер қырық жол бойы зерттеудің және дамытудың маңызды субъектісі болды. Олар 47%-дан 50%-ға дейінгі ПӘК-ті қамтиді.
Қатты оксидті отын элементі электролит ретінде керамиканы қолданысқа енгізеді. Мұндай отын элементтері 1800ºF жоғары температураларды шыдайды және ауа, табиғи газбен (немесе басқа да отын түрлерімен) тікелей әрекеттесе алады.
Протон ауыспалы мембранасы бар отын элементі (басқаша полимерлі электролиттік мембранасы бар отын элемент ретінде таныс) иілімді электролиттен тұрады. Мембрананың материалын алғаш рет DuPont компаниясы жасап шығарды. Бұл мембрананың сыртқы көрінісі тамақты сақтауға арналған иілімді орама қағаз сияқты. «Протон» сөзі полимерлі мембранадан өтетін сутек иондарын білдіреді. Мұндай отын элементтерінің потенциалы автомобильдердің іштен тұтанатын қозғалтқыштарын алмастыра алу қасиетімен әлемде басқа отын элементтеріне қарағанда жақсырақ мәлім. Осындай отын элементтерін үйде, кеңселерде және фабрикаларда қолдануды қазіргі уақытта түрлі компаниялар дамытып және көбейтіп жатыр.
Отын элементінің құрылысы
2.1 Автомобиль құрылысы және оның отын жүйесі
“AlMobile” автомобилін жасау барысында алдымен автомобиль ішінде өтетін сутек өндірісі кезіндегі химиялық және электрохимиялық реакцияларды есептеу, өндірілген сутекті тазарту үшін фильтр жүйесін жасау және құрылғының отын элементі жүйесін сипаттау мәселелерін шешуді қажет ететін, негізгі техникалық мәселелерге назар аудару қажет.
Радио байланыс арқылы басқарылатын “AlMobile” келешек автомобилі алюминий қалдықтары мен судан нәр алады және кәдімгі натрий гидрооксидін катализатор ретінде қолданады.
Алюминий қалдықтары (біздің жағдайда, шөліңді қандыратын сусынның сыртқы құты) натрий гидроксиді ерітілген суы бар ыдысқа орналастырылады.
Алюминий жеңіл металлдар тобына жатады. Ол әлемде кеңінен таралған металл әрі жер қыртысындағы оттек пен кремнийден кейін үшінші орында тұрған химиялық элемент. Тұңғыш рет алюминийді 1825 жылы дат ғалымы Ганс Эрстед сынаптың кейінгі қайнатып алуынан калий амальгамының алюминий хлоридімен әсері кезінде ашты. Элемент атауы латынның aluminis – «ашытқы» сөзінен шықты. Алюминийдің оттекпен өте берік химиялық байланысы бар. [10]
Алюминий – жеңіл және иілімді ақ түсті металл, жұқа оксид қабатына байланысты күңгірт күміс түсті болып келеді. Ол химиялық элементтердің периодтық жүйесінде III- топқа кіреды, Al белгісімен белгіленеді, атомдық нөмірі 13-ке және атомдық массасы 26,98154-ке тең. Балқу температурасы 660ºС. Алюминий әлемде кеңінен таралған: осы параметрі жағынан ол бүкіл элементтердің ішінен 4-ші орынға, ал металлдардың ішінен 1-ші орынға (жер қыртысының 8,8% массасына) ие, бірақ таза күйінде ешбір кездеспейді. Оны әдетте бокситтерден өндіреді және алюминий минералдарының (алюмиосиликаттар, алуниттер, т.б.) 100 түрі белгілі, олардың көбісі алюминий өндіруге жарамсыз болып келеді.
Қолданысының кең шоғырына арқау боларлық алюминийдің керемет қасиеттері бар. Өндірістің түрлі салаларында қолданылуы жағынан алюминий тек темірден ғана қалыс қалады. Қақтауға төзімді әрі иілімді алюминий түрлі формаларды қабылдай алады. Оның оксид қабаты коррозияға қарсы беріктігін ұлғайтады, сондықтан оның қолданылу мерзімі өте ұзақ уақытты қамтуы мүмкін. Бұдан басқа, алюминийдің жетістіктеріне оның жоғары ток өткізу қабілеті, улағыш емес қасиеті және қайта жасап шығару жағынан жеңілдігі жатады.

Сурет 6. Таза күйінде өндірілген алюминий
Алюминийдің қасиеттері оның әлем экономикасында жеңіл металл ретіндегі маңызын ұлғайтады. Ол - автомобиль, жүйрік пойыздардың вагондарын, кемелерді жасауда өте қажетті материал. Қазіргі заман құрылысында алюминийден жасалған құрылыс өнімдері қолданылады. Алюминий электр тогын өткізетін жоғарғы вольтты сымдарда толықтай дерлік мыстың орнын басты. Әр жыл сайын сатылатын тамақ жасауға қажетті ыдыс-аяқтардың жартысынан жуығы алюминийден жасалады. Дүкендерде сатылатын шөліңді қандыратын сусынның сыртқы құтын және қаптама қағазды (фольга) алюминийден басқа басқа металлдан жасалған түрін елестету қазіргі уақытта мүмкін емес. 2007 жылы әлемде әуелгі алюминийдің 38 млн т, ал 2008 жылы 39,7 млн т шығарылды. [11]
Алюминий – белсенді металл, бірақ сыртқы оксид қабатына байланысты оның сыртқы беті сумен әрекеттеспейді және қышқылданбайды. Алайда, оның сыртқы оксид қабатын алып тастасақ, алюминий белсенді түрде сумен әрекеттеседі.
Натрий гидроксиді (лат. Natrii hydroxidum; басқаша атаулары – күйдіргіш сода, каустик, күйдіргіш натр, күйдіргіш сілті) – ең көп таралған сілті, химиялық формуласы NaOH. Жыл сайын әлемде 57 тоннадан көп күйдіргіш натрий өндіріледі және қолданылады. Натрий тотығының гидраты NaOH – ақ түсті қатты зат. Егер күйдіргіш натрдың бір бөлігін ауада қалдырып кетсек, көп ұзамай ол сыртқа жайылып кетеді, себебі, ол ауаның барлық ылғалын өзінің бойына сіңіріп алады. Күйдіргіш натр суда жақсы ериді, әсіресе еру кезінде сыртқа көп мөлшерде жылу бөледі. Күйдіргіш натрдың ерітіндісі жақсы көпіреді.[12] Бұл біздің автомобильге қажетті қасиеттің бірі, себебі, су мен алюминий арасындағы химиялық әрекеттесуді бастау үшін натрий гидроксидінің жылу бөлу және көпіргіш қасиеті өте маңызды.


Сурет 7. Алюминий құтылары және натрий гидрооксиді
Натрий гидроксиді алюминиймен реакцияға түседі. Ол темір және мыспен (электрохимиялық потенциалы өте төмен металлдармен) әрекеттеспейді. Алюминий күйдіргіш сілтінің құрамында натрий тетрагидроксиалюминаты және сутек өндіру арқылы жеңіл ериді:
2Al0 + 2NaOH + 6H2O → 3H2↑ + 2Na[Al(OH)4]
2Al0 + 2Na+ + 8OH− + 6H+ → 3H2↑ + 2Na+[Al3+(OH)−4]− [13]
Біздің автомобильде алюминий мен судағы натрий гидроксидінің ерітіндісінде реакция жүреді:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Алюминий қалдықтары еріген натрий гидроксидімен әрекетке түскенде, сутек, кейін қайта қолданыла алатын натрий тетрагидрооксиалюминатын өндіреді. Бұл химиялық реакция алюминийдің өмір сүру кезеңін аяқтайды. 3 килограмм сусынның құтысы автомобильдің 1 сағатта жүру қуатына жетеді.
Әрі қарай бөлінген водород тазарту (фильтрация) жүйесіне өтеді. Ол екі кезеңді тазартудан тұрады. Тазартудың бірінші кезеңінде сірке қышқылы пайдаланылады. Сутек гидроксид қалдығын ұстап қалатын су мен сірке қышқылынан, тікелей тазартудан өтеді.


