
- •Способы очистки от взвешенных веществ
- •Окисление.
- •Хлорирование.
- •Окисление о2 воздуха под давлением.
- •Озонирование.
- •Электрохимические методы.
- •Метод электрокоагуляции
- •Электролиз. (окисление)
- •Метод гальванокоагуляции
- •Электродиализ.
- •Выводы.
- •Биологическая очистка воды
- •Контроль качества питьевой воды
- •Правила
Окисление.
Очистка производственных СВ. Метод применяют для окисления HCN,цианидов, H2S, HS- метилмеркаптана, хлорпроизводных органических в-в, фенолов, ПАВ, нефти.
Важным моментом является выбор окислителя. Ниже приведены основные окислители и значения окислительно-восстановительного потенциала. Как правило, чем больше E0 , тем эффективней окислитель:
Cl2 E0=1,36 (B)
HClO 1,50 (pH<7) ; 0,88 (pH>=7)
ClO4- 1,38 ; 0,56
O3 2,07
H2O2 1,77 ; 0,88
MnO4- 1,7-1,5 ; 0,57
FeO42- 2,20 ; 0,72
CH3COOOH 1,8
Самые распространённые, дешёвые и простые – кислородом воздуха и хлорированием.
Хлорирование.
Для обезвреживания цианидов согласно СНиП 2.04.03-85 применяют окисление реагентами, содержащими активный хлор:
Cl2 + H2O=>HCl + HClO
HClO = H+ + ClO
К таким реагентам относятся жидкий хлор, хлорная известь, гипохлориты Са и Na. Чаще всего используют NaClO, обеспечивающий наибольшую технологическую безопасность процесса. Водный р-р NaClO выпускают в промышленном масштабе С=180-200 г/л. Вследствие гидролиза раствор имеет щелочную реакцию:
NaClO+ H2O= HClO + Na+ + OH
При pH=6-8 в растворе присутствуют HClO и ClO в соизмеримых кол-вах, идёт р-я диспропорционирования:
2HClO + ClO => ClO3 +2Cl + 2H +
При Т>70° С реакция становится преобладающей.
Цианиды переходят в цианаты:
CN + ClO => CNO + Cl
Последние быстро подвергаются гидролизу:
CNO +2H2O => HCO3 + NH3
Аммиак окисляется до азота:
2NH3 + 2ClO => N2 + 2H2O + 2HCl
Суммарная реакция:
2CN + 5 ClO + H2O => 5Cl +2 HCO3 + N2 + Q
Чтобы избежать перегрева, концентрацию циансодержащего раствора подбирают, чтобы она не превышала 10,6 г/л по CN (20 г/л NaCN). Вследствие гидролиза такой раствор имеет щелочную среду pH≈11,2. Обезвреженный раствор pH≈8,7. При pH<9,2 возникает опасность образования хлорциана при взаимодействии цианидов с оксидом хлора (Cl2O), образующимся по реакции разложения хлорноватистой кислоты.
CN-+Cl2O = ClCN + ClO-
Образование хлорциана легко обнаруживается по слезоточивому действию. Начальная раздражающая С 0,002 мг/л.
Чтобы этого избежать, в раствор необходимо добавлять щёлочь.
2СN+5ClO- +2OH- => CO32- +N2+5Cl-+H2O+Q
2NaCN+5NaClO+2NaOH=>2Na2CO3+N2+5NaCl+H2O
Q=1815,83 кДж/моль
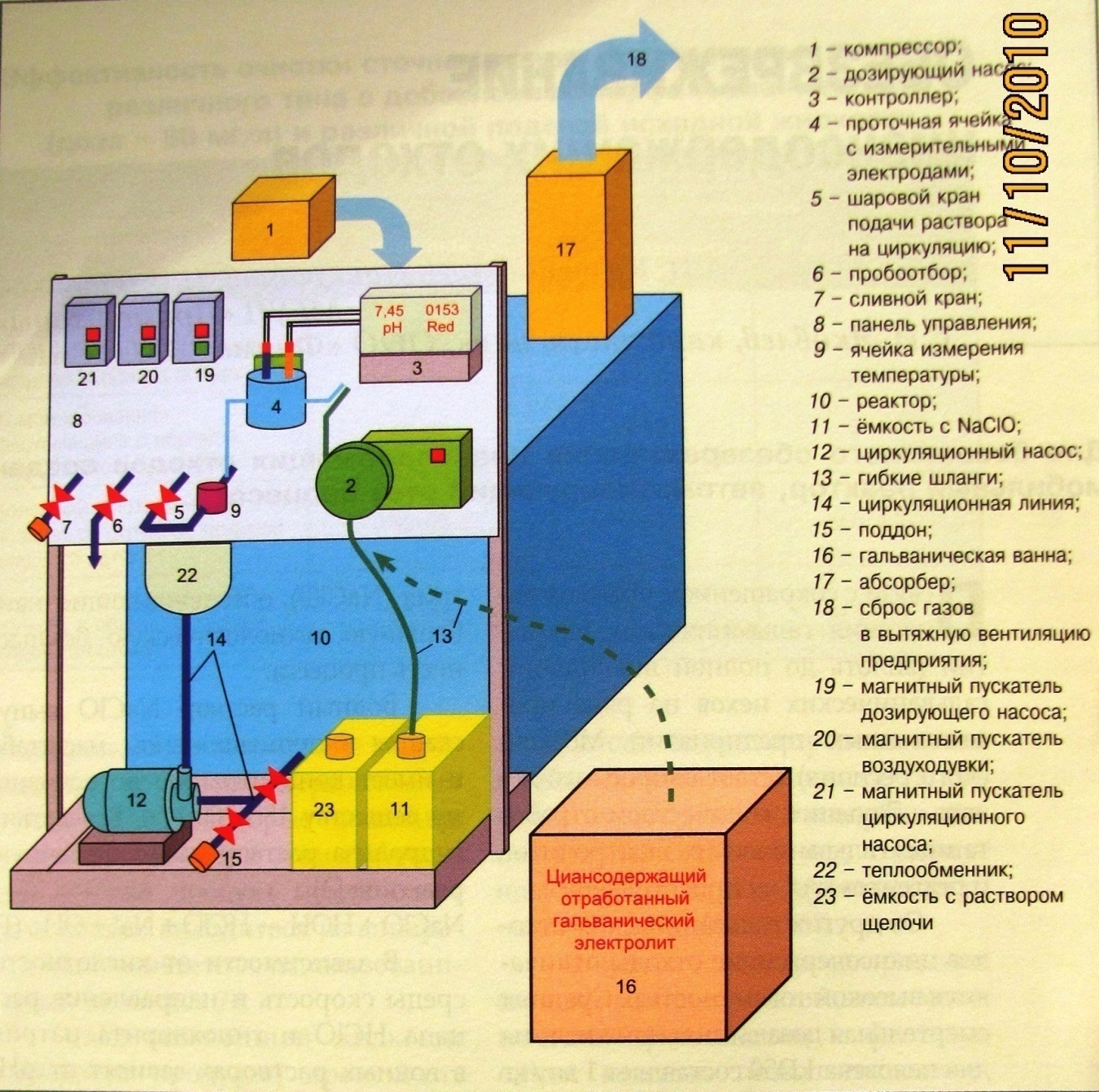
На рисунке представлен общий вид мобильной установки по обезвреживанию цианидов, в которой проходят вышеперечисленные реакции. Основа установки – реактор 10 из толстостенного полиэтилена V≈0,6-1 м3 . Циансодержащий раствор из ёмкости 16 и раствор гипохлорита из 11 по шлангам 13 насосом 2 подаются в реактор. Выполнение условий для оптимального протекания процесса определяется в проточной ячейке с измерительными электродами 4, соединённой с контроллером 3. Последний даёт команды насосу для подачи растворов цианидов, а также расчётного количества гипохлорита из ёмкости 11 и щёлочи из 23 для поддержания pH≈11. Система циркуляции раствора обеспечивает поддержание Т не более 70° С. Это достигается засчёт наличия ячейки измерения Т 9, передающей показания на контроллер, с которого команды поступают на шаровой кран 5 для подачи раствора на циркуляцию, которая осуществляется с помощью насоса 12 через теплообменник 22. Выделяющиеся газы через абсорбер 17 в системы вентиляции 18. По завершении через пробоотборник 6 отбирается проба для анализа на отсутствие цианидов в растворе.
Рис.1 Пример установки (опытная, мобильная) по обезвреживанию СВ от цианидов.
При хлорировании воды с последующей сорбцией на активном угле происходит удаление аммонийного азота. При хлорировании воды, содержащей аммонийный азот, в зависимости от рН, соотношения дозы активного хлора и концентрации аммонийного азота образуется смесь монохлораминов, дихлораминов, треххлористого азота, сорбируемых при фильтрации активным углем, и молекулярного азота, уходящего в атмосферу.
Недостатком способа является увеличение концентрации хлоридов в очищенной воде, особенно при обработке сточных вод с относительно высокой концентрацией аммонийного азота; преимуществом - увеличение срока службы угля до замены или регенерации за счет окисления органических веществ хлором на пористой поверхности угля, более высокая степень очистки от органических веществ, полное обеззараживание воды, удаление аммонийного азота с превращением в молекулярный азот, уходящий в атмосферу.
