
1.3 Определение атомной массы металла
Вычислив таким образом удельную теплоёмкость металла, можно определить его приближённую атомную массу по правилу Дюлонга и Пти. Атомная теплоёмкость большинства простых веществ в твёрдом состоянии лежит в пределах 22 ÷ 29 Дж/моль·°К (в среднем около 26 Дж/моль·°К).
Атомная теплоёмкость представляет собой количество теплоты необходимое для нагревания 1 моля атомов элемента на 1 º С.
8
Тогда правило Дюлонга и Пти можно сформулировать следующим образом: произведение удельной теплоёмкости простого вещества в твёрдом состоянии на мольную массу атомов соответствующего элемента для большинства элементов приблизительно одинаково и равно 26 Дж/моль·°К:
М·С ≈ 26 Дж/моль·°К, (1.7)
где:
М – мольная масса (численно равная ей атомная масса);
С – удельная теплоёмкость.
Из правила Дюлонга и Пти следует, что разделив 26 на удельную теплоёмкость простого вещества, можно найти приближённое значение мольной массы атомов, а значит, и численно равное ей приближённое значение атомной массы.
Точное значение атомной массы находят, сравнивая это значение с эквивалентной массой. Атомная и эквивалентная масса связаны соотношением:
Эквивалентная масса = |
Атомная масса |
(1.8) |
Валентность |
Пользуясь этой зависимостью, можно по удельной теплоёмкости и эквивалентной массе определить точную атомную массу металла.
Пример: Эквивалентная масса индия равна 38,273 г/моль; удельная теплоёмкость этого металла 0,222 Дж/г·°К. Определить точную атомную массу индия.
Сначала на основании правила Дюлонга и Пти определяем приближённую мольную массу атомов индия:
26 : 0,222 = 117 г/моль
Затем делением этой приближённой величины на эквивалентную массу находим валентность индия:
117 : 38,273 ≈ 3
Умножая эквивалентную массу на валентность, получаем мольную массу атомов индия:
9
38,273 · 3 = 114,82 г/моль
Следовательно, атомная масса индия равна 114,82 а.е.м.
2 Описание установки
Для определения удельной теплоёмкости пользуются калориметром, который состоит из двух стаканов, вставленных один в другой. Внутренний стакан (1) ёмкостью 150 мл для уменьшения теплоотдачи поставлен на корковую пробку (2). Через асбестовую или картонную крышку (3), закрывающую внешний стакан (4), проходит термометр (5).
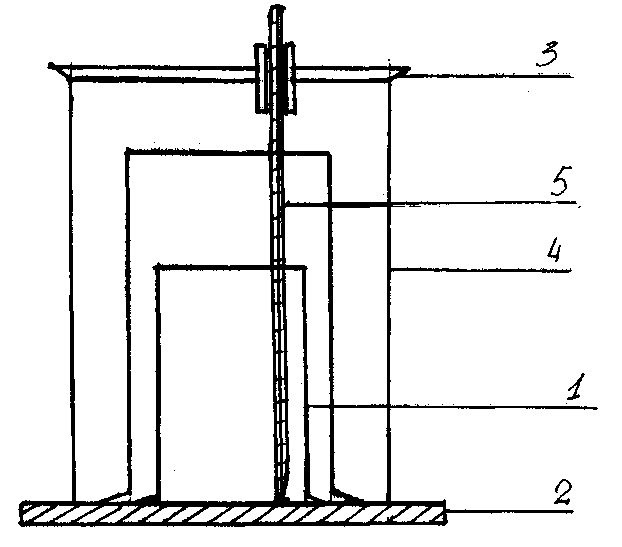
Рисунок 1
10
3 Методика выполнения работы
1 Включить электроплитку, поставить на неё сосуд с водой и нагреть воду до кипения.
2 На техно-химических весах взвесить кусочек исследуемого металла, привязать его на нитку и опустить на 10 – 15 минут в кипящую воду.
3 Взвесить внутренний стакан калориметра, налить в него 50 ÷ 70 мл. воды и ещё раз взвесить.
4 Поместить этот стакан на его место в приборе и определить температуру воды.
5 Нагретый до 100º С (в кипящей воде) металл быстро перенести в воду калориметра, прикрыть калориметр крышкой и, помешивая термометром (осторожно!), установить наивысшую температуру, которую примет вода за счёт теплообмена с металлом.
Пользуясь описанной методикой, определить удельную теплоёмкость металла. Затем рассчитать приближённое и точное значение атомной массы. Посчитать % ошибки. Данные занести в таблицу.
Таблица 1-Результаты измерений
Mм |
mж |
mк |
t1 |
Θ |
cм |
А' |
А |
% ошибки (относит.) |
|
|
|
|
|
|
|
|
|
11
