
- •1. Основные положения
- •§ 1. Предмет технической
- •§ 2. Термодинамическая система.
- •Лекция 2
- •§ 1. Уравнения состояния идеальных
- •§ 2. Газовые смеси
- •Лекция 3 теплоемкость газов
- •§ 1. Истинная и средняя теплоемкости
- •§ 2. Изобарная и изохорная
- •1. Значения молярных теплоемкостей и коэффициента k в зависимости от атомности
- •§ 3. Теплоемкость газовых смесей
- •Лекция 4 первый закон термодинамики
- •§ 1. Термодинамический процесс
- •§ 2. Работа расширения газа
- •§ 3. Теплота
- •§ 4. Первый закон термодинамики
- •Лекция 5 термодинамические процессы в газах
- •§ 1. Метод исследования
- •§ 2. Изохорный процесс
- •§ 3. Изобарный процесс
- •§ 4. Энтальпия газа
- •§ 5. Изотермический процесс
- •§ 6. Адиабатный процесс
- •§ 7. Политропный процесс
- •§ 8. Анализ политропных процессов
- •2. Результаты анализа политропных процессов
- •Лекция 6 второй закон термодинамики
- •§ 1. Круговые процессы
- •§ 2. Прямой обратимый цикл карно
- •§ 3. Обратный обратимый цикл карно
- •§ 4. Сущность и формулировки
- •§ 1. Общие понятия об идеальных циклах
- •§ 2. Циклы газотурбинных установок
- •§ 3. Термодинамические основы работы
- •Лекция 8 водяной пар
- •§ 1. Основные понятия и определения
- •§ 3. Основные термодинамические
- •Лекция 9 циклы паросиловых установок
- •§ 1. Цикл карно для водяного пара
- •§ 2. Цикл ренкина
- •§ 3. Влияние основных параметров пара
- •Лекция 10 влажный воздух
- •§ 1. Физические свойства
- •Лекция 11 основы теплообмена план
- •1. Теплопроводность
- •§ 1. Основные понятия и определения
- •§ 2. Закон фурье
- •§ 3. Частные случаи теплопроводности
- •Лекция 12 конвективный теплообмен. Теплообмен излучением
- •§ 1. Общие понятия
- •§ 2. Особенности теплоотдачи
- •§ 3. Основные понятия
- •§ 4. Некоторые задачи
- •Лекция 13 теплопередача. Сновы расчета теплообменных аппаратов
- •§ 1. Теплопередача через плоскую стенку
- •§ 2. Теплопередача через цилиндрическую стенку
- •§ 3. Интенсификация теплопередачи.
- •§ 4. Теплообменные аппараты
- •Лекция 14 топливо и основы теории процессов горения
- •14. Энергетическое топливо
- •§ 1. Классификация топлива
- •§ 2. Состав топлива
- •3. Общая классификация топлив
- •§ 3. Теплота сгорания топлива.
- •§ 4. Теплотехническая характеристика
- •§ 5. Характеристика отдельных
- •Лекция 15 основы процесса горения топлива
- •§ 1. Сущность процесса горения топлива
- •§ 2. Определение необходимого
- •§ 3. Объем и состав продуктов сгорания
- •§ 4. Энтальпия и теплоемкость
- •4. Численные значения энтальпий составляющих продуктов сгорания и воздуха при различных температурах
Лекция 8 водяной пар
Водяной пар в качестве рабочего тела находит широкое применение в паровых турбинах, являющихся основными тепловыми двигателями на тепловых и атомных электростанциях.
В качестве теплоносителя водяной пар используется: в технологических процессах многих отраслей народного хозяйства, включая и сельскохозяйственное производство; в системах отопления и вентиляции жилых и производственных зданий, обеспечения микроклимата помещений и сооружений защищенного грунта, овоще- и фруктохранилищ, а также в таких технологических процессах, как кормоприготовление, пастеризация, пропаривание грунта и т. д.
§ 1. Основные понятия и определения
V- И Ts-ДИАГРАММЫ ВОДЯНОГО ПАРА
Парообразование может осуществляться путем испарения или кипения.
Испарением называется парообразование, происходящее только с поверхности жидкости. Этот процесс происходит при любой температуре жидкости, причем с повышением температуры интенсивность его возрастает.
Кипением называется процесс бурного парообразования во всем объеме жидкости. Кипение происходит при постоянном давлении ( = const) и соответствующей этому давлению постоянной температуре (tн = const), называемой температурой насыщения или кипения.
Температура кипения (насыщения) tн возрастает с увеличением давления. Зависимость между tн и определяется опытным путем. Для воды, например, хорошее соотношение между ними получается из уравнения Руша:
tн = 100
![]() , (115)
, (115)
где – абсолютное давление, ат.
Все параметры кипящей жидкости принято обозначать соответствующей буквой со штрихом, например: – удельный объем, h – энтальпия, s – энтропия, u – внутренняя энергия, q – теплота.
В процессе кипения жидкости вместе с пузырьками пара выносятся мельчайшие частицы воды. Смесь пара и частиц жидкости называется влажным насыщенным паром.
Если при данном давлении к кипящей жидкости подвести количество теплоты, необходимо для полного превращения в пар всей массы жидкости, то в момент исчезновения последних капель получим сухой насыщенный пар при температуре насыщения tн. Все параметры сухого пара обозначаются теми же буквами, но с двумя штрихами: , h, s, u.
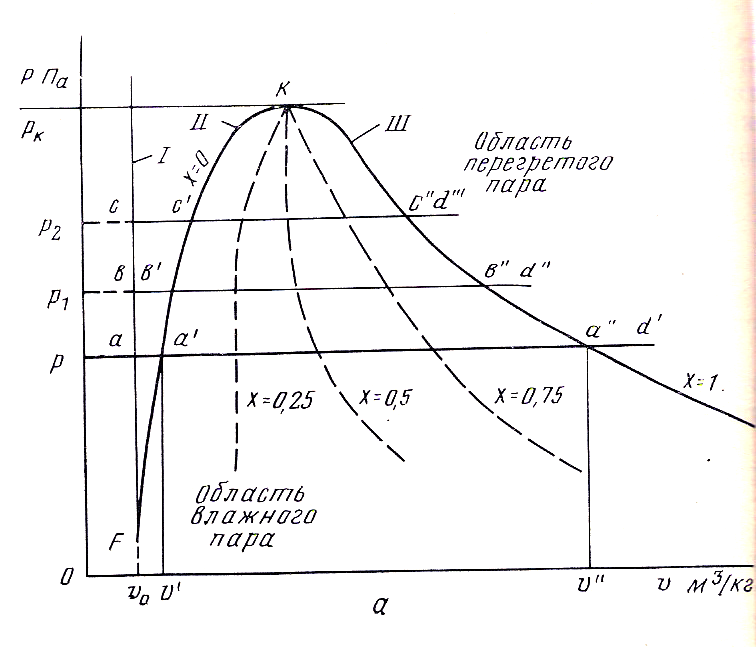
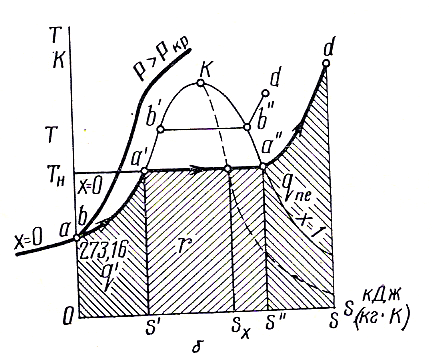
Рис. 20. (а)- и Ts (б)-диаграммы водяного пара: FK – нижняя пограничная кривая; KL – верхняя пограничная кривая.
Сухой насыщенный пар является в парогенераторах неустойчивым, практически мгновенным состоянием при переходе в перегретый пар.
Перегретым паром называется пар, который при одинаковом давлении с сухим насыщенным имеет большую температуру, чем температура насыщения. Получают пар в паровых котлах (парогенераторах) при постоянном давлении. Это давление определяется при конструировании в зависимости от назначения парогенератора.
Рассмотрим процесс преобразования воды в пар в -координатах (рис. 20, а). Пусть при данном давлении 1 кг воды при температуре 0 0С занимает удельный объем 0 (точка а). При подводе теплоты температура воды повышается до тех пор, пока не станет равной температуре насыщения tн, то есть температуре кипения при данном давлении . Удельный объем воды увеличится и достигнет . Состояние кипящей жидкости обозначено на диаграмме точкой a.
При дальнейшем подводе теплоты к кипящей воде она превращается в пар, причем давление и температура смеси воды и пара остаются неизменными, то есть процесс парообразования является изобарно-изотермическим. В тот момент, когда последние частицы кипящей жидкости испаряется, будет получен сухой насыщенный пар. Состояние сухого насыщенного пара отмечено на диаграмме точкой a. Следовательно, на линии aa имеет место смесь кипящей воды и пара – влажный насыщенный пар. Состояние влажного пара в любой точке на линии aa определяется давлением , температурой насыщения tн и степенью сухости х.
Степенью сухости х называется массовая доля сухого пара, содержащегося во влажном паре:
x = mсух/mвл = mсух/mсух + mж , (116)
где mсух, mж – соответственно масса сухого пара и масса жидкости, находящихся в 1 кг смеси.
Для сухого пара х = 1, для кипящей жидкости х = 0. Величина (1 – х) называется степенью влажности пара. Таким образом, влажный насыщенный пар отличается от сухого только степенью сухости: влажный пар имеет степень сухости x < 1, сухой – x =1.
Если к сухому насыщенному пару состояния a продолжать подводить теплоту при том же давлении , то он превращается в перегретый пар. Состояние перегретого пара отмечено точкой d. Перегретый пар отличается от сухого пара тем, что при данном давлении имеет температуру выше температуры насыщения.
При более высоком давлении 1 процесс получения пара происходит аналогично. Однако удельный объем кипящей воды (точка b) будет увеличиваться, поскольку с повышением давления повышается и температура насыщения tн, оказывающая большее влияние на увеличение удельного объема, чем давление – на его уменьшение.
Удельный объем сухого пара (точка b) с повышением давления, наоборот, уменьшается. На диаграмме точка b лежит левее точки a. Если соединить стояние воды и пара при различных давлениях, то на -диаграмме получим линии I, II, III.
Л и н и я I определяет состояние воды при температуре 0 0С и различных давлениях. Вследствие малой сжимаемости воды зависимость 0 от незначительна, и ею, как правило, пренебрегают.
Л и н и я II определяет состояние кипящей жидкости (х = 0) и показывает, что удельный объем с повышением давления увеличивается. Эта линия называется нижней пограничной кривой. Слева от нее – область нагреваемой воды, справа – область влажного пара. При уменьшении давления линии I и II пересекаются в точке F, называемой тройной точкой. Каждое вещество в этой точке находится в трех состояниях: твердом, жидком и газообразном. в тройной точке каждое вещество имеет определенные параметры. Например, для воды температура и давление в тройной точке соответственно равны: tтр = 0,01 0С, тр = 4,6 мм рт. ст.
Л и н и я III характеризует состояние сухого насыщенного пара (х = 1) при различных давлениях и называется верхней пограничной кривой. Справа от нее находится область перегретого пара, слева – влажного насыщенного пара. Из рисунка видно, что удельный объем сухого пара будет тем меньше, чем больше давление.
При повышении давления кривые II и III сходятся в точке К, называемой критической точкой. Эта точка соответствует состоянию, при котором исчезает различие между жидкостью и паром. Анализ показывает, что сконденсировать перегретый пар путем его сжатия по изотерме можно только в том случае, если его температура будет ниже критической. Критическое состояние вещества впервые было установлено Д. И. Менделеевым в 1861 г. Критические параметры для воды имеют следующие значения: кр = 221,15 бар, tкр = 374,12 0С, кр = 0,003147 м3/кг.
При анализе циклов тепловых двигателей (в частности, паротурбинных установок) широко применяется Ts-диаграмма. Для водяного пара Ts-диаграмма представлена на рисунке 20, б. В тройной точке (tтр = 0,01 0С, = 4,6 мм рт. ст.) энтропия условно принята равной нулю. Поэтому линия I (см. рис. 20, а) в Ts-диаграмме превращается в точку на оси ординат на 273,16 К выше абсолютного нуля. Это точка является началом нижней пограничной кривой (х = 0). Изобары нагрева жидкости (a–a, b–b и т. п.) от 0 0С до tтн в Ts-диаграмме являются логарифмическими кривыми, кривизна которых практически совпадает с кривизной нижней пограничной кривой. Следовательно, точки a, b… располагаются на нижней пограничной кривой. Процесс парообразования (a–a, b–b и т. п.) протекает при = const и при tн = const, поэтому изобары парообразования изображаются в Ts-диаграммах горизонтальными линиями; изобары перегрева пара (a–d, b–d и т. п.) – линиями, близкими к логарифмическим. Площади под кривыми процесса обозначают: q – количество теплоты на нагрев при данном давлении 1 кг жидкости от 0 0С до tн; r – удельная теплота парообразования; qпе – теплота, затраченная на перегрев пара при данном давлении до температуры tпе > tн.
§ 2. hs-ДИАГРАММА ВОДЯНОГО ПАРА
В инженерной практике термодинамические процессы с водяным паром рассчитывают с помощью hs-диаграммы. Эта диаграмма в СССР построена до давления 100,0 МПа и до температуры 1000 0С по табличным данным, предложенным проф. М. П. Вукаловичем. Схематично hs-диаграмма показана на рисунке 21. За начало координат принято состояние воды в тройной точке (0 = 611 Па, t0 = 0,01 0С, 0 = 0,001). Откладывая на диаграмме для различных состояний значения s и h для воды при температуре насыщения tн, а также s и h для сухого насыщенного пара, получают нижнюю и верхнюю пограничные кривые.
Изобары в области нагреваемой воды имеют характер логарифмических кривых и проходят близко от нижней пограничной кривой ОК, практически сливаясь с ней.
Изобары в области влажного пара (между верхней и нижней пограничными кривыми) изображаются прямыми наклонными линиями, расходящимися веерообразно вверх; изотермы в области влажного пара, как отмечалось выше, совпадают с изобарами.

Рис. 21. hs-диаграмма водяного пара.
В области перегретого пара изобары – кривые, близкие к логарифмическим. Поскольку в изотермическом процессе энтальпия идеального газа (а сильно перегретый пар по своим свойствам близок к идеальному газу) не изменяется, то изотермы вдали от области насыщения (от верхней пограничной кривой) идут горизонтально. Вблизи от верхней пограничной кривой перегретый пар значительно отклоняется от идеального газа и поэтому изотермы искривляются.
В hs-диаграмме нанесены также линии = const, идущие круче изобар (пунктиром).
Обычно всю диаграмму не выполняют, а строят только ее верхнюю часть, наиболее употребительную в практике расчетов. Это позволяет изображать ее в более крупном масштабе. Основное достоинство hs-диаграммы состоит в том, что данные количества теплоты изображаются в ней отрезками, а не площадями, как в Ts-диаграмме.
