- •13. Дополнительные направления использования хроматографии в промышленности и научных исследованиях.
- •14. Некоторое Резюме для молодежи.
- •2.0. История открытия
- •3.0. Сущность хроматографии
- •4.0 Классификация хроматографических методов
- •5.0 Способы получения хроматограмм
- •6.0 Основные механизмы хроматографического разделения
- •7.0 Хроматограф
- •8.0 Сорбенты для хроматографических разделений
- •9.0 Область применения
- •10. Области возможных исследований:
- •11.Заключение
- •12.Список используемой литературы:
- •13. Дополнительные направления использования хроматографии в промышленности и научных исследованиях.
- •14. Некоторое Резюме для молодежи.
- •15.0 Приложение
6.0 Основные механизмы хроматографического разделения
6.1 Газовая хроматография.
Газовой хроматографией называется хроматографический метод, в котором в качестве подвижной фазы применяется газ или пар. В свою очередь газовая хроматография может быть разделена на газо-адсорбционную (особенность метода газоадсорбционной хроматографии (ГАХ) в том, что в качестве неподвижной фазы применяют адсорбенты с высокой удельной поверхностью (10—1000 м2/ г), и распределение веществ между неподвижной и подвижной фазами определяется процессом адсорбции) (газо-твердую) и газо-жидкостную (в аналитической практике чаще используют метод газожидкостной хроматографии (ГЖХ). Это связано с чрезвычайным разнообразием жидких неподвижных фаз, что облегчает выбор селективной для данного анализа фазы, с линейностью изотермы распределения в более широкой области концентраций, что позволяет работать с большими пробами, и с легкостью получения воспроизводимых по эффективности колонок.) В первом случае неподвижной фазой служит твердое вещество — адсорбент, во втором — жидкость, распределенная тонким слоем по поверхности какого-либо твердого носителя (зерненного материала, стенок колонки).
Газовую хроматографию принято считать, прежде всего, аналитическим методом, что совершенно справедливо с точки зрения далеко идущих возможностей ее применения. Бурное развитие газовой хроматографии в последние годы определяется именно перспективами ее применения, которые и в настоящее время стимулируют ее развитие. Газовая хроматография развивается в двух направлениях, определяемых двумя факторами: с одной стороны, совершенствуется техника метода, т. е. появляются все новые приборы, усовершенствованные детекторы и другое вспомогательное оборудование; с другой стороны, возникающие перед исследователями многочисленные аналитические задачи охватывают все новые области знаний и требуют своего немедленного решения. В настоящее время газовая хроматография позволяет быстро и надежно производить неограниченное число анализов, часто даже таких, осуществление которых другими методами или слишком трудоемко, или просто невозможно. Проблема быстрого контроля производственных процессов, их автоматического регулирования, а также сокращения времени анализа стала настолько острой, что ее решение возможно лишь с помощью хроматографии.
Благодаря большому практическому значению газовой хроматографии становится понятным то, что все проводимые в этой области исследования развиваются главным образом и почти исключительно в двух ука- занных направлениях; значительно меньше внимания уделяется выяснению основных теоретических принципов метода. Исторически жидкостная хроматография развилась раньше газовой. Теория жидкостной хроматографии была в свое время довольно полно и подробно разработана. Когда на первый план выдвинулась газовая хроматография, к ней без особых изменений была применена старая теория. В литературе довольно широко распространено мнение, что эта теория является вполне удовлетворительной и что принципиальные различия в обоих хроматографических методах практически отсутствуют.
6.2 Распределительная жидкостная хроматография.
Распределительная хроматография на колонках по идее близка к газожидкостной хроматографии. На твердый носитель также наносится пленка жидкой, однако через колонку, наполненную таким сорбентом, пропускают не газовую пробу, а жидкий раствор. В связи с этим такой вид хроматографии называют жидкостно-жидкостной или просто распределительной хроматографией.
6.3 Осадочная хроматография.
Разделение вещества в осадочной хроматографии основано на образовании малорастворимых соединений. Успешное разделение смеси достигается многократным повторением процесса образования осадка и его растворения в ходе хроматографирования.
6.4 Молекулярная адсорбционная хроматография
В этом случае разделение веществ осуществляется за счет выборочной (селективной) адсорбции веществ на неподвижной фазе. Такая селективная адсорбция обусловлена сродством того или иного соединения к твердому адсорбенту (неподвижной фазе), а оно, в свою очередь, определяется полярными взаимодействиями их молекул. Поэтому часто хроматографию такого типа используют при анализе соединений, свойства которых определяются числом и типом полярных групп. К адсорбционной хроматографии причисляют ионообменную, жидкостную, бумажную, тонкослойную и газо-адсорбционную хроматографию. Газоадсорбционная хроматография более детально описана в разделе «Элюентный анализ».
Разделение в этом методе основано на различной молекулярной адсорбируемости компонентов смеси. Распределение вещества между сорбентом и раствором характеризуется изотермой адсорбции, показывающей зависимость количества адсорбированного вещества от концентрации при постоянной температуре. В лабораторной практике процесс адсорбционной хроматографии реализуется обычно в двух видах - колоночная хроматография и хроматография в тонком слое (ТСХ).
6.5 Ионообменная хроматография.
Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 3) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе. Она основана на обратимом стехиометрическом обмене ионов, находящихся в растворе, на ионы в ходящие в состав ионообменника.
|
– заряженные функциональные группы, ковалентно связанные с нитями решетки; – свободно перемещающиеся противоположно заряженные противоионы; *- электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами |
Рис. 3. Изображение структуры частицы ионообменной смолы:
6.6 Колоночная хроматография
В этом случае хроматографическое разделение основано на различной степени адсорбции компонентов смеси и сводится к многократному установлению равновесия между твердым неподвижным адсорбентом и перемещающимся по хроматографической колонке раствором разделяемой смеси веществ, при этом разделяемые вещества перемещаются с разной скоростью: те, которые имеют большее сродство к растворителю, перемещаются с большей скоростью, чем те, которые обладают большим сродством к неподвижной фазе. В идеальном случае каждое соединение занимает в колонке отдельную узкую зону. Если компоненты смеси окрашены (например, пигменты, красители), то их разделение можно наблюдать визуально. В дальнейшем осторожно выталкивают столбик адсорбента из колонки и, разрезав его на отдельные зоны, экстрагируют вещества из каждой зоны отдельно. Этот механический способ применяют, редко, чаще продолжают элюирование колонки растворителем или смесью растворителей, при этом более сильно адсорбируемые вещества появляются в элюате позже, чем менее сильно адсорбируемые. Последовательные порции элюированных компонентов собирают в колбы или пробирки равными объемами (фракциями) по 0,5 - 10 мл; растворитель может быть в дальнейшем удален перегонкой, в результате чего получается чистый компонент.
6.7 Метод тонкослойной хроматографии
Тонкослойная хроматография (ТСХ) представляет собой одну из разновидностей адсорбционной хроматографии. Она широко используется в органической химии для идентификации соединений и установления их чистоты, а также иногда в препаративных целях. .
Жидкостная хроматография. В этом случае неподвижной фазой служит жидкость. Наиболее распространенным случаем является адсорбционный вариант жидкостной колоночной хроматографии. Пример разделения природных пигментов представлен на рис.4.
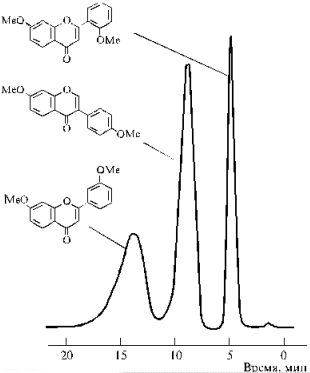
Рис.4. Хроматографическое разделение природных пигментов (флавонов и изофлавонов)
Разделение веществ по методу ТСХ происходит на «открытых» колонках, т.е. в тонком слое адсорбента, нанесенного на стеклянную пластинку. В качестве твердой фазы обычно используется силикагель, оксид алюминия, целлюлоза.
Адсорбент наносят на пластину двумя способами – «сухим» и «мокрым». В первом случае получают хроматографическую пластинку с незакрепленным слоем адсорбента, во втором - с закрепленным. При «сухом» способе адсорбент насыпается на стеклянную пластинку и разравнивается специальным стальным валиком, позволяющим получить однородный ровный по всей площади пластины слой адсорбента толщиной 0,5 -1 мм. При «мокром» способе в адсорбент предварительно добавляют фиксатор (гипс, крахмал и т.п.), На поверхность пластинки наносят сорбционную массу в виде суспензии из сорбента, фиксатора и воды, выравнивают ее на поверхности пластинки. Затем сушат пластинки на воздухе при комнатной температуре при 15 - 20 мин и активируют, нагревая в сушильном шкафу или выдерживая 24 ч на воздухе при 20°С. После сушки слой адсорбента оказывается связанным с поверхностью пластинки, что значительно облегчает работу с ней.
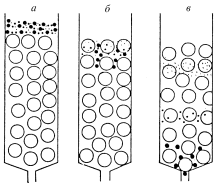
6.8. Гель-фильтрационная, или молекулярно-ситовая, хроматография. Принцип разделения в таких системах несколько иной, чем в предыдущих случаях. Неподвижной фазой являются материалы, обычно гели, со строго контролируемой пористостью, в результате чего одни компоненты смеси в соответствии с размером и формой молекул могут проникать между частицами геля, а другие не могут. Наиболее часто этот вид хроматографии используется для разделения высокомолекулярных соединений. Один из вариантов применения этого метода – определение молекулярных масс разделяемых веществ, часто необходимых для химических исследований (рис.5).
|
|
Рис. 5. Схема разделения методом гель-хроматографии: а – начало разделения, б – разделение, в – конец разделения; большие кружки – частицы геля, большие точки – молекулы соединений с большой молекулярной массой, маленькие точки – молекулы соединений с меньшей молекулярной массой |
6.9. Аффинная хроматография. Этот вид хроматографии основан на взаимодействии между веществом, с одной стороны, способным реагировать с выделяемым соединением, а с другой – связанным с твердым носителем неподвижной фазы. Такое вещество обладает сродством к выделяемому соединению и называется аффинным лигандом. Наиболее часто этот метод находит применение в биохимическом анализе. Конечно, число способов хроматографирования не ограничивается перечисленными выше. Часто хроматографию сочетают с другими физико-химическими методами, например с масс-спектрометрией.
6.10. Основные параметры хроматографического разделения.
Основными параметрами
хроматографического разделения являются
удерживаемый объем и время удерживания
компонента смеси (рис. 6). Время
удерживания
tR
- это время,
прошедшее от момента ввода пробы в
колонку до выхода максимума соответствующего
пика. Умножив время удерживания на
объемную скорость элюента F![]() , получим
удерживаемый объем VR:
, получим
удерживаемый объем VR:
VR = tR . F ;
Исправленное время удерживания - время, прошедшее с момента появления максимума пика несорбируемого компонента до пика соответствующего соединения:
tR' = tR - t0;
Приведенный или исправленный объем удерживания - это объем удерживания с поправкой на мертвый объем колонки V0, т. е. на объем удерживания несорбируемого компонента:
VR' = VR - V0;
Характеристикой удерживания является также коэффициент емкости k', определяемый как отношение массы вещества в неподвижной фазе к массе вещества в подвижной фазе: k' = mн / mп; Величину k' легко определить по хроматограмме:
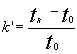
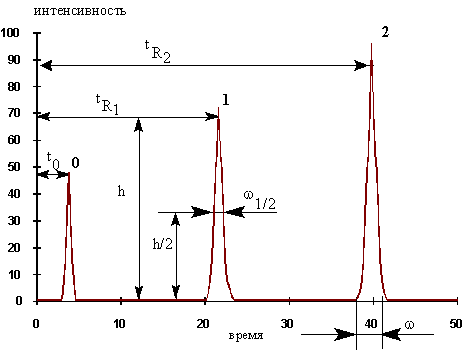
Рис. 6. Количественные характеристики компонентов разделения
Важнейшими параметрами хроматографического разделения являются его эффективность и селективность. Эффективность колонки, измеряемая высотой теоретических тарелок (ВЭТТ) и обратно пропорциональная их числу (N) тем выше, чем уже пик вещества, выходящего при том же времени удерживания.
Значение эффективности может быть вычислено по хроматограмме по следующей формуле:
N = 5.54 . (tR / 1/2)2,
где tR - время удерживания, w 1/2 - ширина пика на половине высоты
Зная число теоретических тарелок, приходящееся на колонку, длину колонки L и средний диаметр зерна сорбента dc, легко получить значения высоты, эквивалентной теоретической тарелке (ВЭТТ), и приведенной высоты (ПВЭТТ):
ВЭТТ = L/N ПВЭТТ = ВЭТТ/dc
Эти характеристики позволяют сравнивать эффективности колонок различных типов, оценивать качество сорбента и качество заполнения колонок.
Селективность
разделения
двух веществ
![]() определяется по уравнению:
определяется по уравнению:
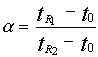 ,
,
При рассмотрении разделения смеси двух компонентов важным параметром служит также степень разделения RS:
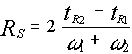 ;
;
Пики считаются разрешенными, если величина RS больше или равна 1.5. Основные хроматографические параметры связывает следующее уравнение для разрешения:
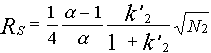 ;
;
Факторами, определяющими селективность разделения, являются: 1) химическая природа сорбента; 2) состав растворителя и его модификаторов; 3) химическая структура и свойства компонентов разделяемой смеси; 4) температура колонки.