
- •Учебное пособие
- •Введение
- •1. Кристаллическое строение металло в
- •2. Кристаллизация металло в и строение металлическо - го слитка
- •3. Фазы в металлических сплавах
- •4. Диаграммы фазового равновесия двойных систем (диаграммы состояния)
- •5. Деформация и разрушение металло в
- •6. Механические свойства металлов
- •7. Влияние нагрева на структуру и свойства деформированного металла
- •8. Д иаграмма состояния железо-углерод (метастабильная д иаграмма)
- •9. Легирующие элементы в сплавах железо-углерод
- •10. Стабильная д иаграмма состояния железо-углерод (графит)
- •11. Чугуны
- •12. Фазовые превращения в сплавах железо-углерод (тео рия термическо й обработки)
- •2. Превращение пер еохл аж д енного ауст енит а
- •1 3. Превращение при непрерывном охлаждении
- •14. Техно ло г ия термическо й обработки металлов и сплавов
- •15. Список литера туры
3. Фазы в металлических сплавах
Сплавы получаются путем с плавления, спекания или одновременного осаждения из газовой фазы отдельных компонентов. Компоненты могут вступать во взаимодействие друг с другом, образуя фазы системы.
СПЛАВЫ
о тс у тс тв ие взаимодействия
компонентов, фазы
так ой системы чистые
компоненты, например
Fe-Pb.
тс у тс тв ие взаимодействия
компонентов, фазы
так ой системы чистые
компоненты, например
Fe-Pb.
взаимодействие компонентов – фаза – новая однородная часть системы, имеющая свой тип кристаллической решетки, состав, свойства и отдельная от других частей систем ы поверхностью раздела.
ФАЗЫ
ж
 идкие
растворы
идкие
растворы
тв ер д ые растворы
промежуточные фазы (химические с оединения)
I
I
т
 енденция
к правильному расположению
атомов на определенном
расстоянии, характерном для данной
Т0
–
ближний порядок.
енденция
к правильному расположению
атомов на определенном
расстоянии, характерном для данной
Т0
–
ближний порядок.
один из компонентов сохраняет свою кристаллическую решетку, а атомы других располагаются в решетке первого, изменяя ее размеры.
Тип кристалли ческой решетки, отличный от ре шетки компонен- то в , в соединении всегда сохраня ется простое кратное соотно шение компонен- то в АmBn, Т0 пла вления постоян на, свойства хи мического со единения резко отличаются от свойств компо нентов.
атомы компонентов В и С в решетке компонента А (растворитель)
16
Т ВЕРДЫЕ
РАСТВОРЫ обозначение - а,
у,
5,
8
и
т.д. микроструктура
не отличается от микроструктуры чистого
компонента.
ВЕРДЫЕ
РАСТВОРЫ обозначение - а,
у,
5,
8
и
т.д. микроструктура
не отличается от микроструктуры чистого
компонента.
З АМЕЩЕНИЯ
– атомы растворенного
компонента заменяют атомы в узлах
решетки растворителя.
АМЕЩЕНИЯ
– атомы растворенного
компонента заменяют атомы в узлах
решетки растворителя.
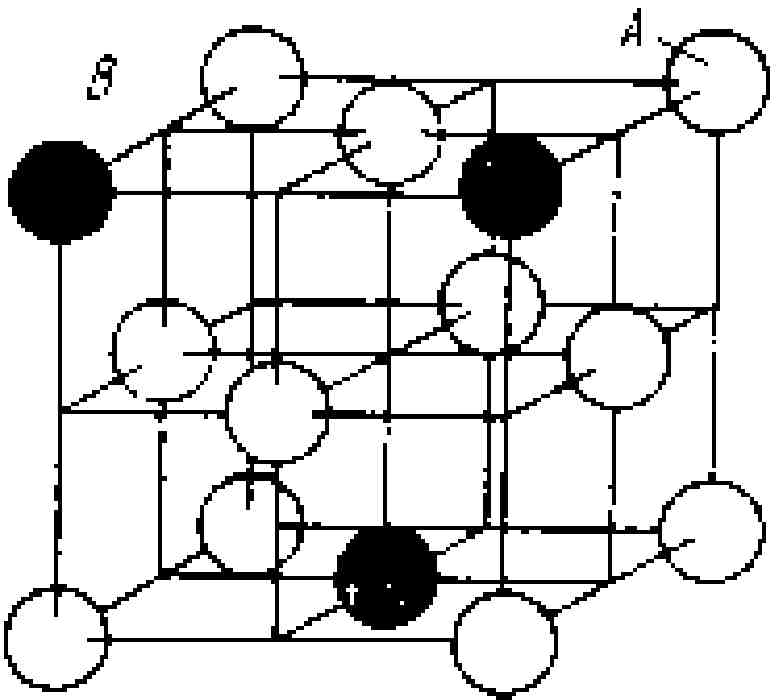
А – атом растворителя; В – атом растворенного компонента.
Твердые растворы замещения – ограниченные и неограниченные.
Неограниченные тв е р д ые растворы образуются при условии:
одинаковый (изоморфный) тип решетки компонентов;
различие атомных радиусов ≤ 8 – 15 %;
близкое расположение в периодической системе. Неограниченно растворяются Сu-Ni, Ag-Au, V-Ti и т.д.
ВНЕД РЕНИЯ – атомы растворенного компонента располагаются в ме-жузлиях (пустотах) кристаллической решетки растворителя.

Твердые растворы внедрения всегда ограниченные. Образуются при условии:
< 0,59;
Rрастворенного(В) Rрастворителя(А)
Чаще всего тв ер дые растворы этого типа образуют переходные металлы Fe, Mn, Co, Ti, Mo, W, V, Zr и др. с металлоидами – С, N, O, H.

17
П ромежуточные
фазы (химические соединения) – состав
может быть
выражен формулой АmBn,
где m и n – простые числа. Промежуточные
фазы, образованные между металлами,
носят название интерметаллиды.
ромежуточные
фазы (химические соединения) – состав
может быть
выражен формулой АmBn,
где m и n – простые числа. Промежуточные
фазы, образованные между металлами,
носят название интерметаллиды.
образуются между компонентами, имеющими большое различие в электронном, кристаллическом строении, а так ж е большее отличие в размерах атомов.
НАИБОЛЕЕ ВАЖНЫЕ РАЗНОВИДНОСТИ ПРОМЕЖУТОЧНЫХ ФАЗ
I
ф
 азы
внедрения
– образуют переходные металлы и
неметаллы с малым
атомным радиусом – С, N,
B, H –
карбиды, нитриды, бориды. Формула:
М4Х
(Fe4N,
Mn4N),
M2X
(W2C,
Fe2N
и др.). Простая кубическая или гексагональная
решетка (отличная от
решетки компонентов). На базе решеток
фаз внедрения образуются тв
е р д ые растворы вычитания.
азы
внедрения
– образуют переходные металлы и
неметаллы с малым
атомным радиусом – С, N,
B, H –
карбиды, нитриды, бориды. Формула:
М4Х
(Fe4N,
Mn4N),
M2X
(W2C,
Fe2N
и др.). Простая кубическая или гексагональная
решетка (отличная от
решетки компонентов). На базе решеток
фаз внедрения образуются тв
е р д ые растворы вычитания.
фазы Лавеса - имеют формулу АВ2 и образуются между компонентами А и В при соотношении атомных диаметров Da/Dв ~ 1,1 – 1,6. Решетка ГПУ. MnZn2, MgNi2 или ГЦК – TiBe2, TiCr2, FeW2, FeMo2 и т.д.
электронные с оединения – имеют определенное соотношение числа валентных электронов к числу атомов в кристаллической ячейке (определенную электронную концентрацию). Образуются между одновалентными (Cu, Ag, Au, Li, Na) или переходными металлами (Fe, Mn, Co и др.) и простыми металлами с валентностью 2-5 (Be, Mg, Zn, Al и др.)
э лектронная
концентрация
3/2 (1,48) – решетка ОЦК, сложная кубическая,
гексагональная, обозначение
β.
CuBe,
CuZn, Cu3A
l и др.
лектронная
концентрация
3/2 (1,48) – решетка ОЦК, сложная кубическая,
гексагональная, обозначение
β.
CuBe,
CuZn, Cu3A
l и др.
электронная концентрация 21/13 (1,62) – сложная решетка, обозначение γ.
Cu5Zn8, Fe5Zn21, Cu5Sn8 и др.
электронная концентрация 7/4 (1,75) ГПУ решетка, обозначение ε. CuZn3, Cu3Si, Cu3Sn и др.
18
ВОПРОСЫ И ЗАДАЧИ ПО ТЕМЕ
Что называется фазой? Какие фазы могут образоваться в металлических сис-те м ах ?
Что та к о е тв е р д ый раствор, какие типы тв е р д ых растворов вы знаете?
Что представляет из себя микроструктура тв ер д о г о раствора?
Условия образования неограниченных тв е р д ых растворов. Во з м о ж н а ли неограниченная растворимость углерода и азота в железе?
Приведите примеры химических соединений металла с металлом. Как они называются?
Приведите примеры химических соединений металла и неметалла, их названия.
Что та к о е электронное соединение?
Какие компоненты образуют фазы внедрения?
Задача № 1
Неограниченно растворяются друг в друге Cu и Ni. Объясните, приведите причины, которые определяют подобное взаимодействие компонентов.
Задача № 2
По ч е м у никель неограниченно растворяется в железе модификации γ и ограниченно в железе модификации α?
Задача № 3
Какие соединения могут образовать между собой медь и цинк, медь и алюминий, железо и азот, железо и водород?
19
