
- •Лабораторна робота № 1 виробництво чавуну
- •Обладнання, матеріали та інструменти
- •Теоретичні відомості
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 2 теоретичні основи виробництва сталі
- •Теоретичні відомості
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 3 виробництво міді
- •Теоретичні відомості
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 6 основи технології порошкової металургії
- •Теоретичні відомості
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 7
- •Композитні матеріали та аморфні метали і сплави
- •Мета: 1. Вивчити теоретичні основи одержання виливок різними способами.
- •Теоретичні відомості
- •Лабораторна робота № 8
- •Основи технології деревообробки
- •Мета: 1. Вивчити теоретичні основи технології отримання конструкційних матеріалів і виробів із деревини.
- •Теоретичні відомості
- •Виробництво фанери
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 9 основи технології виробництва полімерів і пластмас
- •Теоретичні відомості
- •Методи синтезу полімерів
- •Пластичні маси і виробництво виробів з них
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Лабораторна робота № 10 каучуки і гума, виробництво виробів з гуми
- •4.2. Класифікація та властивості гум
- •4.3. Особливості технологи виробництва гумових виробів
- •5. Фактори підвищення ефективності виробництва і використання полімерів, каучуків і виробів з них
- •Лабораторна робота № 11 скло, його склад, застосування. Технологія виготовлення
- •28.1. Загальні відомості
- •28.2. Коротка характеристика сировини необхідної для одержання скла
- •28.3. Приготування скломаси і способи виробництва скловиробів
- •28.4. Вироби із скла, їх застосування
- •Контрольні запитання
- •Лабораторна робота № 24
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Особливості техніки безпеки
- •Контрольні запитання
- •Тема 11. Обробка металів тиском
- •2. Технологічний процес виготовлення заготовок прокаткою
- •3. Технологічний процес виготовлення заготовок пресуванням
- •4. Волочіння як технологічний спосіб отримання дроту, прутків та труб
- •5. Технологічний процес кування
- •6. Технологічний процес штампування. Види штампування
- •Контрольні запитання
- •Практика зварювання
- •Особливості техніки безпеки
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Програма підготовки до виконання роботи
- •Список літературних джерел
- •Завдання й методичні вказівки
- •Контрольні запитання
- •Особливості техніки безпеки
- •Програма підготовки до виконання роботи
- •Завдання й методичні вказівки
- •Контрольні запитання
ЛАБОРАТОРНИЙ ПРАКТИКУМ
З ТЕХНОЛОГІЇ
ВИРОБНИЦТВА
КОНСТРУКЦІЙНИХ МАТЕРІАЛІВ
ВІННИЦЯ - 2011
УДК 621.7+620.22+621.74
ББК 34.5я73+30.3-3я73
А 92
Рецензенти:
Петрук В.Г., доктор технічних наук, професор – Вінницький національний технічний університет
Матвійчук А.Я., кандидат педагогічних наук, професор – Вінницький державний педагогічний університет імені Михайла Коцюбинського
В.В. Атаманюк
Лабораторний практикум з технології виробництва конструкційних матеріалів: Навчально-методичний посібник для вищих навчальних закладів. – Вінниця: ВДПУ, 2011. – ? с.
Наведено теоретичні відомості і методичні рекомендації щодо виконання лабораторних робіт з основних методів виробництва як металевих так і неметалевих конструкційних матеріалів. Тут же розглядаються технології виробництва машин та устаткування (ливарним способом, обробка тиском, зварюванням, паянням).
Призначений для студентів вищих педагогічних навчальних закладів. Може бути корисний для студентів технічних ВНЗ, учнів ПТНЗ, технічних коледжів і ліцеїв.
Іл. 76. Табл. 30. Бібліогр. 8 назв.
© Атаманюк В.В. 2011
ISBN 966-527-165-2
З М І С Т
Вступ ……………………………………………………………………………………………. |
4 |
|
Лабораторна робота № 1 |
Виробництво чавуну ………………………………….. |
|
Лабораторна робота № 2 |
Теоретичні основи виробництва сталі …………… |
|
Лабораторна робота № 3 |
Виробництво міді ………………… |
|
Лабораторна робота № 4 |
Виробництво алюмінію |
|
Лабораторна робота № 5 |
Виробництво титану |
|
Лабораторна робота № 6 |
Виробництво свинцю |
|
Лабораторна робота № 7 |
Основи технології порошкової металургії |
|
Лабораторна робота № 8 |
|
|
Лабораторна робота № 9 |
|
|
Лабораторна робота № 10 |
|
|
Лабораторна робота № 11 |
|
|
Лабораторна робота № 12 |
|
|
Лабораторна робота № 13 |
|
|
Лабораторна робота № 14 |
|
|
Лабораторна робота № 15 |
|
|
Лабораторна робота № 16 |
|
|
Лабораторна робота № 17 |
|
|
Лабораторна робота № 18 |
|
|
Лабораторна робота № 19 |
|
|
Лабораторна робота № 20 |
|
|
Лабораторна робота № 21 |
|
|
Лабораторна робота № 22 |
|
|
Лабораторна робота № 23 |
|
|
Лабораторна робота № 24 |
Ливарне виробництво ………………………………… |
|
Лабораторна робота № 25 |
Ручне електродугове зварювання сталей ……….. |
|
Лабораторна робота № 26 |
Точкове електроконтактне зварювання сталей ... |
|
Лабораторна робота № 27 |
Паяння та лудіння металів ………………………….. |
|
ДОДАТКИ ………………………………………………………………………………………. |
|
|
В С Т У П
Мета лабораторного практикуму – закріпити і поглибити теоретичні знання; розвинути вміння застосовувати теоретичні знання для розв’язання конкретних практичних завдань, здатність аналізувати результати експерименту, зіставляти їх з теоретичними положеннями і розрахунками; набути практичні навички для самостійного проведення різних методів контролю, дослідження структури та властивостей металів і сплавів, а також вивчити будову і принцип дії необхідних для цього пристосувань, інструментів та лабораторного обладнання; ознайомитися з технологією проведення основних операцій термічної та хіміко-термічної обробки металів і сплавів; ознайомитися з технологією основних видів ливарного виробництва, а також паяння, лудіння і зварювання металів і сплавів.
Навчальний час, що відводиться для виконання кожної лабораторної роботи, буде використаний з максимальною ефективністю лише за умови проведення попередньої високоорганізованої і якісної самостійної роботи студентів.
Порядок підготовки до виконання лабораторної роботи такий:
- уточнити і записати в зошит тему роботи, її мету, прилади, обладнання і матеріали, програму підготовки до виконання роботи, контрольні запитання та літературу;
- вивчити теоретичний матеріал до лабораторної роботи згідно з вказаними літературними джерелами. Якщо ж виявиться, що їх недостатньо, ознайомитись і з додатковими;
- виконати в письмовій формі контрольні завдання, зазначені в розділі “Програма підготовки до виконання роботи”. Відповіді повинні бути короткі, чіткі, але досить точно і повно розкривати суть питання.
Звіт про виконану роботу необхідно підготувати до наступного заняття в лабораторії і наданий для перегляду викладачу перед початком занять.
В лабораторії студентам необхідно дотримуватися таких правили техніки безпеки:
- приступати до виконання лабораторної роботи можна тільки з дозволу викладача, після проведеного ним інструктажу з техніки безпеки;
- на занятті студент виконує тільки ту роботу, що зазначена викладачем;
- перехід на інше робоче місце, без дозволу викладача, не допускається;
- включення й вимикання лабораторного устаткування проводиться тільки викладачем, навчальним лаборантом або з їхнього дозволу студентами;
- при виконанні лабораторної роботи необхідно бути гранично уважним, зосередженим, не проявляти поспіху, неуважності;
- працювати в лабораторії у відсутності викладача або лаборанта, а також у невстановлений час без дозволу викладача – забороняється;
- категорично забороняється студентам виконувати в навчальній лабораторії експериментальні роботи, не пов'язані з навчальним лабораторним практикумом, під час відсутності викладача.
Лабораторна робота № 1 виробництво чавуну
Мета: Вивчити основні види залізних руд, металургійного палива, флюсів і вогнетривких матеріалів; технологію виробництва чавуну в доменній печі; основну продукцію доменного виробництва.
Обладнання, матеріали та інструменти
Зразки залізних руд (магнетиту, гепатиту, лімоніту, сидериту), коксу, вапняку, вогнетривких матеріалів (динасу, шамоту, магнезиту, графіту, вугілля), чавунів, феросплавів і шлаку.
Теоретичні відомості
На виробництві і в техніці, як правило, використовуються не чисті метали, а сплави, що обумовлено більш високою конструкційною міцністю сплавів, наявністю в них таких специфічних властивостей, або їх комплексу, які не зустрічаються у чистих металів. Крім того окремі властивості металевих сплавів можна додатково поліпшувати, використовуючи відповідну термічну чи хіміко-термічну обробки. Кількість сплавів у сучасній техніці невпинно зростає, що розкриває нові можливості у створенні високоефективного промислового обладнання. Досить нагадати, що лише на основі заліза створено більше як 10 тисяч сплавів.
Метали поділяють на дві групи – чорні й кольорові. До чорних металів належать залізо і сплави на його основі – сталі та чавуни. Ці сплави займають важливе місце в машинобудівній промисловості завдяки порівняно невисокій вартості, добрим експлуатаційним і механічним властивостям. Недоліками чорних металів є велика густина та низька корозійна тривкість. З огляду на це в розвинутих державах світу спостерігається стійка тенденція до широкого використання металевих сплавів на основі титану, алюмінію та магнію.
Спочатку залізо добували безпосередньо із руди відновленням у горнах. Із збільшенням висоти горнів залізо насичувалось вуглецем, від чого виплавлений сплав ставав крихким, але з добрими ливарними властивостями. Такий сплав дістав назву чавуну. З XIII ст. чавун почали переробляти на сталь – сплав з меншим, ніж у чавуні, вмістом вуглецю, силіцію, марганцю та деяких інших елементів, а тому з більшою пластичністю та міцністю. Продукцією чорної металургії є чавуни, феросплави (сплави заліза з підвищеним вмістом інших елементів) та стальні зливки для виготовлення сортового прокату і великих деталей машин.
Кольоровими вважають всі інші метали, крім чорних. Для технічних потреб застосовують близько 70 кольорових металів. Серед них найбільше значення мають алюміній, мідь, магній, титан, нікель, свинець, цинк, олово, молібден, вольфрам, кобальт, тантал, цирконій, ніобій. Мідь і алюміній у чистому вигляді використовують для потреб електротехніки та теплотехніки. Здебільшого кольорові метали застосовують у вигляді сплавів. Багато кольорових металів слугують легувальними елементами для сплавів.
Виробництво кольорових металів характеризується великою різноманітністю технологічних процесів виплавки і визначається особливостями складу їхніх руд. Продукцією кольорової металургії є чисті метали та їхні сплави, а також зливки для виготовлення сортового прокату.
Матеріали для виробництва металів. Для виробництва металів використовують руди, флюси, паливо, вогнетривкі матеріали. У природних умовах майже всі метали, крім платини, золота, срібла і самородної міді, перебувають у сполуках з іншими елементами.
Рудою називають гірські породи, які містять у собі метали в кількості, що забезпечує їх економічно доцільну переробку. Залізні руди, наприклад, містять 30...60 % металу. Вміст кольорових металів у рудах не більше 5 %, а інших – долі процента (молібдену, наприклад, до 0,02 %).
Руда складається з мінералів, в яких метал перебуває у вигляді оксидів, сульфідів, карбонатів та пустої породи (в основному пісковику Sі02, глинозему Аl2О3, рідше вапняку СаСО3 і доломіту СаСО3 · МgСО3 з домішками сірки, фосфору, миш'яку тощо). Шкідливі домішки – це фосфор, сірка, миш’як. У рудах, наприклад, залізних, можуть бути також корисні домішки: марганець, хром, нікель, ванадій, вольфрам, молібден.
Флюсом називається матеріал, що утворює при виплавці шлак - легкоплавку сполуку з пустою породою руди, золою палива та іншими неметалевими вкрапленнями. Водночас флюси можуть знижувати кількість шкідливих домішок у металі. Густина шлаку менша від густини металу, в зв’язку з чим шлак випливає над ним і його можна зливати в процесі плавлення.
При виплавці чорних і деяких кольорових металів флюсами можуть бути кварцовий пісок, що складається в основному з SіО2, вапняк СаСО3 та інші сполуки кальцію і магнію.
Паливом називають речовини, у процесі згорання (або поділу чи з’єднання ядер) яких виділяється значна кількість теплоти. За походженням паливо поділяють на природне і штучне. До природного палива належать, наприклад, дрова, торф, вугілля, горючі сланці тощо. Штучне паливо отримують, переробленням природного палива. Так, у процесі нагрівання викопного вугілля до високої температури без доступу повітря отримують кокс, з нафти вилучають мазут тощо.
Властивості палива залежать в основному від його хімічного складу. Основним елементом більшості видів палива є вуглець. У різних видах палива вміст вуглецю різний – від 30 до 95 %. До складу палива входять також водень, кисень, азот, сірка, попіл та інші речовини.
Цінність палива визначається кількістю теплоти, яка виділяється в разі повного його згорання. Так, у процесі спалювання 1 кг дров виділяється 10,2 МДж/кг теплоти, кам’яного вугілля – 22 МДж/кг, бензину - 44 МДж/кг. Чим більше вуглецю та водню міститься в паливі, тим більше теплоти виділяється у процесі його згоряння.
Під час спалювання палива утворюються тверді та газові речовини. Тверді – це попіл, сажа, шлак. Газові – оксиди вуглецю, сірки й сірки тощо. Газові і частково тверді продукти згорання палива через димарі викидаються в атмосферу. Щорічно в атмосферу викидаються сотні мільйонів тон різних шкідливих речовин. Для захисту навколишнього середовища від забруднення речовинами, які утворюються в процесі згорання палива використовують різні фільтри та пристрої, які очищають або знешкоджують шкідливі викиди. Перспективним видом палива, яке не забруднює навколишнє середовище, добре зберігається та транспортується, є водень. В процесі згорання водню виділяється водяна пара.
Паливо, що використовується в металургії, є не тільки джерелом тепла, але може брати участь і в хімічних реакціях. До його складу входять горючі речовини (вуглець, водень), негорючі речовини (попіл, вода, азот) і шкідливі залишки (сірка, фосфор). Попіл – мінеральна складова палива, що містить оксиди SіО2, Аl2О3, СаО, МgО та ін. У високоякісному паливі негорючих речовин та шкідливих домішок дуже мало. Металургійна промисловість використовує тверде, рідке і газоподібне паливо. Найпоширенішим є тверде паливо – кокс.
Вогнетривкі матеріали застосовують для внутрішнього облицювання (футерівки) плавильних печей та іншого обладнання, яке знаходиться під дією високих температур і розплавленого металу та шлаку. За хімічним складом вогнетривкі матеріали поділяють на кислі, основні та нейтральні.
До кислих належать динасова цегла, кварцовий порошок та інші матеріали з високим вмістом кремнезему SіО2; до основних - доломітові, магнезитові та інші матеріали з великим вмістом основних оксидів: МgО, СаО; до нейтральних - матеріали, які складаються з оксидів Аl2О3, Сr2О3, Мgo (шамот, хромомагнезит), а також вуглецева цегла.
Способи добування металів із руд. Добувають метали такими способами: пірометалургійним, електрометалургійним, гідрометалургійним, хіміко-металургійним.
Для виробництва металів із руд пірометалургійним способом потрібна значна кількість тепла, що отримується від згоряння палива, через перетворення електричної енергії в теплову, а також від екзотермічних реакцій в металургійних печах. Цей спосіб поки що є головним для виробництва заліза і його сплавів, міді та інших металів.
Електрометалургійний спосіб добування металів здійснюється в дугових, індукційних та інших електричних печах або електролізом із розплавів і водяних розчинів хімічних сполук (наприклад, добування алюмінію із глинозему Аl2О3).
Гідрометалургійний спосіб полягає у вилуговуванні металів із руд різними розчинниками і подальшому їхньому виділенні з розчину. Вилуговування може здійснюватись як на поверхні землі, так і під землею за допомогою свердловин. Цей спосіб широко застосовується, наприклад, для добування міді, а останнім часом – урану і деяких інших металів.
Хіміко-металургійний спосіб об’єднує хімічні та пірометалургійні процеси. Титан, наприклад, одержують відновленням тетрахлориду ТіСl4 магнієм і подальшою плавкою в електродугових печах.
Поряд з розглянутими способами для одержання конструкційних матеріалів на основі металів або їх сполук, а також готових виробів з них останнім часом широко застосовують спосіб порошкової металургії.
Вихідні матеріали для виробництва чавуну. У техніці, сільському господарстві і в побуті особливе значення мають чорні метали, які є сплавами заліза з невеликою кількістю вуглецю та інших елементів. Залежно від концентрації вуглецю чорні метали ділять на три групи: технічне залізо або армко-залізо до 0,02% С, сталі 0,2 - 2,14% С і чавуни більше 2,14% С.
Сучасне виробництво чорних металів проходить так: із природних матеріалів у доменній печі одержують чавун, який потім переробляють у сталь. Вихідними матеріалами для виробництва чавуну є залізні руди, флюси і паливо.
Руда це гірська порода, що містить метал у такій кількості і в такому стані, що за існуючого рівня техніки її економічно доцільно добувати і переробляти. Залізні руди містять залізо у вигляді оксидів, гідратів оксидів, карбонатів, які змішані з пустою породою.
Пустою породою називається природна мінеральна сполука, яка не містить заліза, наприклад кремнезем (SіO2), глинозем (Al2O3) та ін. Можливість використання залізної руди для доменної плавки визначається вмістом у ній заліза, складом пустої породи і концентрацією таких шкідливих домішок, як сірка, фосфор та ін. Важливу роль, крім цього, відіграє швидкість відновлення заліза із руди (яка залежить від природи оксиду заліза, густини і пористості руди). Найбільш важливі типи залізних руд наведені в табл. 1.1.
Таблиця 1.1.Типи найважливіших залізних руд
№ п/п |
Назва руди |
Хімічна формула |
Вміст заліза у відсотках |
Вміст пустої породи у відсотках |
|
|
Магнітний залізняк (магнетит) |
Fe3O4 |
50 - 69 |
31- 50 |
|
|
Червоний залізняк (гепатит) |
Fe2O3 |
55 - 65 |
35 -45 |
|
|
Бурий залізняк (лімоніт) |
2Fe2O3•3Н2O |
35 - 55 |
45 - 65 |
|
|
Шпатовий залізняк (сидерит) |
FeСO3 |
30 - 40 |
60 - 70 |
Щоб звільнити сполуки заліза від кисню, необхідно подіяти на його оксиди іншим елементом – відновником, тобто таким елементом у якого здатність до хімічної реакції з киснем більша, ніж у заліза. Відновником заліза з його оксидів у рудах є вуглець, який використовується у вигляді різноманітного палива. Поряд з відновленням заліза, при згорянні палива виділяється тепло, необхідне для прискорення інших реакцій в доменних печах, а також для розплавлення перероблюваних матеріалів. Паливо повинно мати високу теплотворну здатність, достатню міцність, щоб не кришитися і не перетворюватися в дріб’язок, мати найменшу кількість шкідливих домішок, таких, наприклад, як сірка і фосфор, містити незначну кількість золи (зола це нелетка мінеральна сполука, що залишається після згоряння будь-якого палива). Цим вимогам у значній мірі відповідають кокс і деревне вугілля.
Основним видом палива при виплавці чавуну є кокс. Теплотворна здатність коксу 3,03•107 Дж/кг. Він чинить значний опір стискуванню. Недоліком його є високий вміст у ньому сірки (0,5-0,2%) і золи (9 -12%).
Найбільш досконалим видом палива є деревне вугілля. Вміст золи в ньому біля 0,8...1,0 %, а сірка і фосфор практично відсутні. Теплотворна здатність його 2,97•107 Дж/кг. Недолік деревного вугілля – мала міцність, що обмежує висоту доменних печей. Тому деревне вугілля застосовують лише у доменних печах невеликого об’єму (200...300 м3) при виплавці високоякісного чавуну.
Пуста порода руди, а також зола палива плавляться при дуже високій температурі (1800С і більше), і розплавлення їх в доменних печах не можливе; нагромаджуючись з часом усередині печі, вони можуть порушити її нормальну роботу, якщо їх не видаляти. Для цього в піч вводять речовини, які при порівняно низьких температурах утворюють з пустою породою руди і золою палива легкоплавкі хімічні сполуки. Такі речовини називають флюсами. Сплавляючись з пустою породою, флюси утворюють шлаки. Оксиди, що містяться в залізній руді, діляться на основні (FeO, MnO, CaO, MgO), кислотні (SіO2, Р2О5) і амфотерні (Al2O3). Основні і кислотні оксиди при високих температурах утворюють легкоплавкі сполуки. Так, температура плавлення SіO2 1750C, CaO 2100C, а температура плавлення хімічної сполуки, утвореної з них, (CaO•SіO2 ) 1350C. У зв’язку з цим, якщо в пустій породі руда містить SіO2, до неї додають вапняк СаО, а якщо пустою породою є СаО флюсом повинен бути пісок SіO2. Залізні руди, що добуваються в Україні, мають переважно кислу пусту породу, і тому флюсами служать вапняки.
Чавун виплавляють при високих температурах. Тому велике значення мають вогнетривкі матеріали, що використовуються для будівництва доменних та інших металургійних печей, особливо тих їх частин, які безпосередньо взаємодіють з розплавленим металом і шлаком. На практиці вогнетривкі матеріали використовують у вигляді цегли, фасонних виробів і порошків для кладки печей, ковшів і т.д. Такі матеріали не повинні руйнуватися і розм’якшуватися при високих температурах, щоб витримувати навантаження від закладених у піч інших матеріалів, а також зберігати об’єм при нагріві і витримувати різкі зміни температури.
Залежно від хімічного складу розрізняють кислі вогнетривкі матеріали, основні і нейтральні. До кислих належать динасова цегла, кварцовий пісок та інші матеріали з високим вмістом кремнезему SiO2; до основних доломітові, магнезитові та інші матеріали з великим вмістом основних оксидів: MgO, CaO; до нейтральних матеріали, які складаються з окислів Al2O3, Cr2O3, MgO (шамот, хромомагнезит), а також вуглецеві матеріали, які витримують температуру до 2050С. До їх складу входить біля 90% вуглецю. З них виготовляють вугільні і графітові електроди для дугових печей, тиглі для плавки металів, деталі розливних ковшів і т.п.
Конструкція і принцип роботи доменної печі. Руда перед тим як поступити в доменну піч піддається попередній підготовці на місцях добування, що необхідно для підвищення продуктивності доменної печі, зменшення витрат коксу і поліпшення якості чавуну. Підготовка руди полягає в її подрібненні, класифікації, збагачені (усуненні пустої породи), спіканні (агломерації) дріб’язку, усередненні хімічного складу і сортуванні за розмірами з метою надання руді однорідності за хімічним складом і фізичними властивостями.
Виплавляють чавун в доменних печах. Суть процесу отримання чавуну в них полягає у відновленні оксидів заліза, що входять до складу руди, оксидом вуглецю, воднем і твердим вуглецем та навуглецюванні відновленого заліза.
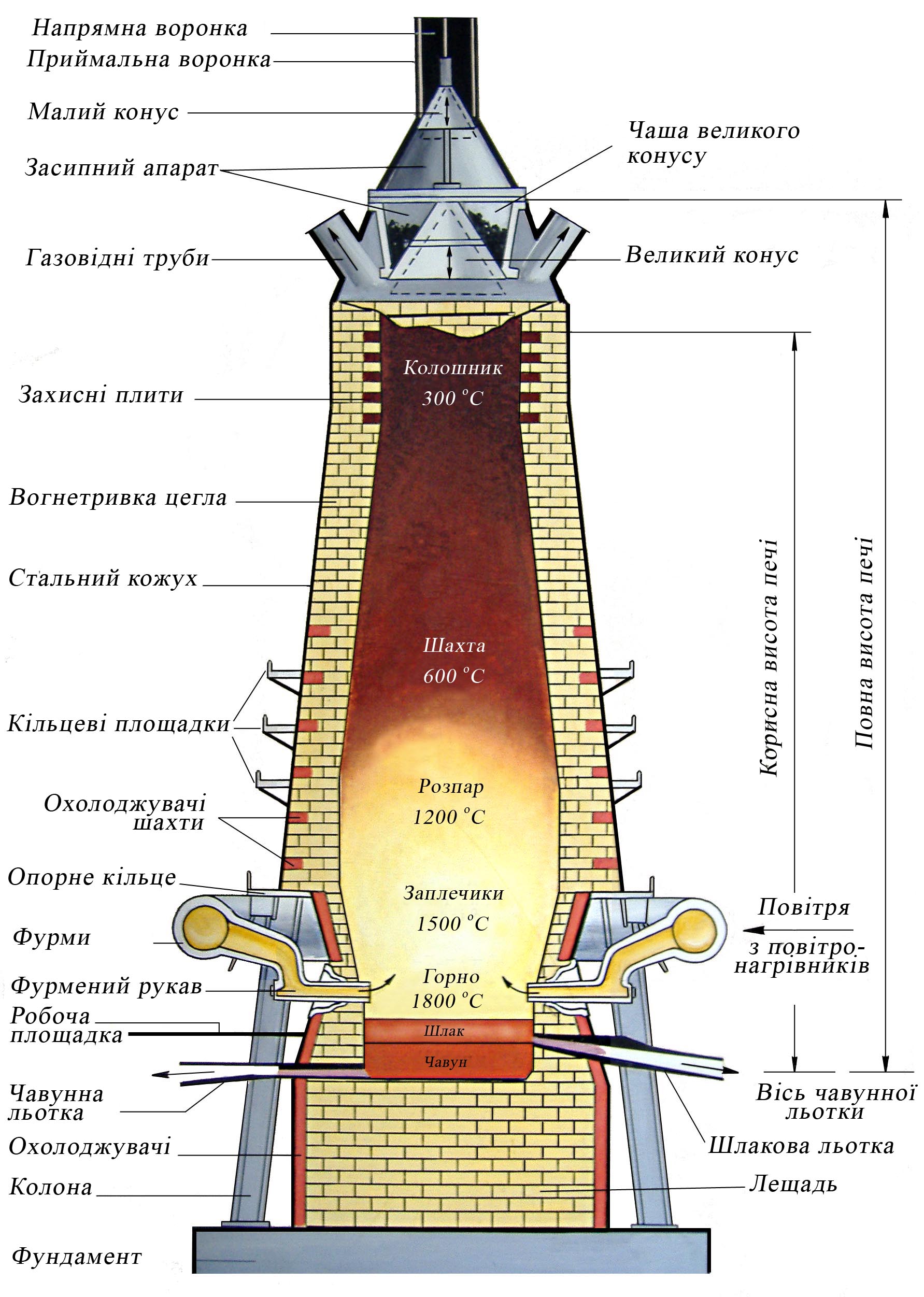
Рис. 8.1. Будова доменної печі
Доменна піч є вертикальним агрегатом шахтного типу (рис. 8.1). Зовні вона замкнута в стальний кожух, а всередині футерована (викладена) вогнетривкою цеглою. Внутрішні обриси робочого простору називаються профілем доменної печі, який залежно від геометричної конфігурації і технологічного призначення ділиться на 5 частин: колошник, шахта, розпар, заплечики, горн.
Колошник, який розташований у верхній частині печі, призначений для прийому шихтових матеріалів і відведення газів. У шахті, яка має форму зрізаного конуса, що розширюється донизу, розміщується основна маса шихти. Така форма шахти забезпечує опускання шихти в міру її плавлення в нижню частину печі і рівномірний розподіл газів у її поперечному перерізі. Найбільш широка частина печі, що має форму циліндра, називається розпаром, а нижня частина печі (також має форму циліндра) горном. Простір між розпаром і горном, у вигляді зрізаного конуса, оберненого більшою основою вверх, заплечиками. Завдяки такій формі заплечики підпирають і втримують всю шихту доменної печі, не дають їй опуститися в горн. Описана конфігурація робочого простору створює сприятливі умови для протікання необхідних аеродинамічних і фізико-хімічних процесів.
Доменна піч працює за принципом протипотоку: шихтові матеріали рухаються зверху вниз, а назустріч їм піднімається потік гарячих газів продуктів згоряння палива. При цьому горить паливо, відновлюється і насичується залізо вуглецем, відновлюються інші елементи, утворюється шлак.
Задування доменної печі. Доменна піч, збудована або капітально відремонтована, старанно просушується протягом 5…6 діб для усунення вологи з вогнетривкої кладки. Після цього починається завантаження печі шихтою найкращої якості (більш міцний малосірчистий кокс, шматки руди). Насамперед проводиться завантаження горна через відкриті фурмені отвори – на під кладеться певна кількість коксу, а потім горно до рівня фурм заповнюється дровами. Подальше завантаження ведеться через колошник – завантажують кокс, потім кокс з вапняком, а потім кокс з вапняком і невеликою кількістю руди. Кількість коксу в шихті повинна бути в 2,5…4 рази більша, ніж при нормальній роботі печі.
Подача дуття починається після повного завантаження печі. Запалюють дрова і кокс при гарячому дутті (не нижче 600°С).
Випускають перший чавун звичайно не пізніше ніж через 24 години після задування, а перший шлак – через 16…20 годин. Задута піч досягає своєї нормальної продуктивності на 10…15 добу після задування.
Доменний процес. Шихтові матеріали в доменній печі поступово пересуваються вниз і, зустрічаючись з газовим потоком при різних температурах, зазнають відповідних змін у складі і властивостях. При русі матеріалів у напрямку від колошника до горна відбуваються такі процеси:
а) сушіння матеріалу;
б) розклад плавильних матеріалів;
в) відновлення заліза та інших елементів з оксидів;
г) навуглецювання відновленого заліза і утворення чавуну;
д) утворення шлаків;
є) горіння вуглецю біля фурм.
Гаряче повітря, що вдувається в доменну піч крізь фурмені отвори, зустрічається з розжареним коксом, через що починається горіння коксу за реакцією:
С + О2 СО2
При цьому виділяється велика кількість тепла і температура біля фурм підвищується до 1700…1800С.
Взаємодія вуглекислого газу з розжареним коксом приводить до утворення оксиду вуглецю СО за реакцією:
СО2 + С 2СО.
Оксид вуглецю є енергійним відновником, здатним не тільки з’єднуватися з вільним киснем, але й відбирати кисень у твердих оксидів заліза та інших елементів.
Розклад плавильних матеріалів. Продукти згоряння палива, піднімаючись вгору назустріч шихті, що опускається, безперервно нагрівають її. Завдяки цьому в різних зонах печі встановлюються різні температури.
У верхній частині печі при порівняно невисокій температурі (100…350С) відбувається просушування і розклад завантажених шихтових матеріалів (виділення хімічно зв’язаної води, летких речовин з палива, розклад вуглекислих солей і т.д.).
Відновлення заліза з оксидів є основною метою доменного процесу, воно відбувається при температурах від 600°С і вище.
У залізних рудах залізо знаходиться у вигляді оксидів Fe2O3, Fe3O4, FeO. Найлегше відновлюється залізо з оксиду Fe2O3, важче - з Fe3O4 і FeO.
Відновлення заліза з оксидів відбувається в такій послідовності:
Fe2O3 Fe3O4 FeO Fe .
Основними відновниками у процесі доменного плавлення є оксид вуглецю (СО) і твердий вуглець (С).
Усунення кисню за допомогою СО називається побічним (непрямим) відновленням і відбувається при температурі вище 570°С за реакціями:
3Fe2O3 + CO 2Fe3O4 + CO2 + 37,137 кДж
Fe3O4 + CO 3 FeO + CO2 +17,166 кДж
FeO + CO Fe + CO2 + 13,607 кДж
Зв’язування кисню твердим вуглецем називається прямим відновленням. Для закису заліза цей процес може бути виражений формулою:
FeO + C Fe + CO – 152,190 кДж
Реакції прямого відновлення заліза відбуваються у доменній печі при температурах 950…1000C.
Відновлення оксидів заліза воднем у доменній печі здійснюється в тій же послідовності, що й відновлення оксидом вуглецю, але має менше значення.
Швидкість відновлення заліза залежить не лише від концентрації його сполук, але й температури і підпорядкованості принципу Ле-Шательє, згідно з яким хімічні реакції, що виділяють тепло, йдуть інтенсивніше при низьких температурах, а реакції, що вбирають тепло – при високих температурах. Тому у верхній частині печі, де температура невисока, інтенсивніше йдуть екзотермічні реакції (з виділенням теплоти) непрямого відновлення, а в нижній частині печі при високих температурах – реакція прямого відновлення заліза.
Марганець відновлюється за такими реакціями:
2MnO2 + CO Mn2O3 + CO2 + 425,379 кДж
3Mn2O3 + CO 2Mn3O4 + CO2 + 170,235 кДж
Mn3O4 + CO → 3MnO+CO2+ 51,916 кДж
MnO + C Mn + CO2 - 287,382 кДж
Відновлення кремнію вуглецем починається при 1050С:
SiO2 + 2C Si + 2CO – 635,096 кДж
Частина сірки (10…20 %) виходить з газами переважно як SO2 i H2S. Решта сірки переходить у чавун і шлак. Під час виготовлення переробного чавуну практично весь фосфор шихти залишається у чавуні. Отже, в горні збирається складний сплав – чавун, до якого входять Fe (основна маса), С (2,14 %), Mn, Si, P, S та інші елементи.
Таким чином, залізна руда при своєму русі до горна печі поступово відновлюється; кількість відновленого заліза на рівні розпару становить вже близько 80 %.
У шихтових матеріалах доменної печі, крім оксидів заліза, є також оксиди й інших елементів (наприклад, Mn, Nі, Cr, V, Sі, Р). Оксиди цих елементів відновлюються і частково переходять в чавун, частково в шлак. Відновлення більшості цих елементів здійснюється прямим шляхом в зоні температур 1100…1500С.
Навуглецювання заліза. Відновлене залізо насичується вуглецем за реакцією:
2CO CO2 + C
C + 3Fe → Fe3C
_______________________
3Fe + 2CO Fe3C + CO2
Цей процес найбільш активно відбувається при температурах понад 820…850°С і, як показують прямі досліди з визначення вмісту вуглецю, уже в нижній частині шахти і в розпарі концентрація вуглецю в залізі досягає 1,0 %. Утворення сплаву заліза з вуглецем, що має температуру плавлення нижчу, ніж чисте залізо, приводить до формування крапель рідкого чавуну, який стікає в нижню частину печі через шар розжареного коксу, ще більше насичуючись вуглецем і його вміст у чавуні досягає звичайно 3…4 %.
Неминучість навуглецювання відновленого заліза у доменній печі виключає можливість одержання в ній як кінцевого продукту заліза або сталі. Марганець, хром, ванадій і титан сприяють навуглецюванню чавуну, а кремній, сірка і фосфор зменшують вміст вуглецю в чавуні.
Шлакоутворення і його вплив на хід доменного плавлення. Кількість утворюваних шлаків становить 50…60 % від кількості чавуну, що випускається доменною піччю. Продуктивність доменної печі і кількість чавуну, що випускається, значною мірою залежать від складу і властивостей утворюваних шлаків. Шлак утворюється при взаємодії пустої породи (SіO2, Al2O3), закису заліза (FeO) і вапняку (CaCO3).
Первинний шлак, що утворився спочатку, поступово просочується до горна печі, збагачуючись при цьому різними окислами пустої породи і змінюючи свій склад та властивості, стає більш тугоплавким і іноді густим.
Хід доменного плавлення і температура горна визначаються в основному властивостями утворюваних шлаків.
Легкоплавкі шлаки швидко проходять зону максимальної температури, не встигають нагрітися і охолоджують горно печі. Більш тугоплавкі шлаки сприяють збереженню в горні високої температури, що особливо важливо при плавленні спеціальних чавунів.
Випускання рідких продуктів плавки. Рідкий чавун та шлак, що нагромаджуються в горні печі, періодично випускають з горна через спеціальну чавунну льотку, забиту вогнетривкою масою. Отвір у ній пробивають чи просвердлюють за допомогою спеціальних машин або пропалюють киснем.
Рідкий чавун шість раз на добу по спеціальному жолобу, футерованому вогнетривким матеріалом, зливають у ковші місткістю до 80…100 т і транспортують до місця дальшого призначення.
Шлак випускають частіше. Він виливається через шлакову льотку, що закривається залізною конічною пробкою, у шлаковозні ковші, які мають об’єм 16 м3.
Продукти доменного виробництва. У процесі перероблення залізної руди в доменній печі отримують чавун, шлак, доменний газ, доменний пил. Чавун основна продукція, а шлак, доменний газ – побічна. Головними продуктами доменного виробництва є чавуни і феросплави, побічними - шлак і доменний газ. Залежно від хімічного складу, будови і призначення виплавлені в доменній печі чавуни поділяються на переробні, ливарні і спеціальні.
Переробний чавун - основний вид чавуну, призначений для виробництва сталі. У кисневих конверторах, в мартенівських печах і в незначній кількості в електропечах. Звичайний його склад: 3,5...4,5 % С; 0,3…1,3 % Sі; 0,8... 1,2 % Мn; до 0,3 % Р і 0,07 % S. Особливістю переробних чавунів є те, що вуглець в них знаходиться у вигляді сполуки Fе3С - цементиту. Такі чавуни на зламі мають білий відтінок, тому їх ще називають білими. Вони відрізняються великою твердістю, обробляти різанням їх важко, тому як конструкційний матеріал вони використовуються рідко. У ливарному виробництві з них дістають ковкий чавун.
Ливарний чавун призначений для одержання фасонного литва, відзначається підвищеним вмістом кремнію (до 3,6 %). Більша частина вуглецю в ньому перебуває у вільному стані - у вигляді пластинчастого графіту, тому на зламі вони мають сірий відтінок. Такі чавуни називають сірими.
Ливарний чавун везуть у ковші до розливальної машини і розливають у закріплені на безперервному конвеєрі виливниці. Після затвердіння і охолодження водою п'ятидесятикілограмові чавунні чушки випадають при повороті конвеєра із виливниць на залізничні платформи.
Спеціальні чавуни, або феросплави, - це сплави заліза із значним вмістом кремнію, марганцю та інших елементів. До них належать: феросиліцій (9...13 % Sі), феромарганець (70...75 % Мn), дзеркальний чавун (10...25 % Мn) та ін. Їх застосовують для розкислення та легування сталі.
Головну масу серед продуктів доменного виробництва становлять переробні чавуни - 75...80 %. На долю ливарних чавунів припадає 15...20 % і феросплавів – 1...2 %.
Спеціалісти металургійної промисловості підрахували, що майже половина руди переходить у шлак. Так, доменна піч об’ємом 3000 м3 за добу перероблює 8500 т шихти, а видає 5000...5500 т чавуну.
