
- •1.2. Основные этапы развития лекарствоведения
- •1.3. Краткая история отечественного лекарствоведения
- •1.4. Методы исследования, применяемые в фармакологии
- •1.5. Пути получения новых лекарственных веществ
- •2. Общая фармакология
- •2.1. Пути введения лекарственных веществ в организм
- •2.2. Фармакокинетика
- •2.2.1. Резорбция лекарственных веществ
- •2.2.2. Распределение лекарственных веществ в организме
- •2.2.3. Биотрансформация лекарственных веществ
- •2.2.4. Пути выведения лекарственных веществ из организма
- •2.3. Фармакодинамика и факторы, влияющие на нее
- •2.3.1. Влияние химической структуры лекарственного вещества на его фармакодинамику
- •2.3.2. Доза и принципы дозирования
- •2.3.3. Лекарственная форма и ее значение в проявлении фармакодинамики
- •2.3.5. Фармакодинамические эффекты при одновременном введении двух и более лекарственных веществ
- •2.3.6. Отрицательные фармакодинамические эффекты при повторных введениях лекарственных веществ
- •2.3.7. Виды действия лекарственных веществ
- •2.4. Механизм действия лекарственных веществ
- •2.5. Положительное и отрицательное действие лекарственных веществ
- •2.6. Взаимосвязь между фармакодинамическим и фармакотерапевтическим комплексом эффектов лекарственных веществ
- •2.7. Общие принципы лечения при отравлении лекарственными веществами
- •2.8. Классификация лекарственных веществ
2.2. Фармакокинетика
Понятие «фармакокинетика» (от греч. pharmacon — лекарство, kineo — двигать) включает все виды концентрационных, количественных и качественных состояний лекарственного вещества от момента резорбции до момента его выведения из организма в неизмененном или измененном состоянии. В частности, фармакокинетика рассматривает процессы резорбции, распределения, биотрансформации и выведения лекарственных веществ из организма. Фармакокинетика позволяет рассматривать взаимоотношения между лекарственным веществом и организмом на уровне концентраций фармакологических веществ в различных органах и биологических жидкостях организма, что обеспечивает более точный анализ закономерного распределения лекарств, их биологической доступности, локализации, а также положительного и побочного прямого действия. Несомненно, фармакокинетические исследования служат фундаментальной основой для создания оптимальных схем лечения с одновременным учетом фундаментальных фармакодинамических данных.
2.2.1. Резорбция лекарственных веществ
Скорость и полнота всасывания лекарственных веществ зависят от пути введения, площади всасывания, кровоснабжения органа, лекарственной формы, функционального и морфологического состояния тканей и других факторов. О скорости и полноте всасывания наиболее объективно можно судить только по количеству исчезающего из «депо» лекарственного вещества за определенный промежуток времени, что указывает на количественное содержание его непосредственно во внутренней среде организма. Однако аматемтические расчеты количества лекарства в организме на соответствующий отрезок времени меньше количества резорбированного. Это объясняется тем, что одновременно с резорбцией (от лат. resorbere — поглощение, всасывание) тут же происходят и выделение, и образование комплексов (молекула белка альбумина + + молекула лекарственного вещества), и биотрансформация, и распределение по органам и тканям.
П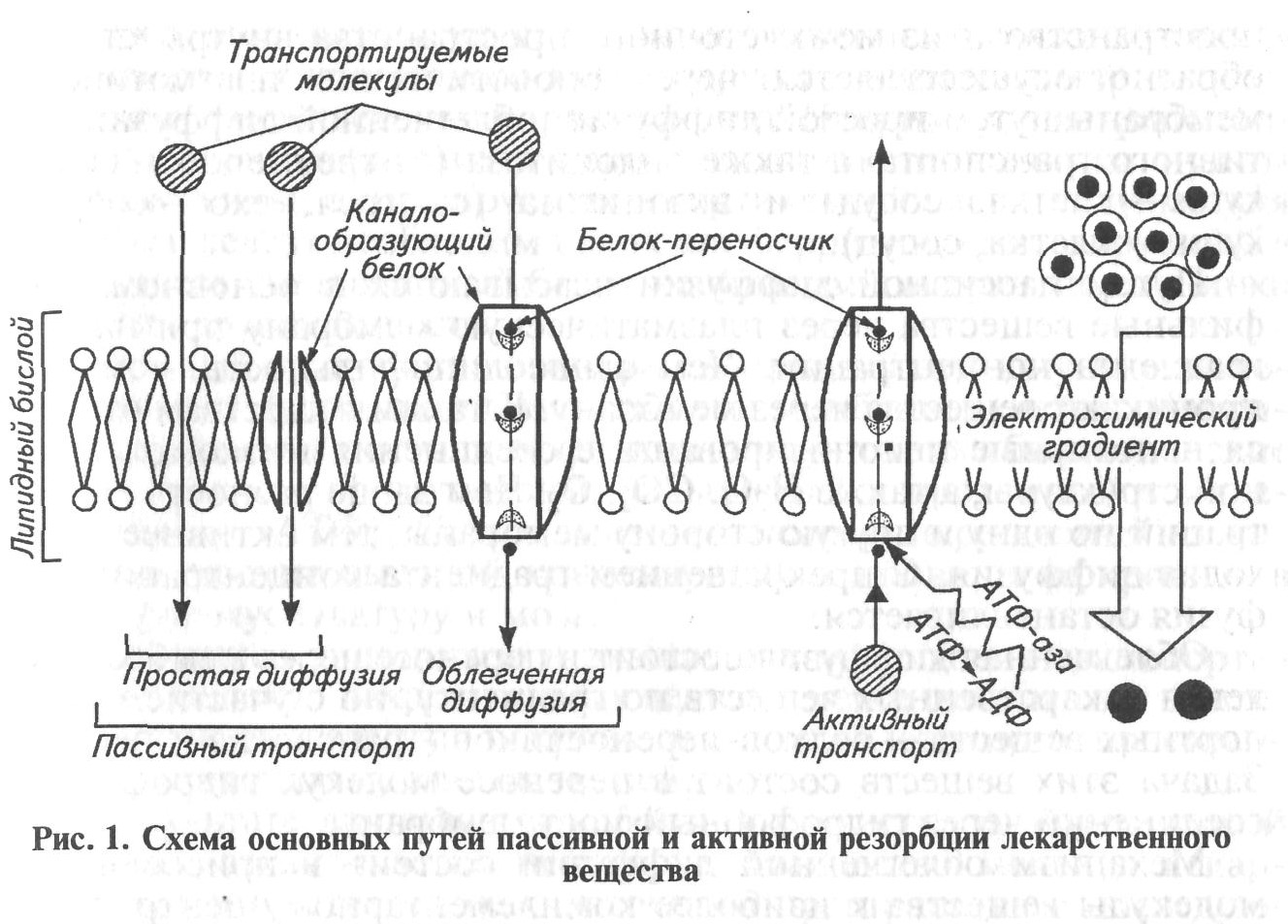 ри
резорбции молекулы лекарственных
веществ должны преодолеть различной
сложности биологические барьеры. Чаще
всего биологические барьеры состоят
из одного или нескольких слоев
эпителиальных или эндотелиальных
клеток. Общеизвестно, что цитоплазматические
мембраны, через которые должны проникать
лекарственные вещества в кровь, строго
детерминируют проницаемость. Пассивный
переход лекарственных веществ через
комплексные барьеры подчиняется тем
же физическим законам, которые
определяют переход через простые
липидные мембраны. Жирорастворимые
вещества, вода и небольшие молекулы или
ионы переходят весьма свободно, тогда
как крупные гидрофильные молекулы
могут проникать через мембраны только
посредством специфических транспортных
механизмов (рис. 1).
ри
резорбции молекулы лекарственных
веществ должны преодолеть различной
сложности биологические барьеры. Чаще
всего биологические барьеры состоят
из одного или нескольких слоев
эпителиальных или эндотелиальных
клеток. Общеизвестно, что цитоплазматические
мембраны, через которые должны проникать
лекарственные вещества в кровь, строго
детерминируют проницаемость. Пассивный
переход лекарственных веществ через
комплексные барьеры подчиняется тем
же физическим законам, которые
определяют переход через простые
липидные мембраны. Жирорастворимые
вещества, вода и небольшие молекулы или
ионы переходят весьма свободно, тогда
как крупные гидрофильные молекулы
могут проникать через мембраны только
посредством специфических транспортных
механизмов (рис. 1).
Резорбция лекарственных веществ, а также, всех компонентов питательных, минеральных и биологически активных веществ из Желудочно-кишечного тракта в кровь, из крови в межклеточное
пространство и из межклеточного пространства внутрь клетки и обратно осуществляется через биологические плазматические мембраны путем простой диффузии, облегченной диффузии и активного транспорта, а также эндоцитоза (от греч. endo — внутри, kytos — клетка, сосуд) и экзоцитоза (от греч. ехо — снаружи, kytos — клетка, сосуд).
Путем пассивной диффузии всасываются в основном липо-фильные вещества через плазматическую мембрану при наличии градиента концентрации. Чем выше липофильность, тем легче проникают вещества через мембрану. К таким веществам относятся неполярные неионизированные соединения низкомолекулярной структуры, а также Н20, СО2, 02. Чем выше разность концентраций по одну и другую сторону мембраны, тем активнее происходит диффузия. С прекращением градиента концентраций диффузия останавливается.
Облегченная диффузия состоит в переносе через мембрану молекул лекарственных веществ по градиенту, но с участием транспортных веществ — белков-переносчиков (транслоказ и пермеаз). Задача этих веществ состоит в переносе молекул гидрофильных соединений через гидрофобный мост мембраны.
Механизм облегченной диффузии состоит в присоединении молекулы вещества к наиболее комплементарному центру транслоказы, что обеспечивает конформацию ее молекулы и открывание гидрофильного канала с последующим освобождением молекулы фармакологического вещества по другую сторону мембраны. Таким образом, для облегченной диффузии в отличие от простой необходима высокая избирательность.
Простая и облегченная диффузии действуют непрерывно, пока в организм вводят фармакологическое вещество.
Активный транспорт осуществляется транспортными средствами биологических клеточных мембран и характеризуется избирательностно к определенным соединениям, насыщенностью (концентрацией) вещества в межклеточном пространстве, вероятной конкуренцией двух соединений за одно транспортное вещество, возможностью транспорта против градиента с затратой энергии. Активный транспорт осуществляется в отношении гидрофильных полярных (ионизированных) молекул, некоторых неорганических ионов, Сахаров, аминокислот, пиримидинов и др.
При активном транспорте через цитоплазматические мембраны молекулы лекарственного вещества образуют временный комплекс с комплементарной молекулой транспортного средства. Образованный комплекс проходит через всю толщину плазматической мембраны, и на внутренней ее поверхности молекула лекарственного вещества отделяется от комплекса и дальше диффундирует в цитоплазме к базальному участку с последующим транспортом в кровь. Поскольку транспортирование происходит в двух полярных направлениях, то, по-видимому, молекула транспортного соединения из цитоплазмы переносит также молекулу ненужного для клетки того же или другого комплементарного соединения в межклеточное пространство. Например, для транспортировки цианокобаламина через слизистую кишечника нужны гликопротеиды, синтезируемые в кардиальной части желудка; для переноса железа необходим белок апоферритин, синтезируемый в депо железа. Аналогичный белок необходим для транспорта цинка и многих других веществ.
Активный транспорт можно рассматривать как одну из основополагающих функций плазматической мембраны клеток. Например, в организме постоянно функционируют такие биологические насосы, как калий-натриевый, кальциевый и протонный с затратой энергии (АТФ). Сахара и аминокислоты переносятся из кишечника против высокой концентрации в крови, а из крови — в скелетную мускулатуру и мозг.
С помощью эндоцитоза и экзоцитоза происходит транспортирование молекул лекарственных веществ через цитоплазму эпителия клеток кишечника в кровь и из межклеточного пространства — в цитоплазму клеток тканей.
В результате впячивания небольшого участка плазматической мембраны захватывается некоторое количество молекул лекарственного вещества из межклеточного пространства с последующим образованием пузырька, его отшнуровыванием и мигрированием в цитоплазме к противоположному участку внутренней поверхности мембраны, где в результате црисоединения к ее поверхности происходит выбрасывание его содержимого в кровь (экзоцитоз).
Таким образом, при любом пути всасывания лекарственного вещества из просвета кишечника его молекулы из апикальной части клетки эпителия кишечника поступают в цитоплазму и, завершив диффузию до базального участка клетки, выводятся одним из путей в кровь. При резорбции из межклеточного пространства молекулы лекарственных веществ или взаимодействуют с рецепторами цитоплазматической мембраны с передачей генерированного стимула (попадая в результате этого взаимодействия внутрь клетки через биохимические системы), или проникают в цитоплазму клетки и там взаимодействуют с комплементарными макромолекулами (рецепторами) опять же с генерированием стимула полярной направленности. Другая же часть веществ, поступивших в цитоплазму (биохимические мономеры, ионы неорганических соединений и др.), используется в клетке для биосинтеза более сложных соединений — макромолекул, являющихся структурно-функциональными компонентами клетки.
Взаимосвязанной функцией с резорбцией является функция выведения, экскреция лекарственных веществ из организма в неизмененном и измененном виде. Выведение начинается, естественно, из цитоплазмы клетки в межклеточное пространство, от куда вещество поступает в капиллярную систему венозной крови или лимфы, в итоге с током крови достигает клеток секреторно-экскреторных органов и через их плазматические мембраны и межклеточные образования попадает в соответствующие каналы с последующим выведением из организма.
Таким образом, резорбция и выведение лекарственных веществ являются функциями универсальными, имеющими существенное значение для их распределения.
Лекарственные вещества в большинстве своем представляют органические соединения со слабыми кислотными или щелочными свойствами. В неионизированном состоянии они более жирорастворимы, а в ионизированном состоянии — более водорастворимы, поэтому неионизированные молекулы лекарственного вещества будут более свободно проходить через мембрану, чем ионизированные. Эти данные указывают на то, что резорбция, распределение и выведение лекарственных веществ в значительной степени будут зависеть от концентрации водородных ионов.
