
- •1.2. Основные этапы развития лекарствоведения
- •1.3. Краткая история отечественного лекарствоведения
- •1.4. Методы исследования, применяемые в фармакологии
- •1.5. Пути получения новых лекарственных веществ
- •2. Общая фармакология
- •2.1. Пути введения лекарственных веществ в организм
- •2.2. Фармакокинетика
- •2.2.1. Резорбция лекарственных веществ
- •2.2.2. Распределение лекарственных веществ в организме
- •2.2.3. Биотрансформация лекарственных веществ
- •2.2.4. Пути выведения лекарственных веществ из организма
- •2.3. Фармакодинамика и факторы, влияющие на нее
- •2.3.1. Влияние химической структуры лекарственного вещества на его фармакодинамику
- •2.3.2. Доза и принципы дозирования
- •2.3.3. Лекарственная форма и ее значение в проявлении фармакодинамики
- •2.3.5. Фармакодинамические эффекты при одновременном введении двух и более лекарственных веществ
- •2.3.6. Отрицательные фармакодинамические эффекты при повторных введениях лекарственных веществ
- •2.3.7. Виды действия лекарственных веществ
- •2.4. Механизм действия лекарственных веществ
- •2.5. Положительное и отрицательное действие лекарственных веществ
- •2.6. Взаимосвязь между фармакодинамическим и фармакотерапевтическим комплексом эффектов лекарственных веществ
- •2.7. Общие принципы лечения при отравлении лекарственными веществами
- •2.8. Классификация лекарственных веществ
2.3. Фармакодинамика и факторы, влияющие на нее
Фармакодинамика (от греч. pharmacon — лекарство, dinamis — сила) изучает закономерности проявления комплекса эффектов при введении фармакологических веществ в динамике на метаболическом, функциональном и морфологическом уровнях — от момента их начального возникновения и до полного исчезновения и восстановления показателей до нормального уровня.
Следует иметь в виду, что как динамика одного эффекта, так и динамика всего комплекса эффектов, обусловленного фармакологическим веществом, возникает, развивается и угасает закономерно.
Введенное в организм лекарственное вещество на молекулярном уровне взаимодействует непосредственно с определенными рецепторами клетки, расположенными на плазматической мембране, во внутриклеточных структурах и цитоплазме, в результате чего возникает ответная реакция клетки на метаболическом и функциональном уровнях с последующим распространением всего комплекса эффектов на орган, систему и организм в целом.
Поскольку любое лекарственное вещество в организме животных распределяется неравномерно, то, естественно, и величина реакции взаимодействия в ткани, органе и системе будет регистрироваться с разной степенью выраженности. Фармакодинамика, как и все биохимические процессы и функции, развивается строго закономерно. Через определенный интервал, продолжительность которого зависит от многих факторов, а в основном от биологической активности и пути введения, после резорбции лекарственного вещества в организме начинают проявляться первые ответные реакции на введенное фармакологическое вещество. Степень выраженности этих реакций очень слабая, но они могут быть зарегистрированы инструментально и даже визуально. Первоначальные реакции регистрируются во всех органах и тканях, в которых концентрация лекарственного вещества достигает пороговых величин, а там, где она не достигла этого уровня, реакция еще не регистрируется. Сразу же после введения начинается резорбция лекарственного вещества, но его концентрация в тканях и органах находится на таком уровне, который в силу действия гомеостатических и адаптационных факторов не проявляет себя в такой мере, чтобы быть зарегистрированным.
П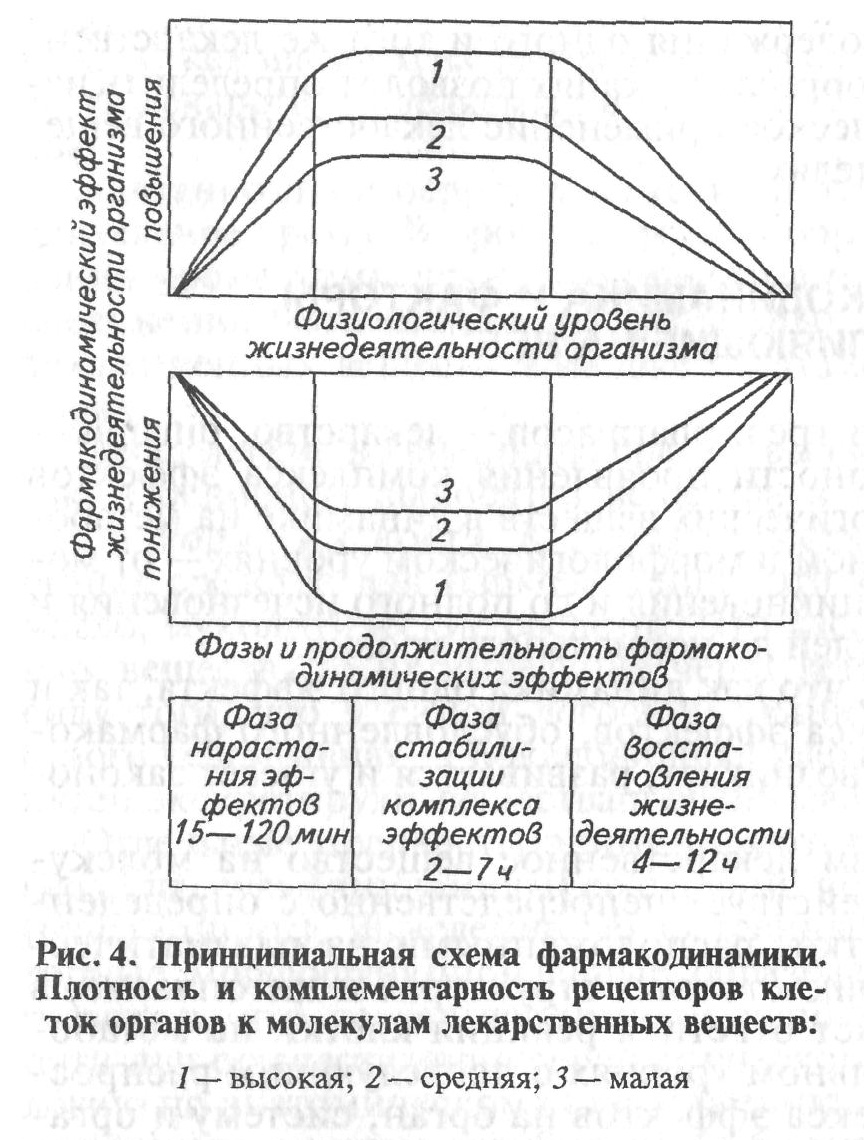 о
степени выраженности и направленности
комплекса фармакодинамических
эффектов
весь период фармакодинамики можно
разделить на три фазы. Первая фаза,
регистрация которой на метаболическом
и функциональном уровнях начинается
через небольшой промежуток времени
после введения лекарственного
вещества, характеризуется быстрым
нарастанием выраженности
фармакодинамических эффектов и
достижением их максимальных
параметров через
15—120 мин. Максимально
выраженный фармакодинамический комплекс
в течение некоторого времени (2— 8 ч)
поддерживается в исключительно высоких
параметрах (вторая фаза). В течение
третьей фазы выраженность
фармакодинамических эффектов постепенно
начинает уменьшаться во всех органах
с достижением нулевых показателей
(рис. 4).
о
степени выраженности и направленности
комплекса фармакодинамических
эффектов
весь период фармакодинамики можно
разделить на три фазы. Первая фаза,
регистрация которой на метаболическом
и функциональном уровнях начинается
через небольшой промежуток времени
после введения лекарственного
вещества, характеризуется быстрым
нарастанием выраженности
фармакодинамических эффектов и
достижением их максимальных
параметров через
15—120 мин. Максимально
выраженный фармакодинамический комплекс
в течение некоторого времени (2— 8 ч)
поддерживается в исключительно высоких
параметрах (вторая фаза). В течение
третьей фазы выраженность
фармакодинамических эффектов постепенно
начинает уменьшаться во всех органах
с достижением нулевых показателей
(рис. 4).
Второй закономерностью в фармакодинамике является разная степень выраженности изменений в различных органах и системах с разновременным их исполнением и исчезновением.
Как уже было сказано, разная степень комплементарности и плотности рецепторов клеток в основном определяет действительное (преимущественное) влияние лекарственных веществ. Из рис. 4 видно, что выраженность фармакодинамических эффектов в различных органах разная при введении веществ, обеспечивающих комплекс эффектов как усиления, так и угнетения внутриклеточного метаболизма и функций. Например, кофеин более эффективно изменяет функцию ЦНС, в меньшей степени — функцию сердечно-сосудистой и еще менее выраженно изменяет функцию скелетной мускулатуры и желудочно-кишечного тракта, а эфир сильно угнетает кору большого мозга и спинной мозг, в меньшей степени подавляет функцию продолговатого мозга и менее выраженно подавляет функцию почек, желудка и кишечника.
Между фармакокинетикой и фармакодинамикой существует глубокая взаимосвязь, поскольку концентрация лекарственного вещества определяет выраженность и направленность фармакодинамических эффектов. Так, в первой фазе происходит быстрое нарастание концентрации в разных органах, но с некоторой разновременностью, а параллельно — быстрое усиление фармакодинамических эффектов. Во второй фазе, когда уравновешиваются приток в ткани и потери лекарственного вещества, происходит и сохранение фармакодинамических эффектов с максимальной выраженностью. В заключительной фазе фармакодинамики выраженность эффектов постепенно уменьшается соответственно постепенному, но неуклонному снижению уровня лекарственного вещества в отдельных тканях и органах и организме в целом.
Третьей закономерностью для фармакокинетики и фармакодинамики является постепенное нарастание событий: рост стимулирующей и угнетающей направленности в момент начала проявления, достижения их максимальных значений, начала ослабления действия и в зоне исчезновения эффектов происходит постепенно и равномерно.
Параметры фармакодинамических эффектов усиливающей и угнетающей направленности должны находиться в пределах физиологических возможностей с сохранением закономерностей жизнедеятельности целостного организма. Однако фармакотерапевтическая практика в отдельных случаях требует применения фармакологических средств в дозах, нарушающих закономерности в организме (наркотические средства, местные анестетики, слабительные, химиотерапевтические вещества и др.), т. е. в период проявления токсичного действия.
Морфологическими (гистологическими, электронно-микроскопическими) и биохимическими исследованиями внутренних органов, органов эндокринной системы и скелетной мышцы установлено, что изменения во внутриклеточном метаболизме после прекращения введения пенициллинов, тетрациклинов и тилозинсодержащих препаратов сохраняются в течение 60—90 сут и более. Рядом исследователей определено, что в теле убитых животных после введения антибиотиков из группы пенициллинов, тетрациклинов и стрептомицина их обнаруживают в связанном состоянии с миоглобином до 6 мес и более.
Таким образом, между обнаруживаемыми биохимическими и функциональными изменениями существует разрыв во времени, т. е. во внутриклеточном метаболизме сохраняются изменения, а в функциональном отношении изменений не выявляется. По-видимому, нужны более чувствительные методы исследования, чтобы определить сохраняющиеся небольшие изменения во внутриклеточном интегративном функциональном ответе.
После окончания резорбции, когда концентрация лекарственного вещества постепенно снижается, все фармакодинамические эффекты начинают угасать в обратной последовательности, т. е. вначале в органах с пороговыми, затем с оптимальными и в последнюю очередь с максимальными концентрациями лекарственного вещества.
Каждое лекарственное вещество при введении в оптимальных терапевтических дозах вызывает в органах, системах и организме в целом соответствующие изменения в метаболических процессах и физиологических функциях, а возможно, и во внутриклеточной структуре.
По сумме вызываемых фармакодинамических эффектов на метаболическом, функциональном и структурном уровнях и их направленности лекарства можно разделить на две большие группы: вещества, повышающие метаболизм и функцию структур, и вещества, угнетающие их.
Поскольку нейроэндокринная система выполняет регулирующую, интегрирующую, трофическую и пусковую функции, то естественно, комплекс фармакодинамических эффектов и их направленность в первую очередь будут определяться ее состоянием. Однако избирательность действия каждого лекарственного вещества в результате непосредственного воздействия определяет выраженность и направленность фармакодинамических эффектов преимущественно каким-то органом или системой, например усиление или угнетение гемопоэтической функции кроветворной системы, иммунной системы, моторно-секреторной функции желудочно-кишечного тракта, сердечно-сосудистой системы и др.
Применение лекарственных веществ для лечебно-профилактических целей также преследует две цели: усиление или ослабление функционального состояния органа, системы или всего организма в целом с целью доведения измененных обмена, функций и структуры до уровня физиологических показателей.
Исходный уровень жизнедеятельности организма животного вследствие физической и интеллектуальной усталости или патологического состояния может быть резко снижен и находиться на нижних границах нормы или даже ниже нормы. В этих случаях введение лекарственных веществ общетонизирующего действия приводит к восстановлению функционального состояния центральной нервной системы и всей жизнедеятельности до уровня, соответствующего данному индивидууму. Этот эффект называется тонизирующим.
П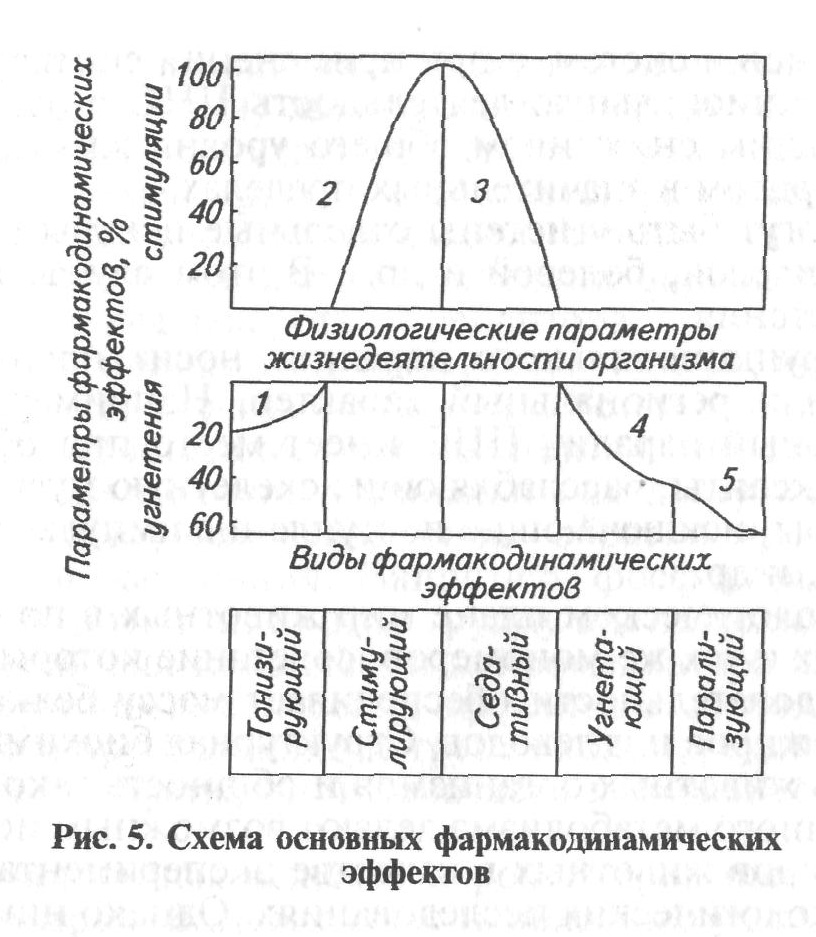 ри
ряде болезней, эмоциональных состояний
и действии факторов внешней среды
активность ЦНС и в целом жизнедеятельность
организма находятся на более высоком
уровне по сравнению
с нормой. Например, при перевозке
животных, а также при
технологических перегруппировках
животных и действии других
факторов развивается стресс-реакция,
которая не только приводит
к понижению прироста живой массы, но и
к развитию патологических
состояний. С целью восстановления
функционального уровня организма
до физиологических пределов необходимо
применить фармакологические препараты
из группы седативных и транквилизаторов,
а также адаптагенов, ослабляющие процессы
возбуждения в ЦНС, снижающие метаболические
процессы в организме и обеспечивающие
нормализацию жизнедеятельности
организма. Этот эффект называют
успокаивающим, седативным (рис. 5).
ри
ряде болезней, эмоциональных состояний
и действии факторов внешней среды
активность ЦНС и в целом жизнедеятельность
организма находятся на более высоком
уровне по сравнению
с нормой. Например, при перевозке
животных, а также при
технологических перегруппировках
животных и действии других
факторов развивается стресс-реакция,
которая не только приводит
к понижению прироста живой массы, но и
к развитию патологических
состояний. С целью восстановления
функционального уровня организма
до физиологических пределов необходимо
применить фармакологические препараты
из группы седативных и транквилизаторов,
а также адаптагенов, ослабляющие процессы
возбуждения в ЦНС, снижающие метаболические
процессы в организме и обеспечивающие
нормализацию жизнедеятельности
организма. Этот эффект называют
успокаивающим, седативным (рис. 5).
В некоторых случаях у животных с низким физиологическим уровнем жизнедеятельности, а также на определенной стадии болезни в ходе терапевтического вмешательства возникает необходимость усиления функционального состояния ЦНС и жизнедеятельности организма в целом до высоких границ нормы и даже выше нормы. Целесообразно стимулировать гемопоэз, регенерацию тканей, секреторную функцию пищеварительных желез, иммуногенез, рост животных, функциональное состояние нервной системы, мочеобразовательной функции почек и др.
Эффект стимуляции в большинстве случаев является временным феноменом, поскольку он не соответствует физиологическим параметрам и тем самым обусловливает истощение возможностей органа, системы или даже организма в целом с одновременным Усилением адаптационно-трофических процессов.
В отдельных случаях, наоборот, появляется необходимость не стимулировать жизнедеятельность организма, а снижать ее до низких границ нормы и ниже. С помощью местноанестезирующих средств в значительной степени можно снизить функцию от дельных органов и систем, а при применении снотворных средств ослабить функциональную деятельность ЦНС с одновременным соответствующим снижением общего уровня жизнедеятельности организма, притом в значительных пределах.
В ЦНС могут быть угнетены отдельные центры (теплорегулирующий, кашлевой, болевой и др.). В этом случае речь идет об эффекте угнетения.
Эффект функционального паралича носит преимущественно системный или региональный характер. Например, временный функциональный паралич ЦНС имеет место при общей анестезии: миорелаксанты, расслабляющие скелетную мускулатуру; ганглиоблокаторы, исключающие поступление импульсов к внутренним органам, и др.
В общебиологическом плане мир животных в принципе построен из одних и тех же мономеров, сочетание которых по количеству и последовательности обеспечивает массу белков и в меньшей степени жиров и углеводов. Структурная биохимическая универсальность животных организмов и общность закономерностей внутриклеточного метаболизма делают возможным использование различных видов животных в качестве экспериментальных моделей в фармакологических исследованиях. Однако никогда не надо забывать, что организм инфузории, лягушки, крысы и т. д. отличается от организма свиньи, коровы, лошади и т. д. как в норме, так и в патологии, поэтому данные, полученные на лабораторных животных, нельзя полностью трансполировать на сельскохозяйственных животных. Поэтому после установления общих закономерностей в фармакодинамических реакциях на мелких животных следует провести экспериментальные исследования в меньших размерах на сельскохозяйственных животных, которые могут внести коррективы не в саму фармакодинамическую закономерность, полученную на мелких животных, а в силу реакции и продолжительность регистрации реакции на фармакологический препарат.
Многочисленными исследованиями установлено: у животных одного вида один и тот же фармакологический препарат в основном вызывает однотипные, но не идентичные фармакодинамические эффекты, что обусловлено индивидуальными, генетическими особенностями организма.
