
- •Введение Предмет и задачи химии окружающей среды
- •Происхождение и эволюция Земли
- •Образование земной коры и атмосферы
- •Эволюция атмосферы и происхождение жизни
- •Гидросфера
- •Глава 1. Физико-химические процессы в атмосфере
- •1.1. Состав атмосферы
- •1.2. Микрокомпонентные примеси в атмосфере
- •Время пребывания следов газов в естественной атмосфере
- •1.2.1. Геохимические источники
- •1.2.2. Биологические источники.
- •1.2.3. Антропогенные источники
- •Содержание основных компонентов выхлопов двигателей внутреннего сгорания (двс)
- •1.3 Смоги
- •1.4. Радиоактивное загрязнение атмосферы
- •Основные радиоактивные изотопы, обнаруживаемые в атмосфере после ядерного взрыва
- •1.5. Озоновый защитный слой
- •1.5.1. Механизмы разрушения озона
- •1.6. «Парниковый эффект»
- •Глава 2. Физико-химические процессы в литосфере
- •2.1. Состав и строение литосферы
- •2.2. Процессы выветривания
- •2.3. Почвы. Химический состав, свойства, загрязнение
- •2.3.1. Общие для большинства почв реакции
- •2.3.2. Катионный обмен
- •2.3.3. Потенциальная кислотность почв
- •2.3.4. Щелочность почв
- •2.3.5. Окислительно-восстановительные режимы
- •2.3.6. Гумификация
- •2.3.7. Химическое загрязнение и охрана почв
- •Глава 3. Физико-химические процессы в гидросфере
- •3.1. Пресные воды подземной гидросферы
- •3.2. Химия пресных поверхностных вод
- •3.2.1. Химия воды и режимы выветривания
- •3.2.2. Растворенные твердые вещества пресных вод
- •3.23. Биологические процессы
- •3.2.4. Диаграммы Eh-pH
- •3.2.5. Питательные вещества и эвтрофикация
- •3.3. Кислотные осадки
- •3.4. Океаны
- •3.5. Процессы в дельтах и эстуариях
- •Глава 4. Особенности распространения, трансформации и накопления загрязняющих веществ в окружающей среде
- •4.1. Изменения веществ в окружающем среде
- •4.1.1. Изменения во времени
- •4.1.2. Пространственные изменения
- •4.1.3. Распространение в окружающей среде
- •4.2. Перенос между различными средами
- •4.2.1. Перенос почва — вода
- •4.2.2 Перенос вода — воздух
- •4.23. Перенос почва -—воздух
- •4.2.4. Поступление и накопление в живых организмах
- •4.2.5. Географический и биотический перенос
- •4.3. Геохимические барьеры
- •4.4. Круговороты макроэлементов
- •Вещества, попавшие в окружающую среду исключительно в результате.Человеческой деятельности
- •4.4.1. Углерод
- •Атмосфера
- •4.4.2. Азот
- •Белок Аммонификация Фотосинтез
- •4.4.3. Фосфор
- •4.4.4. Сера
- •4.5. Круговороты второстепенных элементов
- •4.5.1. Галогены
- •Соединения хлора
- •Соединения йода
- •Соединения брома
- •Соединения фтора
- •4.5.2. Тяжелые металлы
- •Атмосфера
- •Биомасса
- •Общий запас
- •Общий запас
- •Стронций
Стронций
Sr -хороший пример ранее малоизученного элемента, который теперь служит объектом особого внимания в связи с большой опасностью его радиоактивного изотопа для человека и животных. По свойствам стронций похож на кальций. На 1000 атомов кальция, участвующих в биогеохимическом цикле в природе, приходится 2,4 атома стронция. При производстве ядерного оружия и при работе атомных станций среди отходов обнаруживается радиоактивный стронций-90, который был неизвестен до расщепления атома человеком. Даже ничтожно малые количества радиоактивного Sr, поступающие в окружающую среду с утечками из ядерных реакторов и после испытаний атомного оружия, опасны, поскольку мигрируют вместе с кальцием. Стронций, попадая через растения и животных в пищу человека, может накапливаться в костных тканях людей, как и кальций. По мнению некоторых ученых, в костях человека уже содержится такое количество стронция, которое может оказывать канцерогенное действие.
Ртуть
В соединениях ртуть может быть как двухзарядной, так и формально однозарядной; она характеризуется высоким потенциалом ионизации и окислительным потенциалом, является химически стойким элементом. Одной из главных особенностей иона ртути является способность к образованию комплексных соединений с координационными числами от 2 до 8. Связь «ртуть — лиганд» во всех комплексах является ковалентной. Наиболее устойчивы комплексы с лигандами, содержащими атомы галогенов, углерода, азота, фосфора, серы. Ртуть образует также значительное число комплексов с органическими реагентами, характеризующихся высокой прочностью (8-меркаптохинолин, тиомочевина). Известны и ртуть органические соединения типа RHgX или R2Hg, обнаруженные в последнее время в различных компонентах биосферы — донных осадках, природных водах.
Электростанции, работающие на угле

Рис. 29. Загрязнение озера ртутью
Ртуть встречается в природе как в самородном состоянии, так и в соединениях, образуя ртутные минералы: киноварь HgS, тиманит HgSe, ливингстонит HgS•2Sb2S3 монтроидит HgO. Ртуть входит в качестве изоморфной или механической примеси в реальгар, антимонит, молибденит, пирит, пирротин, сфалерит. Среднее содержание ртути в каменном угле составляет 1 • 10-6 %.
За геологическое время в биосферу в результате природных процессов (вулканическая деятельность) поступило около 1,6 • 1010 т ртути. Около 0,1% остается в океанах в растворенном виде.
Биогеохимический цикл ртути Hg - пример круговорота природного элемента, который почти не влиял на организмы до наступления индустриальной эры. Ртуть химически малоподвижна, а концентрации ее в природе невелики. Разработка месторождений и промышленное использование увеличили поток ртути в атмосферу. Соответственно увеличился и ее сток с поверхностными водами. Увеличение содержания ртути, как, впрочем, и других тяжелых металлов (кадмия, меди, цинка, хрома) в окружающей среде стало серьезной проблемой. Ртуть используется в различном электротехническом оборудовании, термометрах, зубных пломбах, лекарствах, красках, фунгицидах и др. Больше половины расходуемой ртути не возвращается в производство. Эта означает, что она попадает в природные воды и оказывается в окружающей среде (рис. 29).
На рис. 30 показаны оценки потоков ртути в сравнении с ее потоками в доиндустриальный период. Запасы ртути указаны в прямоугольниках в сотнях тонн, а потоки (стрелки) - в сотнях тонн в год. Цифры в скобках показывают потоки до появления человека. Штрихами обозначены два новых потока, порожденных деятельностью человека
В результате разработки отложений и увеличения выбросов ртути возрастает ее количество в почвах, воде, живых организмах. При этом микроорганизмы, участвующие в круговороте, превращают ее нерастворимые формы в растворимую, очень подвижную и очень ядовитую - метилртуть. Рыбы и моллюски накапливают метилртуть до концентраций, опасных для человека, использующего их в пищу.
Трансформация веществ в окружающей среде и накопление их в живых организмах в процессе круговорота должны учитываться при использовании опасных химических элементов.
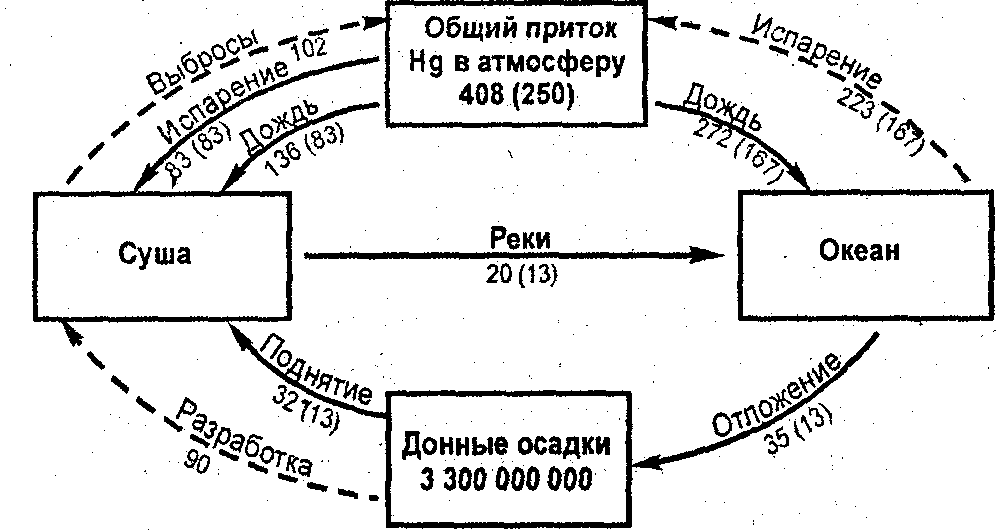
Рис. 30. Схема круговорота ртути
