- •Часть I
- •Введение
- •I. Структурные формулы
- •Запомните
- •II. Изомерия
- •Запомните Свойства веществ зависят не только от их качественного и количественного состава, но и от строения молекулы.
- •III. Предельные углеводороды
- •Запомните Гомологи – вещества, имеющие сходное строение и свойства и отличающиеся друг от друга на одну или несколько групп – сн2 -
- •Общие правила номенклатуры июпак (международный союз чистой и прикладной химии)
- •2) Из природного и нефтяного попутного газов;
- •3) Из галогеналканов (синтез Вюрца)
- •Для алканов характерны реакции замещения атомов водорода на другие атомы.
- •Запомните Все предельные углеводороды горят с образованием оксида углерода (IV) и воды.
- •IV. Циклоалканы запомните
- •З Для малых циклов характерны реакции присоединения (3 или 4 атома углерода), для больших циклов – р-ции замещения. Апомните
- •V. Непредельные углеводороды.
- •Запомните Если одинаковые заместители находятся по одну сторону двойной связи, это – цис-изомер, если по разные – это транс-изомер
- •Запомните
- •З При взаимодействии галогенодородов с алкенами атом водорода присоединяется к более гидрированному атому углерода, а галоген – к менее гидрированному. Апомните
- •З Алкадиены после основы названия добавляется – «диен», а через дефис указывают атомы углерода, от которых следуют двойные связи. Апомните
- •Запомните в диенах, в которых двойные связи разделены одной простой, присоединение идет в положении 1 и 4.
- •Запомните Чтобы назвать алкин, необходимо в названии соответствующего алкана заменить суффикс «ан» на «ин»
Запомните Чтобы назвать алкин, необходимо в названии соответствующего алкана заменить суффикс «ан» на «ин»
СН = СН этин СН2 – С = СН пропин
1 2 3 4 5
СН3 – С = С – СН – СН3
│ 4 – метилиентин-2
СН3
45. Назовите вещества:
а) СН = С – СН2 – СН3 б) СН3 – С = С – СН3
в) СН = С – СН2 – СН2 – СН3 г) СН = С – СН – СН3
│
СН3
ПОЛУЧЕНИЕ АЛКИНОВ
46. а) Метановый способ (пиролиз)
15000с
СН4 + О2 → СН = СН + СО + Н2 – уравняйте
б) Дегидрогалогенирование дигалогеналканов
t,k
I этап. CH2Br – CH2Br + KOH → CH2 – CHBr + KBr + H2O
II этап. ____________________________________________________________
в) Карбидный способ
СаС2 + Н2О → Са (ОН)2 + С2Н2 ↑ - уравняйте
Химические свойства
47. Реакции присоединения
а) гидрирование ____________________________________________________
б) галогенирование ________________________________________________
в) гидрогалогенирование ____________________________________________
г) гидратация ______________________________________________________
Реакции полимеризации
__________________________________________________________________
48. Напишите уравнения возможных реакций трех углеводородов с О2, Сl2, HCl, H2O, KMnO4.
а) этан
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
б) этен
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
в) этин
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ПРОВЕРЬТЕ СВОИ ЗНАНИЯ
(АЛКИНЫ)
1. Какое из приведенных названий соответствует формуле:
СН3 – СН2
│
СН – С = С – СН – СН3
│ │
СН3 СН3
а) 2,5 – диметилгептен – 3
б) 2,5,6 – триметилгексин – 3
в) 3,6 – диметилгептин – 4
г) 1,3,6 – триметилгексин – 1
2. Осуществите цепочку превращений
СаО → СаС2 → С2Н2 → С2Н4 → (-СН2 – СН2 - )n
1._________________________________________________________________
2.________________________________________________________________
3._________________________________________________________________
4._________________________________________________________________
3. Из смеси массой 64 г, состоящей из СаС2 и SiO2 получили 11,2 л ацетилена. Сколько % карбида кальция было в исходной смеси?
а) 100%
б) 75%
в) 50%
г)25%
АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
(Арены)
Общая формула Сn H2n-6
49. Экспериментальные данные показывают, что в молекуле бензола примерно 92,3%. Плотность паров бензола по водороду равна 39. Какова формула?

Дано: Решение:
ω(с) = 92,3%
D(H2) = 39
_____________
CxHy
Изомерия и номенклатура
50. Как назвать вещества по номенклатуре ИЮПАК?
а) толуол - СН3 ________________________
б) кумол С Н
Получение бензола
51. Напишите 3 способа получения бензола:
а) Из ацетилена _________________________________________________
б) Из циклогексана _____________________________________________
в) Из гексана __________________________________________________
52. Химические свойства
Приведите примеры реакций, подтверждающие сходство бензола
- С предельными водородами:
1._____________________________________________________________
2._____________________________________________________________
- с непредельными водородами:
1._____________________________________________________________
2._____________________________________________________________
53. Осуществить превращения:
СН4 → С2Н2 → С2Н6 → С6Н5Сl
1.____________________________________________________________
2.____________________________________________________________
3.____________________________________________________________
54. Из 13,44 л ацетилена получили 12 г бензола (н.у.). Сколько это составляет % по сравнению с теоретическим?
ПРИРОДНЫЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ
55. Природный газ.
Основной компонент - метан ____________________________;
Также этан _______________; пропан ______________; бутан ____________.
Попутный нефтяной газ.
В состав входят циклопарафины, предельные и ароматические углеводороды.
Способы переработки нефти:
______________________________________________________________________________________________________________________________________________________________________________________________________
Основные фракции нефти:
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Коксохимическое производство.
Продукты пиролиза каменного угля:
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
56. Глоссарий.
Дайте определения следующим понятиям:
Органическая химия –
Изомерия –
Изомеры –
Гомологи –
Углеводороды –
Радикал –
Полимеризация –
Крекинг –
Пиролиз –
Риформинг –
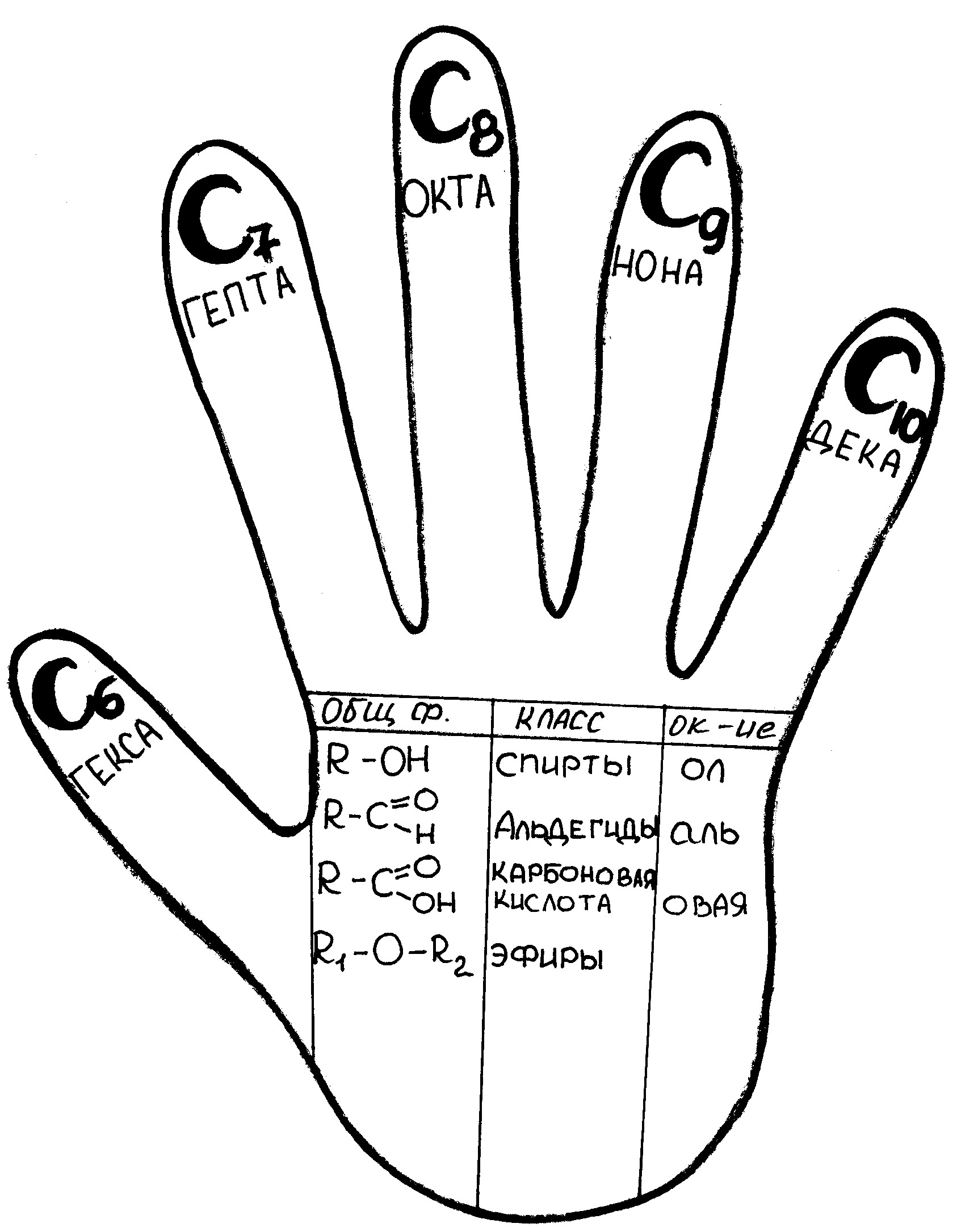
«ОРГАНИКА В ТВОИХ РУКАХ»
Приложение 1
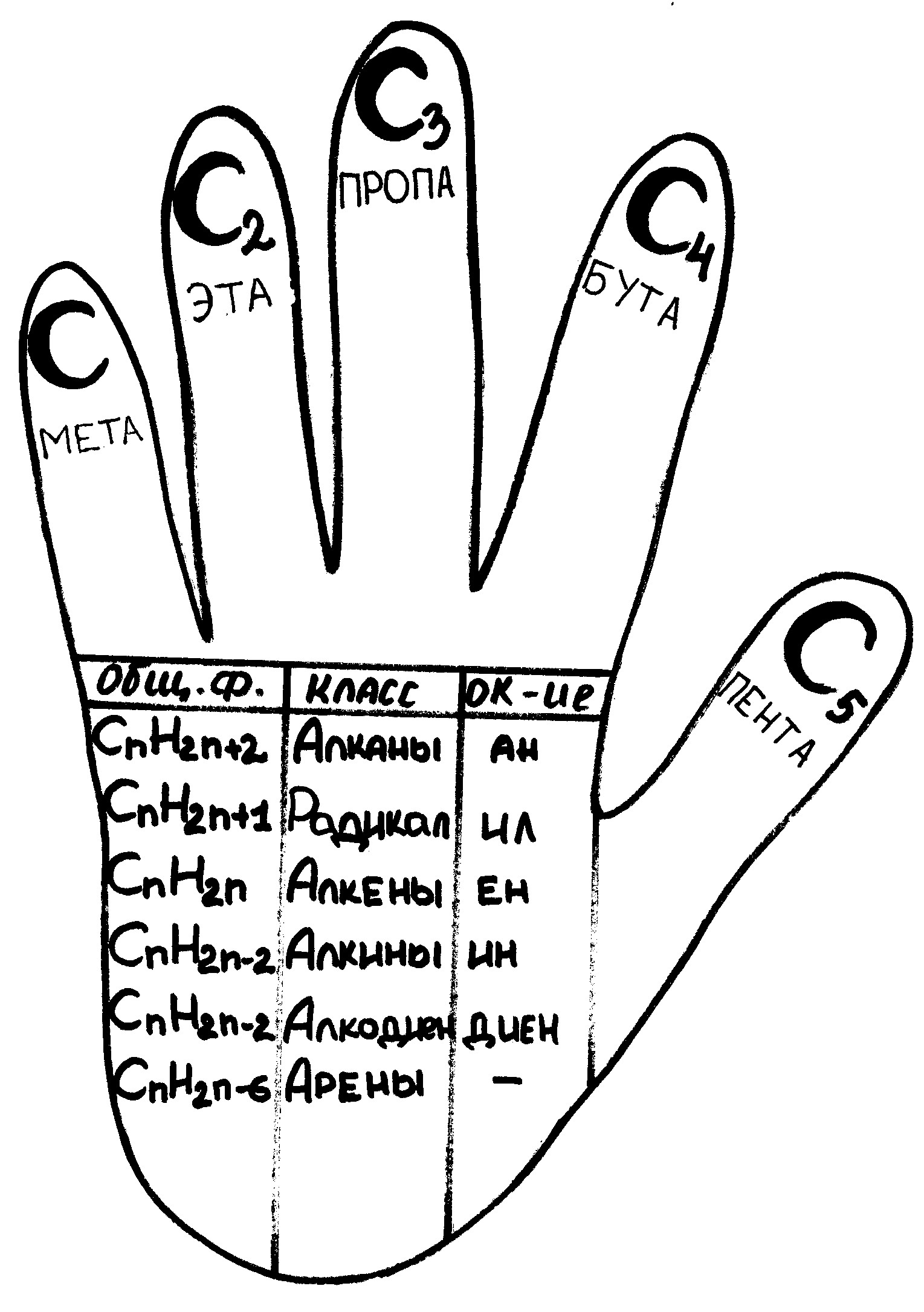
«ОРГАНИКА В ТВОИХ РУКАХ»
Приложение 2