
- •11 Класс
- •Раздел I органические соединения
- •§ 1. Предельные одноатомные спирты
- •§ 2. Глицерин
- •§ 3. Фенол
- •§ 4. Альдегиды
- •§ 5. Предельные одноосновные карбоновые кислоты
- •§ 6. Взаимосвязь между углеводородами, спиртами, альдегидами и карбоновыми кислотами
- •§ 7. Сложные эфиры
- •§ 8. Жиры. Мыло
- •§ 9. Углеводы. Глюкоза
- •§ 10. Сахароза
- •§ 12. Целлюлоза
- •§ 13. Аминокислоты. Белки
- •§ 14. Искусственные и синтетические волокна
- •§ 15. Взаимосвязь между органическими веществами, их многообразие
- •Раздел II роль химии в жизни общества
- •Альдегиды.
- •§ 16. Значение химии в создании
- •§ 17. Значение химии в решении сырьевой проблемы
- •§ 18. Значение химии в решении энергетической проблемы
- •§ 19. Значение химии в повседневной жизни
- •§ 20. Химия и экология
- •§ 21. Место химии среди наук о природе, ее значение для понимания научной картины мира
- •§ 22. Основные понятия химии
- •§ 23. Основные законы химии. Атомно-молекулярное учение
- •§ 24. Химическая связь
- •§ 25. Строение неорганических и органических веществ
- •§ 27. Классификация химических реакций
- •§ 28. Основные закономерности
- •§ 29. Генетическая связь между неорганическими и органическими веществами
- •2. Растворимость кислот, основ и солей в воде
§ 12. Целлюлоза
Состав и строение молекулы целлюлозы. Из звеньев состава —С6Н]0О5— такого же, как и у крахмала, построены цепные молекулы другого природного полимера — целлюлозы, или клетчатки.
Именно эта реакция происходит при сжигании древесины.
Как и крахмал, целлюлоза подвергается гидролизу при нагревании с разбавленными кислотами, превращаясь в глюкозу. Суммарное уравнение реакции:
![]()
У жвачных животных и термитов в органах пищеварения имеются вещества, под влиянием которых происходит гид-

• Припомните из курса биологии, каково значение клетчатки для пищеварения.
Целлюлоза подвергается частичному гидролизу при силосовании соломы, кукурузы и пр., поэтому такие продукты являются ценным кормом для сельскохозяйственных животных.
В результате нагревания древесины без доступа воздуха происходит разложение целлюлозы с образованием древесного угля, метанола и ряда других ценных кислородсодержащих соединений.
Применение целлюлозы. Целлюлоза широко применяется в виде древесины (назовите, где именно), тканей (каких?), из нее изготовляют бумагу. Все это позволяет утверждать, что современная цивилизация в значительной мере зависит от целлюлозы.
Чтобы изготовить бумагу из целлюлозы, ее необходимо прежде всего выделить из древесины. С этой целью применяют специальные вещества, растворяющие сопутствующие компоненты, но не растворяющие целлюлозу, которую можно отделить фильтрованием.
Большое количество ценных веществ образуется в результате химической переработки целлюлозы. Среди них — искусственный шелк, взрывчатые вещества, спирты.
В биомассе растений, основным компонентом которой является целлюлоза, на земном шаре запасено огромное количество энергии. Оказывается, эту энергию можно осободить, используя продукты переработки биомассы. Современная наука рассматривает ее как перспективное сырье для получения углеводородов и других ценных органических веществ. Это достигается методами биотехнологии, которая предусматривает использование ферментов (биохимических катализаторов). Полученные таким образом продукты пока имеют сравнительно высокую стоимость, но в будущем к нефти, природному газу и каменному углю как источникам органических соединений добавится еще и биомасса.
Задания для самоконтроля
Сравните состав и строение крахмала и целлюлозы. Составь те сравнительную таблицу.
Поясните практическое значение реакции гидролиза целлю лозы.
Каким путем, по вашему мнению, можно превратить клет чатку в этиловый спирт? Какие реакции происходят при этом? Со ставьте их уравнения.
Иногда можно встретить неправильное употребление терми на «углеводы» вместо «углеводороды», и наоборот. Объясните эти термины.
§ 13. Аминокислоты. Белки
Аминокислоты. Вы уже знаете, что в состав растительных и животных организмов входят представители таких классов органических соединений, как жиры и углеводы. Не менее важными для функционирования живых организмов являются белки. Это высокомолекулярные соединения, состоящие из звеньев аминокислот.
Идею о том, что аминокислоты являются «кирпичиками», из которых построены белки, впервые высказал выдающийся украинский биохимик и химик Иван Яковлевич Горбачевский.

В чем состоит отличие аминокислот от изученных вами карбоновых кислот? Карбоновые кислоты содержат функциональную карбоксильную группу —СООН, а аминокислоты — две функциональные группы: карбоксильную и аминогруппу —МН2.
Аминогруппу можно рассматривать как остаток молекулы аммиака. Если в молекуле уксусной кислоты СН3СООН один атом водорода в метильной группе заместить на аминогруппу, образуется аминоуксусная кислота

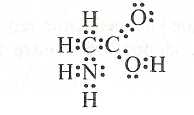

ГОРБАЧЕВСКИЙ ИВАН ЯКОВЛЕВИЧ
(1854—1942)
Украинский ученый, академик. Родился в Украине, работал в Вене, Праге, профессор, ректор Украинского университета в Праге. Научные работы в области органической химии и биохимии. Впервые синтезировал мочевую кислоту и выяснил пути ее образования в организме. Высказал мысль об аминокислотном составе белков. Внес вклад в развитие украинской научной терминологии. Автор учебников по химии на украинском языке.
Аминоуксусная кислота — простейшая из аминокислот. Среди них имеются такие, которые содержат две карбоксильные или две аминогруппы, ароматические радикалы, гидро-ксильные и серосодержащие группы. Примеры аминокислот приведены в табл. 3.
ТаЬлица _?. Некоторые представители аминокислот
Название |
Формула |
Глицин (аминоуксусная) |
|
а-Аланин (а-аминопропионовая) |
|
Глутамин |
|
Лизин |
|
Серии |
|
Цистеин |
|
По физическим свойствам аминокислоты — бесцветные кристаллические вещества с высокими температурами плавления, большинство из них хорошо растворимы в воде.
Карбоксильная и аминогруппы противоположны по химическому характеру: первая является носителем кислотных свойств, а вторая — основных. Поэтому аминокислоты принадлежат к амфотерным соединениям.
: Вспомните, в чем состоят особенности амфотерных неорганических соединеий, приведите примеры реакций.
Важнейшей особенностью аминокислот является взаимодействие молекул между собой. В реакцию вступают противоположные по функциям группы: карбоксильная группа


![]()
Связь между остатками аминокислот называется пептид-
пептидной группой.
ной связью, а группа
Строение белков. Полимерная полипептидная цепь — основа строения молекулы любого белка. Первые синтезы полипептидов осуществил немецкий ученый Э. Фишер в 1903— 1907 гг.
Каждый белок имеет набор аминокислот, соединенных в определенной, свойственной только ему последовательности. Около 20 аминокислот принимают участие в построении белковых молекул, а число соединенных в разной последователь-ности аминокислотных остатков достигает 10 . Молекулярная масса некоторых белков составляет сотни миллионов.
Строение белков очень сложное и обусловлено не только последовательностью аминокислотных остатков. Длинные цепи белковых молекул скручиваются в спирали, спирали — в клубки, которые определенным образом размещаются в пространстве (рис. 13, 14). Все это в совокупности определяет особенности каждого белка в отдельности. Из-за такой слож-
Рис. 13. Фрагмент модели полипептидной цепи
ности расшифровать структуру природных белков — чрезвычайно сложная задача.
Свойства белков. Белки очень различаются между собой по свойствам, которые зависят от наличия в их составе аминокислот с разными функциональными группами, способными вступать в характерные для них реакции.
Среди белков имеются растворимые в воде и такие, которые образуют коллоидные растворы. К числу первых при-
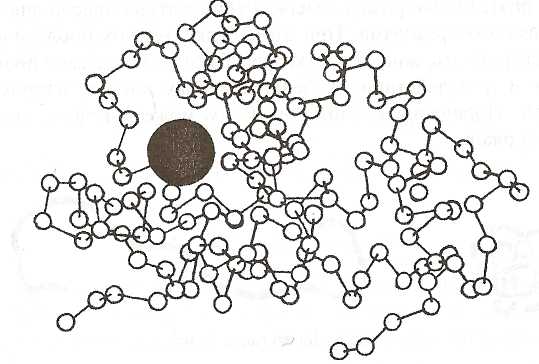
Рис. 14. Модель одной из полипептидных цепей белка гемоглобина (в центре — атом железа)

(1852—1919)
Немецкий химик, член Берлинской АН. Научные труды посвящены химии физиологически активных веществ.
Синтезировал ряд углеводов, в частности глюкозу и фруктозу. Установил, что аминокислоты связываются между собой при помощи пептидных связей, образуя полипептиды, впервые получил полипептид. Лауреат Нобелевской премии 1902 г.
надлежит белок куриного яйца. Именно с этим раствором удобно проводить опыты.
Нагреем раствор белка, наблюдая при этом, как он сворачивается, или денатурирует (от лат. пепЫигаге — лишать природных свойств). Именно этот процесс денатурации имеет место при кулинарной обработке белковых пищевых продуктов — мяса, рыбы, яиц.
С химической точки зрения денатурация — это разрушение сложной структуры белка, которое приводит к потере им биологической активности (рис. 15). Это необратимый процесс, поэтому, например, высокая температура опасна для человеческого организма. При этом белки теряют биологическую активность, живые клетки погибают. То же самое происходит и при действии на белки сильных кислот, например серной. Попадание кислоты на кожу может вызвать химический ожог.

Лабораторная работа 9 Цветные реакции белков
К раствору белка в пробирке добавьте такой же объем раствора щелочи и несколько капель слабого раствора сульфата меди(Н).
Что наблюдается? Как изменилась окраска раствора?
Если к раствору белка добавить концентрированной азотной кислоты, белок сворачивается и постепенно окрашивается в желтый цвет.
Взаимодействие белков с концентрированной азотной кислотой и раствором гидроксида меди(П) — это так называемые цветные реакции белков, используемые для их аналитического определения. При помощи первой определяется наличие бензольных колец в структуре белка, а вторая позволяет определить наличие пептидных связей.
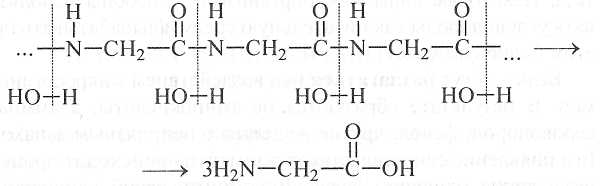
Важным химическим свойством белков является их способность к гидролизу. Под воздействием кислот, щелочей или ферментов (в случае живого организма) происходит расщепление полимерной белковой молекулы на аминокислоты. Гидролиз — процесс, обратный образованию полипептидной цепи. При гидролизе молекулы воды присоединяются по месту пептидных связей, последние разрушаются, вместо пептидных групп образуются карбоксильные и аминогруппы. Таким образом белок расщепляется на отдельные аминокислоты, из которых он состоит:
Трудно переоценить биологическое значение этого процесса. Белки, входящие в состав пищи, прежде всего расщепляются (гидролизируют) до аминокислот под воздействием веществ, содержащихся в пищеварительном тракте, затем аминокислоты всасываются в кровь и уже ею переносятся в пе-
чень, где организм синтезирует белки, характерные именно для него.
Белки являются основным строительным материалом животных организмов, точнее их клеток. Мышцы, гемоглобин крови, волосы, кожа, ферменты, имеют белковую природу.
Если растения синтезируют аминокислоты из веществ, которыми питаются, то животные и человек лишены природой такой способности. Для нормального функционирования они должны постоянно пополнять запас аминокислот преимущественно за счет белков пищи, то есть получать их в готовом виде. Это особенно важно для молодого организма, который растет и развивается. Поэтому пища должна содержать достаточное количество белков. Наиболее богаты белками мясо, рыба, молоко, сыр, яйца, орехи, бобовые. Больным, ослабленным людям иногда вводят аминокислоты как лекарство, тем самым облегчается их усвоение и поддерживаются силы организма.
• Припомните из курса биологии человека, что такое заменимые и незаменимые аминокислоты.
Для откорма сельскохозяйственных животных используют синтетические аминокислоты. Белковую массу можно получить также из углеводородов нефти, природного газа или отходов переработки древесины путем микробиологического синтеза. Некоторые виды микроорганизмов способны использовать углеводороды как питательную среду и вырабатывать при этом белковую массу.
Белки могут разлагаться под воздействием микроорганизмов. В результате образуются не аминокислоты, а аммиак, сероводород, фенол, другие вещества с неприятным запахом. Его появление свидетельствует о том, что происходит процесс разложения (гниения) белка. Вспомните, какой неприятный запах имеют протухшее яйцо, испорченные мясо или рыба. Замораживание продуктов, маринование, копчение понижают активность микроорганизмов или даже уничтожают их, процесс разложения замедляется, и продукты сохраняются дольше.
Задания для самоконтроля
Поясните термин «аминокислоты». Назовите функциональ ные группы в молекулах этих соединений.
Глутамин добавляют к пищевым концентратам для улучше ния их вкуса. Назовите функциональные группы, которые входят в состав молекулы этого соединения.
Благодаря каким свойствам аминокислот образуются поли пептиды?
Чем обусловлено огромное разнообразие белков?
Охарактеризуйте термическую устойчивость белков.
Чем отличаются процессы гидролиза и разложения белков?
Составьте формулы трипептидов, образованных тремя лю быми аминокислотами, формулы которых приведены в табл. 3.
Белки принадлежат к биополимерам. Можно ли так назвать крахмал? Клетчатку? Глюкозу?
83*. Охарактеризуйте значение процесса гидролиза белков, жиров, углеводов для функционирования организма.
Можно ли полностью заменить белковую пищу на углевод ную? Почему?
Белки горят с образованием характерного запаха. Убедитесь в этом, осторожно сжигая перышко, шерстяную нитку. Сравните запах с запахом горящей хлопковой нитки.
Зная свойства белков, объясните, почему посуду из-под мо лочных продуктов следует мыть сначала холодной, а затем горячей водой, а не наоборот.
