- •Органічна хімія Опорні лекції Нітрогенвмісні органічні сполуки
- •Аміни жирного ряду
- •2. Взаємодія амінів з нітритною кислотою
- •Окислення амінів
- •Ароматичні аміни
- •*Реакції амінів як нуклеофільних реагентів
- •Дія нітритної кислоти
- •Окислення ароматичних амінів
- •Окремі представники амінів
- •* Ароматичні діазо- і азосполуки
- •Амінокислоти
- •Утворення солей з кислотами
- •Реакція декарбоксилювання
- •Ацилювання амінокислот
- •Відношення різних амінокислот до нагрівання
- •Утворення пептидів
Амфотерні властивості (взаємодія з мінеральними кислотами та основами з утворенням солей).
Утворення солей з кислотами
NH2 – CH2 – COOH + НСІ → [+NH3 – CH2 – COOH] CI- (хлорид гліцину)
Утворення солей з основами: звичайних солей з лугами та внутрішньо комплексних солей з купрумом (ІІ) інтенсивно-синього кольору:
натрієва сіль амінокислоти

внутрішньокомплексна сіль амінокислоти
Утворення естерів (взаємодія зі спиртами):
![]()
а мінооцтова
кислота
етанол етилгліциноат (етиловий естер
гліцину)
мінооцтова
кислота
етанол етилгліциноат (етиловий естер
гліцину)
Реакцію використовують для розділення і виділення амінокислот із білкових гідролізатів.
Утворення хлорангідридів відбувається при взаємодії амінокислот з пентахлоридом фосфору РСІ5, утворюються хлорангідриди амінокислот. Вони нестійкі і існують тільки у вигляді солей:
![]()
Реакція декарбоксилювання
![]()
аланін етиламін
Ферментативна реакція, що відбувається в клітинах живих організмів під впливом ферментів декарбоксилаз.
Дезамінування амінокислот відбувається під впливом нітритної кислоти або ферментів дезамінази:
![]()
гліцин нітритна кислота гліколева кислота
С Н3
– СНNH2
– COOH + H2O
CH3
– CHOH – COOH + NH3
Н3
– СНNH2
– COOH + H2O
CH3
– CHOH – COOH + NH3
аланін лактатна (молочна) кислота
Окислювальне дезамінування відбувається під впливом окислювачів (гіпохлорити, хлорамін Т, персульфати), утворюються кетокислоти:

Реакція окислювального дезамінування відбувається в організмах людини і тварин під впливом специфічних ферментів.
*Для якісного і кількісного визначення амінокислот використовується нінгідрин. При нагріванні з амінокислотою відбувається відновлення нінгідрину до дикетооксигідриндену, а амінокислота розщеплюється на альдегід, вуглекислий газ і аміак:
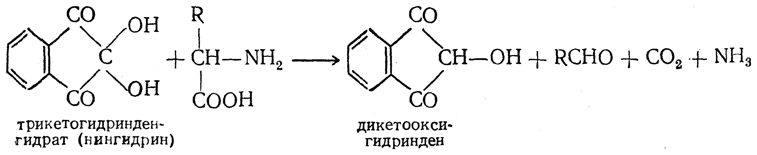
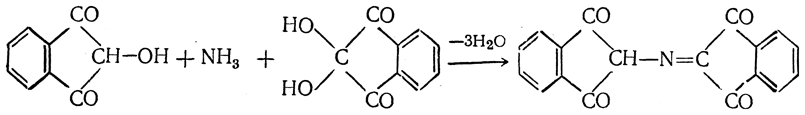
Внаслідок конденсації аміаку з молекулами нінгідрону та дикетооксигідриндену відбувається утворення амонійної солі, що забарвлена в синьо-фіолетовий колір:
|
Сполука забарвлена у синьо-фіолетовий колір завдяки наявності спряжених зв’язків. За інтенсивністю забарвлення можна кількісно визначати вміст амінокислоти в розчині. Аналогічне забарвлення з нінгідроном спостерігається також з пептидами, первинними і вторинними амінами. |
Ацилювання амінокислот
Амінокислоти реагують з хлорангідридами та ангідридами кислот з утворенням N-ацильованих похідних. Реакція відбувається до кінця тільки у водно-лужних або неводних середовищах так як у взаємодію вступає амінна група:
![]()
ацетилхлорид гліцин N-ацетилгліцин
N-Ацильовані похідні амінокислот використовуються при синтезі пептидів.
Окремі ацильовані амінокислоти здатні знешкоджувати отруйні речовини, які всмоктуються у кров з кишківника. Так, наприклад, отруйна бензойна кислота зв’язується з гліцином та видаляється з організму з сечею в формі гіпурової кислоти:
![]()
бензойна кислота гліцин гіпюрова кислота
Відношення різних амінокислот до нагрівання
утворення лактамів при нагріванні γ-, δ-, ε-амінокислот:
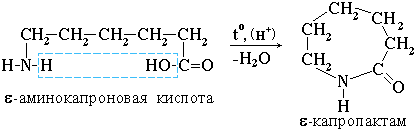
утворення ненасичених карбонових кислот при нагріванні β-амінокислот:
СН3 – СН – CH2 – COOH → CH3 – CH = CH – COOH + NH3
│
NH2 β-аміномасляна кислота кротонова кислота