
- •Идеальный газ, определение и его свойства
- •Термодинамическая система, термодинамический процесс, параметры идеального газа.
- •4Внутренняя энергия идеального газа. Параметры состояния
- •5.Работа газа. Параметр процесса.
- •6.Теплоемкость газа
- •7.Газовые смеси
- •Выражение 1-ого закона термодинамики для различных процессов.
- •Круговые циклы. Термодин. И холодильный коэф.
- •11.Цикл Карно. Теорема Карно.
- •12. Реальный газ. Парообразование в координатах pv.Теплота парообразования. Степень сухости пара.
- •13.Влажный воздух. Его св-ва.
- •15. Температурного поле тела. Температурный градиент.
- •16. Теплопроводность. Закон Фурье.
- •17.Теплопроводность плоской стенки. Основное ур-ние теплопроводности.
- •18.Конвективный теплообмен.Ур-ние Ньютона-Рихмана. Коэф.Теплоотдачи.
- •19. Определение коэф. Теплоотдачи с использованием критериальных ур-ний.
- •20.Лучистый теплообмен. Ур-ние Стефана-Больцмана.
- •21. Закон Кирхгофа, Ламберта
- •22. Теплопередача. Уравнение и коэффициент теплопередачи для плоской стенки
- •24. Микроклимат помещений
- •23. Теплообменные аппараты. Определение поверхности нагрева рекуперативных теплообменников
- •25.Сопротивление теплопередачи.
- •26. Теплоустойчивость ограждений. Коэффициент теплоусвоения s. Величина тепловой инерции d.
- •27.Воздухопроницаемость ограждений. Сопротивление воздухопроницаемости
- •29. Определение тепловых потерь здания по укрупненным измерителям.
- •30. Системы отопления
- •28.Определение тепловых потерь чз ограждения
- •31.Системы водяного отопления.
- •32.Гравитационное давление.
- •33. Опред. Циркуляционное давление в однотрубной системе водяного отопления.
- •34.Трубопроводы систем центрального отопления, их соединения.
- •35.Расширительный бак.
- •36.Воздухоудаление.
- •37. Свойство пара как теплоносителя:
- •38.Нагревательные приборы системцентр. Отопления.
- •39.Размещение от-ых приборов.
- •40. Выбор типа нагревательных приборов и определение их поверхности нагрева.
- •42.Регулировка теплоотдачи нагр. Приборов.
- •43. Топливо.
- •44. Горение топлива
- •45. Способы сжигания топлива. Виды топочных устр., их характер.
- •46. Котельная установка.
- •47. Централизованное теплоснабжение. Схема тэц.Тепловые сети.
- •48.Присоединение местных сист. Отопления к тепл. Сетям
- •49. Расчет и подбор водоструйного элеватора.
- •50. Назначение и классификация систем вентиляции, воздухообмен, способы его определения.
- •56. Вентиляторы.
4Внутренняя энергия идеального газа. Параметры состояния
Внутренняя энергия - суммарный запас кинетической энергии газа, обусловленный поступательным, вращательным движением, энергией между атомами молекул, энергией межмолекулярного взаимодействия.
Кинетическая энергия поступательного и вращательного движения молекул зависят только от t. Если принять, что влияние сил взаимодействия между молекулами равно нулю, т. е. рассматривать идеальный газ, то величина внутренней энергии: u = f(t).
Изменение внутренней энергии рабочего тела не зависит от его промежуточных состояний и определяется полностью величиной его начальных (u1) и конечных (u2) параметров:
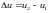 (Дж/кг)
(Дж/кг)
Во всех термодинамических процессах, если v =const т. е. рабочее тело не расширяется и не совершает работы, сообщаемая ему теплоту q=сV (Т2- Т1) идет только на увеличение его внутр. энергии
U2-U1 = Cv(T2-T1).
Для ∞ малого изменения состояния du=cVdt внутренняя энергия тела является параметром состояния.
5.Работа газа. Параметр процесса.
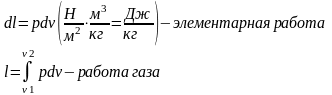
Принято считать работу расширения “+”, а сжатия “-“
Работа, в отличие от теплоты, представляет собой макрофизически упорядоченную форму передачи энергии путем взаимного механического воздействия тел. В этом и заключается качественное отличие понятий «работа» и «теплота». По существу, понятие теплоты близко к понятию работы. Различие между теплотой и работой состоит лишь в том, что они являются разными формами передачи энергии. Теплота представляет собой форму передачи энергии, которая определяется непосредственным контактом между телами, либо лучистым переносом энергии. Теплота не может самопроизвольно превращаться в работу. Этот процесс сопровождается другими энергетическими изменениями в окружающей среде или в рабочем теле. Особенность перехода теплоты состоит в том, что этот процесс носит односторонний характер - теплота переходит самопроизвольно только от тела с более высокой t к телу с меньшей t. А обратный переход теплоты от тела с меньшей t к телу с большей t может быть лишь принудительным (тепловые машины).
6.Теплоемкость газа
Теплоемкость тела – кол-во теплоты, необходимое для нагрева тела на 1°. Теплоемкость измеряется в Дж/К, допускается единица Дж/°С; в технических расчётах — кДж/К. Если теплоемкость относят к какой-либо единице количества вещества (кг, м3, кмоль), то такая теплоемкость - удельная и ее единица соответственно будет кДж/(кг·К), кДж/(м3·К) и кДж/(кмоль·К). В зависимости от выбранной количественной единицы вещества различают массовую с, объемную с' и кило-мольную µс теплоемкости. Между ними имеют место следующие соотношения: с = µс/22,41; с' = ρс. Теплоёмкость существенным образом зависит от характера процесса. Поэтому значения теплоемкости в различных процессах различны.
Истинная
теплоемкость при данной температуре
представляет собой предел, к которому
стремится теплоемкость, средняя для
прилегающего температурного
интервала, когда этот интервал стремится
к нулю.
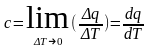
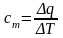 (средняя
теплоёмкость)
(средняя
теплоёмкость)
В соответствии с определениями истинной и средней теплоемкости можно написать следующие выражения для теплоты, сообщенной 1 кг газа:
а) при бесконечно малом изменении t газа, кДж/кг:dq = cdt
б) при изменении t газа от t1 до t2, кДж/кг: q=cm(t2-t1).
Для нагревания массы Q (кг) от t t1 до t2 потребуется теплота Q (кДж): Q=G cm(t2-t1)
Особое значение для нагревания (или охлаждения) газа имеют условия, при которых происходит процесс подвода (или отвода) теплоты. В теплотехнике наиболее важным является:
нагревание
(или охлаждение) при постоянном объеме
- изохорный
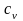 ;
;
нагревание
(или охлаждение) при постоянном давлении
– изобарный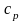 .
.
Связь
между этими теплоемкостями устанавливается
уравнением Майера:
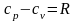
При нагревании 1 кг газа на 1 °С при постоянном объеме сообщаемая газу теплота — теплоемкость cv — расходуется только на увеличение внутренней энергии газа, так как внешняя работа не совершается.
При нагревании же 1 кг газа на 1 °С при постоянном давлении объем газа возрастает и сообщаемую газу теплоту — теплоемкость ср — расходуют не только на увеличение внутренней энергии газа, но и на совершение работы расширения. Поэтому теплоемкость cp всегда больше, чем теплоемкость cv на величину работы, совершаемой 1 кг газа при нагревании его на 1 °С при постоянном давлении.
