
- •1.Строение кристаллических тел (по типу связей, по симметрии кристаллов, элементарная кристаллическая ячейка, кристаллографические плоскости и направления). Дефекты строения кристаллических тел.
- •2. Диффузия в металлах и сплавах.
- •4. Механизм кристаллизации. Связь между величиной зерна, скоростью зарождения и роста кристаллов, степенью переохлаждения. Строение слитка. Ликвация.
- •6. Механические свойства материалов (σв, σ0,2 ,σ 0,01, σпц, φ,ε ,ν , е, закон Гука).
- •3. Энергетические условия кристаллизации (первый закон термодинамики, равновесная температура кристаллизации, самопроизвольная и гетерогенная кристаллизация). Полиморфные превращения.
- •5. Упругая и пластическая деформации. Разрушение материалов, влияние концентраторов напряжения. Виды разрушения твердых тел.
- •7. Твёрдость. Определение твёрдости по Бринеллю
- •8. Определение твёрдости по Роквеллу и Виккерсу
- •9. Определение ударной вязкости и предела выносливости.
- •10. Кристаллизация металлических сплавов. Фазы в сплавах.
- •11. Диаграмма состояния сплавов и принципы её построения. Правило фаз и правило отрезков.
- •12. Диаграмма состояния сплавов с неограниченной растворимостью
- •14. Диаграмма состояния сплавов с ограниченной растворимостью и
- •15.Диаграмма состояния сплавов, компоненты которых образуют устойчивые химические соединения
- •17. Связь между свойствами сплавов и диаграм состояния
- •2 2. Структурные превращения в стали при нагреве (наследственно мелкозернистые и крупнозернистые стали).Ферит растворяется в аустените
- •23. Структурные превращения в стали при охлаждении (диаграммы изотермического распада аустенита, образующиеся структуры, их особенности, твердость).
- •27. Термомеханическая обработка сталей (втмо, нтмо, особенности техпроцессов, влияние на свойства сталей).
- •24. Отжиг (виды, технологические режимы, область их применения). Нормализация.
- •26. Отпуск закаленных сталей. Структурные превращения, температурные диапазоны и виды отпуска, образующиеся структуры, области применения. Улучшение.
- •25. Закалка. Критическая скорость закалки. Прокаливаемость. Виды закалки и их применение. Дефекты закалки, методы их устранения и предотвращения.
- •28.Цементация сталей (цель, цементуемые стали, виды цементации, рабочая среда и
- •29.Азотирование сталей (азотируемые стали, глубина слоя, технологические режи-
17. Связь между свойствами сплавов и диаграм состояния
Для основных видов диаграмм существует зависимость, приве-
денная на рис. 3.8.
1. При образовании твердых растворов свойства сплавов изменя-
ются по криволинейной зависимости, причем многие из них могут су-
щественно превосходить свойства исходных компонентов (в первую
очередь электросопротивление). Поэтому распад твердых растворов на
две и более фазы приводит к увеличению электропроводности.
2. При образовании механических смесей свойства сплавов из-
меняются по линейному закону (аддитивно). Значения свойств нахо-
дятся в интервале между свойствами чистых компонентов.
3. В сплавах с ограниченной растворимостью при концентраци-
ях, cоответствующих однофазному твердому раствору, изменяются свойства по криволинейному закону, а в двухфазной области – по ли-
нейному. Крайние точки на прямой соответствуют свойствам пре-
дельно насыщенных твердых растворов.
4. При образовании химических соединений на диаграмме кон-
центрация–свойства при соответствующей концентрации наблюдает-
ся перелом, т. к. химические соединения обладают индивидуальными
свойствами, отличными от свойств исходных составляющих Сплавы, имеющие структуру однофазных твердых рас-
творов, имеют низкие литейные свойства (низкая жидкотекучесть,
обладают склонностью к образованию рассеянной пористости и тре-
щин), а также трудно обрабатываются резанием. Однако эти сплавы
хорошо обрабатываются методами пластического деформирования
(ковка, штамповка, прокатка и т. д.). Пластичность сплавов сильно
снижается при появлении в структуре эвтектики. Эвтектические спла-
75
вы обладают наилучшей жидкотекучестью, усадка у них проявляется
в виде концентрированной раковины.
------------------------------------------------------------------------------------
18.Диаграмма состояния Fe-FeС (компоненты, фазы, основные превращения и
структурный состав сплавов).. Компоненты железо и углерод. Железо металл серебристо-белого цвета с температурой плавления 1539 град. Углерод – неметаллический элемент с температурой сублимации 3500 град. Имеет плотность 2,5 г/см3 может существовать в в двух модификациях: в виде графита и алмаза. Углерод растворим в железе в жидком и твердом агрегатном состоянии и может вступать с ним в химическое взаимодействие, образуя карбид железа.Фазы. жидкий расплав, твердые растворы – феррит и аустенит, химическое соединение Fe3C (цементит) и свободный углерод в виде графита.Феррит (Ф) – твердый раствор углерода в железе с объемно - центрированной кубической решеткой. Предельная растворимость углерода в низкотемпературной -модификации железа при температуре 727 °С составляет 0,02 %, а в высокотемпературной области в -Fe при температуре 1499 ºС – 0,1 %. Феррит – мягкая, пластичная составляющая со следующими механическими свойствами при комнатной температуре: в = 300 МПа, 0,2 = 120 МПа, = 40 %, = 70 %, КСU = 2,5 МДж/м2, твердость 800…1000 НВ.Аустенит (А) – твердый раствор углерода в железе с гранецентрированной кубической решеткой (-Fe). Максимальная растворимость углерода в -Fe составляет 2,14 % при температуре 1147 °С. Аустенит пластичен, прочнее феррита, твердость его при нормальных физических условиях составляет 1600…2000 НВ.Цементит (Ц) – химическое соединение Fe3C (карбид железа), со сложной ромбической решеткой с плотной упаковкой атомов, содержащее 6,67 % С. Цементит хрупок, малопластичен, имеет высокую твердость до 8000 НВТемпература плавления цементита 1260 °С. Цементит является метостабильной фазой, при нагреве до определенных температур он может распадаться с образованием углерода в свободном состоянии в виде графита.Графит (Г) – углерод в свободном состоянии с гексагональной слоистой кристаллической решеткой, с расстояниями между атомами в плоскости 0,142 нм, а между плоскостями – 0,340 нм. Графит электропроводен, мягок и имеет низкую прочность.
Первичная кристаллизация идет в областях между линиями ликвидус (ABCD) и солидус (AHJECF). Вторичная кристаллизация в твердом агрегатном состоянии является следствием полиморфного превращения железа и изменения растворимости углерода в железе с изменением температуры. На линии ликвидус начинается кристаллизация из расплава соответственно на участке АВ – феррита (Ф) , на участке ВС – аустенита (А) и на участке СD – цементита первичного (ЦI). На линиях АН
и JЕ завершается кристаллизация Ф и аустенита из жидкой фазы
Для диаграммы Fe–Fe3C характерны три изотермических превращения:
– перитектическое на линии HJВ при температуре 1499 °С
ФН
+
ЖB
![]() АJ;
АJ;
– эвтектическое на линии ECF при температуре 1147 °С
ЖC АE + ЦF;
– эвтектоидное на линии PSK при температуре 727 °С
АS ФP + ЦK.
Эвтектическая смесь аустенита и цементита называется ледебуритом (Л), а эвтектоидная смесь феррита и цементита вторичного перлитом (П). Перлит чаще всего имеет пластинчатое строение и обладает высокими механическими свойствами:
в = 800…900 МПа, 0,2 = 450 МПа, 16%, твердость 1800…2200 НВ.
Ледебурит
имеет сотовое или пластинчатое строение.
Сотовая структура образуется при
медленном охлаждении и представляет
собой пластины цементита, переплетенные
кристаллами аустенита. Большое количество
цементита, присутствующего в ледебурите,
обеспечивает его большую твердость,
порядка 6000 НВ, и хрупкость, что затрудняет
механическую обработку сплавов с
ледебуритной с труктурой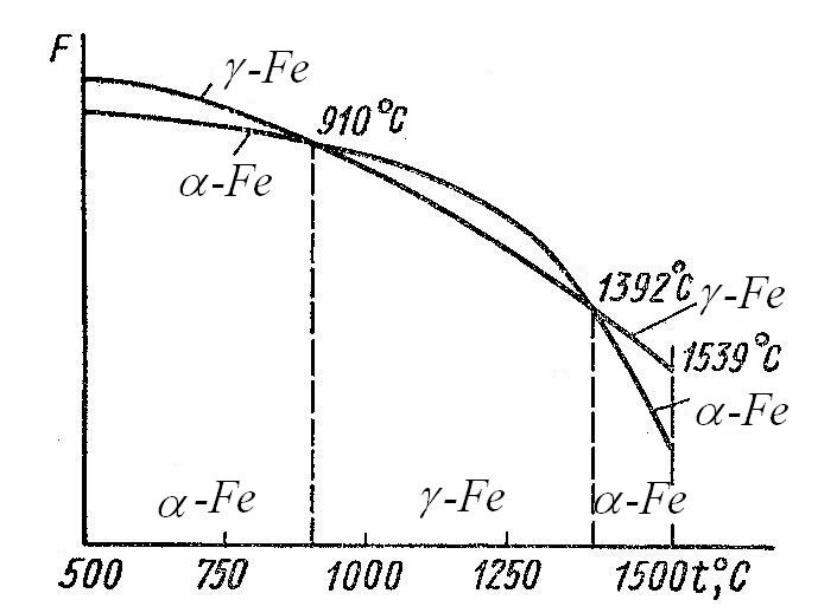
-------------------------------------------------------------------------------------------
19. Диаграмма состояния Fe-С (компоненты, фазы, основные превращения и структурный состав сплавов). График см рис 19. Компоненты: железо, графит.
Железа: Тпл=1539 ρ=7,58 г/см3 в диапазоне 1539-1392 град. И 911град железо имеет ОЦК решетку, в диапазоне 1392-911 град – ГЦК. Железо – пластичный компонент с прочностью 300МПа, твердость 80НВ, пластичность δ ̴ 40 – 50%
Углерод – неметаллический элемент с температурой сублимации 3500 град. Имеет плотность 2,5 г/см3. Углерод может взаимодействовать с химическим железом образуя цементит и может растворяться в железе образуя твердый раствор внедрения.
Фазы.
1 жидкая фаза – расплав (ж)
2 феррит (Ф) – твердый раствор внедрения углерода в железо с ОЦК решёткой образуется δФ, αФ. Является пластической фазой твердость 80 – 100 НВ σв=300-350МПа δ ̴ 40%
3 Аустенит (А) твердый раствор С в γ-Feимеет твердость 150-200 НВ предел прочности 550-700 МПа
4 Цементит (Ц) – химическое соединение Fe3C имеет высокую твердость = 800МПа 6,67%С, жесткий, хрупкий, практически отсутствует пластичность.
5 Графит (Г) – высокая теплопроводность но низкая прочность. В зависимости от состояния С различают 2 вида диаграммы: метостабильная диаграмма (Fe – Fe3C) и стабильная диаграмма Fe-С.

Точка на диаграмме Температура, °С Концентрация
углерода, %
А 1539 0
H 1499 0,1
J 1499 0,16
B 1499 0,51
N 1392 0
D 1260 6,69
E 1147 2,14
C 1147 4,3
F 1147 6,67
G 911 0
P 727 0,02
S 727 0,8
K 727 6,67
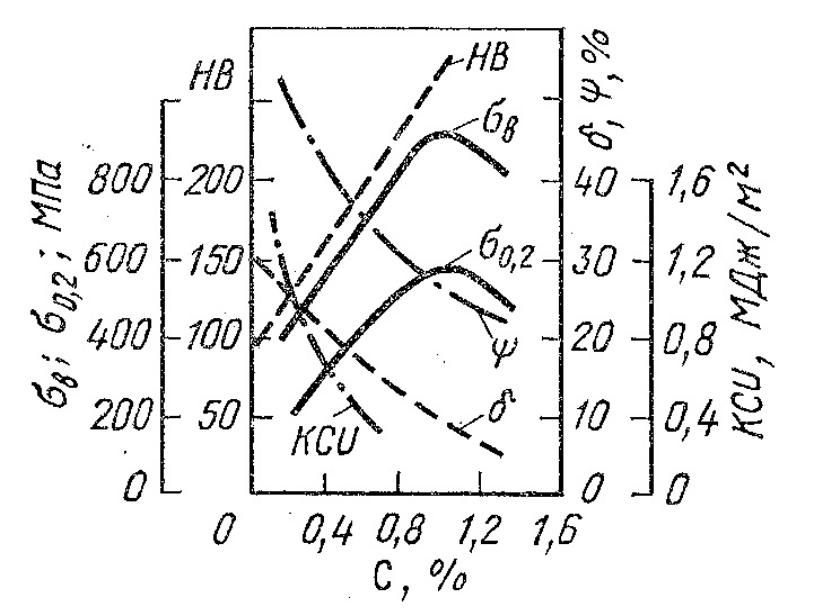
20. Влияние количества углерода и примесей на свойства сталей. График см рис 20
Пределы прочности и текучести возрастают при увеличении количества углерода в стали до 1,0 %, после чего начинается их снижение. Причиной этому является образование цементной сетки вокруг зерен перлита. Пластичность и ударная вязкость с увеличением содержания углерода снижаются. Кремний и марганец, соединяясь с кислородом оксида железа, в виде оксидов уходят в шлак. Кремний дегазирует сталь, увеличивая плотность отливки, растворяясь в феррите повышает предел текучести стали, снижает ударную вязкость, способность к вытяжке и холодной высадке. Количество кремния допускается не более 0,35…0,40 %.
Марганец взаимодействует с серой образуя сульфиды марганца, выделяющегося в виде отдельных частиц. Повышает предел прочности, незначительно предел текучести но снижает пластичность. Обычно в углеродистых сталях содержится марганца до 0,50…0,80 %.
Сера, взаимодействуя с железом, образует сульфид железа FeS. Сульфидные включения существенно снижают механические свойства, особенно ударную вязкость и пластичность, а также предел выносливости сталей, ухудшают их коррозийную стойкость и свариваемость.
Содержание серы в сталях строго ограничено и допускается не более 0,060 % для сталей обыкновенного качества и не более 0,035 % для качественных сталей.
Фосфор, соединяясь с железом, образует фосфиды железа Fe3P,
которые располагаются по границам зерен, повышая порог хладноломкости и снижая коррозийную стойкость сталей. Фосфор, растворяясь в феррите и аустените, искажает кристаллическую решетку, понижает пластичность, ударную вязкость, увеличивая предел
прочности и предел текучести сталей. В сталях допускается количество фосфора не более 0,045 %. Чем меньше фосфора и серы в стали, тем выше ее качество.
Кислород и азот охрупчивают сталь, снижают пластичность, предел прочности, износостойкость.
Водород охрупчивает сталь, способствует образованию флокенов (трещин овальной формы), холодных трещин при сварке.
------------------------------------------------------------------------------
21. Влияние легирующих элементов на структуру и свойства сталей (на температурные области полимерных превращений, карбидообразующие и не образующие карбидов легирующие элементы и их влияние на свойства сталей).
По влиянию на температурную область существования полиморфных модификаций железа легирующие элементы можно разделить на две группы. К первой группе относятся элементы, понижающие точку А3 и повышающие точку А4. К таким элементам относятся: никель, марганец, медь, кобальт, азот. На диаграмме железолегирующий элемент область существования -Fe уменьшается, а -Fe – увеличивается (рис 21.а). стали состава правее точки х2 наз аустенитными они явл однофазными сост из твердого раствора С и лигирующих элементов в γ- Fe.
Стали состава х1 и х2 являются полуаустенитными и испытывают частичные превращения.
Ко второй группе относятся легирующие элементы, понижающие точку А4 и повышающие точку А3. В эту группу входят: хром, вольфрам, молибден, ванадий, кремний, алюминий и др. При определенной концентрации легирующего элемента интервалы А3 и А4 сливаются и область существования -фазы замыкается. (рис 21,б)
При содержании легирующего элемента больше «y» образуются
однофазные сплавы, относящиеся к классу ферритных, состоящих из
твердого раствора легирующего элемента в -Fe. Точка «у» для
большинства легирующих элементов соответствует 1…1,5 % и лишь
для хрома составляет около 12 %. Сплавы частично претерпевшие переход называются полуферритными.
Лигированные элементы увеличивают σпроч не влияя на пластичность кроме марганца и кремния при содержании их 2.5%. Наибольшие упругие свойства при лигировании марганцем кремнием никелем.
Растворимость в аустените повышает предел прочности но снижает предел текучести повышается прокаливаемость повышается устойчивость аустенита. Рис 21.1.
По отношению к легирующим элементам относятся:
1 графитизирующие Cu, Ni, Co, Al, Si
2 карбидообразующие Mn, Cr, W, V, Ti, Nb.
Mn может растворятся в аустените в неограниченном количестве.
При содержании Cr от 3 до 10% образуются карбиды хрома, имеющие гексагональную решетку со структурной формулой Cr7C3 (твердостью 16000…18000 HV), а при более высоком содержании хрома – кубические карбиды типа Cr23C6 (твердостью 10000…11000 HV).
Карбиды типа М3С легко растворимы в аустените. Более трудно растворимы карбиды типа М7С3, М23С6 и М6С, для растворения которых требуются более высокие температуры и длительности выдержки.
Сильные карбидообразователи Мо, W, V, Nb, Ti образуют с углеродом фазы внедрения типа МС, а при определенных условиях – М2С. Эти фазы практически нерастворимы в аустените. Для распада и растворения TiC, NbC, WC необходим нагрев до температуры 1300 С.
При большом содержании лигирующих элементов могут образовываться интерметалидные элементы. Лигирующие элементы влияют на точку эвтектоидного превращения. Они уменьшают количество углерода в эвтектоиде особенно титан, молибден и большинство из них увеличивает температуру эвтектоидного превращения особенно титан молибден ванадий углерод.
----------------------------------------------------------------------------
