
- •1. Загальна характеристика неметалічних елементів. Неметали як прості речовини (лекція-бесіда).
- •1. Загальні хімічні властивості
- •1. Розчинність
- •2. Хімічні властивості
- •3. Поширення в природі
- •Хімічні властивості [ред.]
- •1. Фізичні властивості
- •2. Хімічні властивості
- •Алюміній: будова атома, поширення в природі. Фізичні і хімічні властивості алюмінію. Застосування алюмінію
- •Алюміній оксид (глинозем)
- •Алюміній гідроксид
- •Гомологи метану
- •Ненасичені вуглеводні (алкени, алкіни)
- •Ізомерія алкенів і алкінів
- •Етилен й ацетилен
- •Властивості природного газу [ред.]
- •Фізичні властивості [ред.]
- •Отруйні властивості природного газу [ред.]
- •Застосування [ред.]
- •Застосування[ред.]
- •Оксигеновмісні органічні сполуки Насичені одноатомні спирти
- •Застосування спиртів.
- •Багатоатомні спирти
- •Добування фенолу.
- •Хімічні властивості фенолу.
- •Застосування альдегідів.
- •Насичені одноосновні карбонові кислоти
- •Фізичні властивості карбонових кислот.
- •Біологічна дія.
- •Добування карбонових кислот.
- •Хімічні властивості карбонових кислот (на прикладі оцтової кислоти).
- •Застосування карбонових кислот.
- •Естери. Реакція естерифікації Естери
- •Вуглеводи
- •Глюкоза
- •Крохмаль і целюлоза
- •Нітрогеновмісні органічні сполуки Амінокислоти
Застосування спиртів.
Етанол застосовують для добування синтетичного каучуку, пластмас, різних органічних речовин: діетилового естеру, барвників, оцтової кислоти. Його використовують як розчинник для виготовлення парфумів, одеколонів, ліків, лаків і т. д. Етанол у суміші з бензином можна використовувати як пальне для двигунів внутрішнього згоряння. Метанол застосовують як розчинник або сировину для одержання формальдегіду, деяких барвників, фотореактивів, фармацевтичних препаратів.
Багатоатомні спирти
Багатоатомними називаються
спирти, у молекулах яких два або більше
атомів Гідрогену заміщені на
гідроксигрупи.
Якщо
в молекулі спирту містяться три
гідроксигрупи, він належить
до триатомнихспиртів.
У назві такого багатоатомного спирту
присутній суфікс -тріол.
Загальна
формула триатомних спиртів ![]() .
Наприклад, формула пропантріолу-1,2,3
(гліцерину):
.
Наприклад, формула пропантріолу-1,2,3
(гліцерину):
![]() Фізичні
властивості гліцерину. Безбарвна,
в’язка, гігроскопічна рідина, солодка
на смак. Змішується з водою в будь-яких
співвідношеннях. Температура плавлення
—
Фізичні
властивості гліцерину. Безбарвна,
в’язка, гігроскопічна рідина, солодка
на смак. Змішується з водою в будь-яких
співвідношеннях. Температура плавлення
— ![]() ,
кипіння —
,
кипіння — ![]() .
Добування
гліцерину.
1)
Із жирів.
2)
Із галогенопохідних:
.
Добування
гліцерину.
1)
Із жирів.
2)
Із галогенопохідних:
![]() Хімічні
властивості багатоатомних спиртів (на
прикладі гліцерину).
1)
Горіння:
Хімічні
властивості багатоатомних спиртів (на
прикладі гліцерину).
1)
Горіння:
![]() Утворюються
вуглекислий газ і вода (за достатньої
кількості кисню).
2)
Взаємодія з активними металами (може
відбуватися ступінчасто):
Утворюються
вуглекислий газ і вода (за достатньої
кількості кисню).
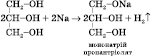
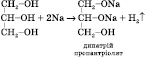
2)
Взаємодія з активними металами (може
відбуватися ступінчасто):
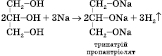 3)
Взаємодія з галогеноводнями (може
відбуватися ступінчасто):
3)
Взаємодія з галогеноводнями (може
відбуватися ступінчасто):
![]() 4)
Нітрування (нітруюча суміш — суміш
концентрованих нітратної і сульфатної
кислот):
4)
Нітрування (нітруюча суміш — суміш
концентрованих нітратної і сульфатної
кислот):
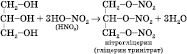 Нітрогліцерин —
вибухова речовина, вибухає від легкого
струсу і нагрівання. Із нітрогліцерину
виробляють динаміт.
5)
Взаємодія з купрум(ІІ) гідроксидом(якісна
реакція на багатоатомні спирти):
Нітрогліцерин —
вибухова речовина, вибухає від легкого
струсу і нагрівання. Із нітрогліцерину
виробляють динаміт.
5)
Взаємодія з купрум(ІІ) гідроксидом(якісна
реакція на багатоатомні спирти):
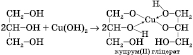 Купрум(ІІ)
гліцерат, що утворюється, — розчин
синього кольору.
Застосування
гліцерину. Гліцерин застосовується
для добування нітрогліцерину (вибухова
речовина), антифризів, у шкіряному
виробництві для пом’якшення шкір, у
медицині.
Купрум(ІІ)
гліцерат, що утворюється, — розчин
синього кольору.
Застосування
гліцерину. Гліцерин застосовується
для добування нітрогліцерину (вибухова
речовина), антифризів, у шкіряному
виробництві для пом’якшення шкір, у
медицині.
Феноли
Феноли —
це органічні сполуки,
у молекулах яких гідроксильні групи
зв’язані збензеновим
ядром.
Феноли
з однією гідроксигрупою
називаються одноатомними.
Найпростіший фенол має загальну
формулу ![]() .
Його структурна
формула:
.
Його структурна
формула:
![]() або
або ![]() Радикал
Радикал ![]() називається феніл.
У
молекулі фенолу відбувається взаємний
вплив гідроксигрупи і бензенового ядра,
в результаті якого атом Гідрогену
гідроксигрупи стає більш реакційноздатним,
а фенол виявляє властивості слабкої
кислоти (слабкішої за карбонатну).
Максимуми електронної густини
в бензеновому кільці знаходяться
в положеннях Карбону 2, 4, 6 відносно групи
-ОН, тому атоми Гідрогену в цих положеннях
легше вступають у реакції заміщення.
Фізичні
властивості фенолу. Безбарвна кристалічна
речовина з різким характерним запахом,
частково розчинна у воді (краще
розчиняється в гарячій воді). Температура
плавлення
називається феніл.
У
молекулі фенолу відбувається взаємний
вплив гідроксигрупи і бензенового ядра,
в результаті якого атом Гідрогену
гідроксигрупи стає більш реакційноздатним,
а фенол виявляє властивості слабкої
кислоти (слабкішої за карбонатну).
Максимуми електронної густини
в бензеновому кільці знаходяться
в положеннях Карбону 2, 4, 6 відносно групи
-ОН, тому атоми Гідрогену в цих положеннях
легше вступають у реакції заміщення.
Фізичні
властивості фенолу. Безбарвна кристалічна
речовина з різким характерним запахом,
частково розчинна у воді (краще
розчиняється в гарячій воді). Температура
плавлення ![]() ,
кипіння
,
кипіння ![]() .
Під час зберігання поступово набуває
рожевого забарвлення (окиснюється
киснем повітря). Розчин фенолу у воді
називається ще карболовою
кислотою.
Біологічна
дія фенолу. Отруйний, має сильні
антисептичні властивості. У разі
попадання на шкіру викликає хімічні
опіки.
.
Під час зберігання поступово набуває
рожевого забарвлення (окиснюється
киснем повітря). Розчин фенолу у воді
називається ще карболовою
кислотою.
Біологічна
дія фенолу. Отруйний, має сильні
антисептичні властивості. У разі
попадання на шкіру викликає хімічні
опіки.
