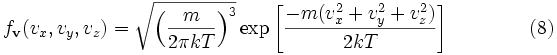- •Вопрос 1.
- •Вопрос 2
- •Вопрос 3.
- •Вопрос 4.
- •Вопрос 5.
- •Вопрос 6.
- •Вопрос 7.
- •Вопрос 8.
- •Вопрос 9.
- •Вопрос 10.
- •Вопрос 11.
- •Вопрос 12.
- •Вопрос 13.
- •Вопрос 14.
- •Вопрос 15.
- •Вопрос 16.
- •Вопрос 17.
- •Вопрос 18.
- •Вопрос 19.
- •Вопрос 20
- •Вопрос 21.
- •Вопрос 22.
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25.
- •Вопрос 26.
- •Вопрос 27.
- •Вопрос 28.
- •Вопрос 29.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32.
- •Вопрос 33.
- •Вопрос 34.
- •Вопрос 35.
- •Вопрос 36.
- •Вопрос 37.
- •Вопрос 38.
- •Вопрос 39.
- •Вопрос 40.
- •Вопрос 41.
- •Вопрос 42.
- •Вопрос 43.
- •Вопрос 44.
- •Вопрос 45.
- •Вопрос 46.
- •Вопрос 47.
- •Вопрос 48.
- •Вопрос 49.
- •Вопрос 50.
- •Вопрос 51.
- •Вопрос 52.
- •Вопрос 53.
- •Вопрос 54.
- •Вопрос 55.
- •Вопрос 56.
- •Вопрос 57.
- •Вопрос 58.
- •Вопрос 59.
- •Вопрос 60.
- •Вопрос 61.
- •Вопрос 62.
- •Вопрос 63.
Вопрос 19.
![]() где
k является отношением газовой постоянной
R к числу Авогадро, а i - число степеней
свободы молекул. Основное уравнение
МКТ связывает макроскопические параметры
(давление, объём, температура) газовой
системы с микроскопическими (масса
молекул, средняя скорость их движения).
где
k является отношением газовой постоянной
R к числу Авогадро, а i - число степеней
свободы молекул. Основное уравнение
МКТ связывает макроскопические параметры
(давление, объём, температура) газовой
системы с микроскопическими (масса
молекул, средняя скорость их движения).
Вывод основного уравнения МКТ
Пусть имеется кубический сосуд с ребром длиной l и одна частица массой m в нём.
Обозначим
скорость движения vx, тогда перед
столкновением со стенкой сосуда импульс
частицы равен mvx, а после - − mvx, поэтому
стенке передается импульс p = 2mvx. Время,
через которое частица сталкивается с
одной и той же стенкой, равно
![]() .
Отсюда следует
.
Отсюда следует
![]() ,
поэтому давление
,
поэтому давление
![]() ,
соответственно
,
соответственно
![]() и
и
![]() Таким образом, для большого числа частиц
верно следующее:
Таким образом, для большого числа частиц
верно следующее:
![]() аналогично
для осей y и z.
аналогично
для осей y и z.
Поскольку
![]() ,
то
,
то
![]() .
Отсюда
.
Отсюда
![]() или
или
![]() Пусть
Пусть
![]() — средняя кинетическая энергия молекул,
а Ek — полная кинетическая энергия всех
молекул, тогда:
— средняя кинетическая энергия молекул,
а Ek — полная кинетическая энергия всех
молекул, тогда:
![]() ,
откуда
,
откуда
![]()
Температура - физическая величина, характеризующая состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру.
Давле́ние (P) — физическая величина, характеризующая состояние сплошной среды и численно равная силе , действующей на единицу площади поверхности перпендикулярно этой поверхности.
Вопрос 20
Под
внутренней энергией термодинамической
системы понимают кинетическую энергию
теплового движения ее молекул и
потенциальную энергию их взаимодействия.
Она зависит от параметров состояния
V,T . Внутренняя энергия идеального
одноатомного газа прямо пропорциональна
его абсолютной температуре:
![]()
Каждое независимое движение называется степенью свободы. Таким образом, одноатомная молекула имеет 3 поступательные степени свободы, «жесткая» двухатомная молекула имеет 5 степеней (3 поступательные и 2 вращательные), а многоатомная молекула – 6 степеней свободы (3 поступательные и 3 вращательные).
В классической статистической физике доказывается так называемая теорема о равномерном распределении энергии по степеням свободы:
Если
система молекул находится в тепловом
равновесии при температуре T, то средняя
кинетическая энергия равномерно
распределена между всеми степенями
свободы и для каждой степени свободы
молекулы она равна
![]()
Вопрос 21.
Молекулы газа вследствие теплового движения испытывают многочисленные соударения друг с другом. При каждом соударении скорости молекул изменяются как по величине, так и по направлению. В результате в сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям, зависящее от абсолютной температуры T. При этом все направления векторов скоростей молекул оказываются равноправными (равновероятными), а величины скоростей подчиняются определенной закономерности. Распределение молекул газа по величине скоростей называется распределением Максвелла. Характерным параметром распределения Максвелла является так называемая среднеквадратичная скорость vкв = <v2>1/2, где <v2> означает среднее значение квадрата скорости.