- •1 Билет)
- •1) Алканы. Строение, нахождение в природе, получение, свойства.
- •2) Механизм электрофильного замещения в ароматическом ряду (SeAr), влияние заместителей на ориентацию
- •2 Билет)
- •1) Алкены: строение, получение, свойства
- •Дегидрирование алканов
- •2) Оптическая изомерия органических соединений с одним асимметричным атомом углерода
- •Рассмотренный вид изомерии называют оптической изомерией, зеркальной изомерией илиэнантиомерией. Обе зеркальные формы составляют пару оптических антиподов или энантиомеров. Проекционные формулы
- •3 Билет)
- •1) Циклоалканы. Стереометрия, методы получения, свойства
- •2) Электронное строение органических соединений. Описание химической связи с помощью метода гибридизации атомных орбиталей. Сигма и пи связь.
- •4 Билет)
- •1) Диены. Строение, получение, свойства
- •2) Оптическая изомерия органических соединений с двумя асимметрическими атомами углерода
- •5 Билет)
- •1) Алкины. Строение, получение, свойства
- •2) Активные промежуточные частицы, обазующиеся в органических реакциях: карбокатионы, карбоанионы, свободные радикалы
- •6 Билет)
- •1) Ароматические угле водороды. Классификация, номенклатура, природные источники. Химические свойства.
- •Свойства
- •Получение
- •2) Геометрическая изомерия
- •7 Билет)
- •1) Спирты. Классификация, номенклатура. Строение, получение и свойства.
- •2) Понятие резонанса в органической химии. Основные положения теории резонанаса
- •8 Билет)
- •1) Фенолы. Строение, получение, свойства
- •Способы получения
- •2) Реакции нуклеофильного замещения при sp3 гибридном атоме углерода. Sn1 механизм
- •9 Билет)
- •1) Простые эфиры и эпоксиды. Строение, получение, свойства
- •Реакционная способность[править]
- •2) Реакции элиминирования, механизм e2, стереохимия
- •10 Билет)
- •1) Галогенпроизводные алканов. Строение, получение, свойства
- •2) Смещение электронной плотности в органических молекулах. Индуктивный и мезомерный эффекты
- •11 Билет)
- •2) Радикальное замещение в ряду алканов, примеры и механизм реакций
- •12 Билет)
- •1) Карбонильные соединения
2) Оптическая изомерия органических соединений с двумя асимметрическими атомами углерода
Так, при наличии в молекуле двух асимметрических атомов углерода число изомеров равно 2 - 4, трех — 2 - 8, четырех — 24 - 16 и т. д.
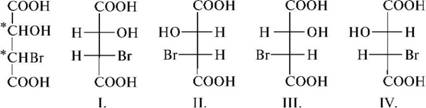
Например, бромяблочная кислота, содержащая два асимметрических атома углерода, существует в виде четырех стереоизоме-ров
5 Билет)
1) Алкины. Строение, получение, свойства
Алки́ны (иначе ацетиленовые углеводороды) — углеводороды, содержащие тройную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n-2. Атомы углерода при тройной связи находятся в состоянии sp-гибридизации.
Для алкинов характерны реакции присоединения. В отличие от алкенов, которым свойственны реакции электрофильного присоединения, алкины могут вступать также и в реакции нуклеофильного присоединения. Это обусловлено значительным s-характером связи и, как следствие, повышенной электроотрицательностью атома углерода. Кроме того, большая подвижность атома водорода при тройной связи обуславливает кислотные свойства алкинов в реакциях замещения. Простейшим алкином является этин (ацетилен C2H2). По номенклатуре IUPAC названия алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»; положение тройной связи указывается арабскими цифрами.
Углеводородные радикалы, образованные от алкинов имеют суффикс «-инил», так CH≡C- называется «этинил».
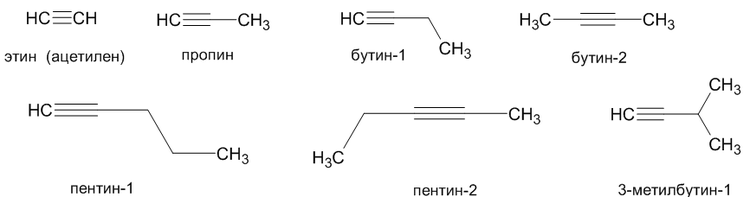
Ниже представлены некоторые представители алкинов и их названия:
Основным промышленным способом получения ацетилена является электро- или термокрекинг метана, пиролиз природного газа и карбидный метод.
Карбидный метод (промышленный способ)[править]
Прокаливанием в электрических печах смеси оксида кальция с коксом при 1800—2000°С получают карбид кальция:
![]()
При действии на полученный карбид воды образуется гидроксид кальция и ацетилен:
![]()
Пиролиз углеводородов (промышленный способ)[править]
Суть способа заключается в пропускании над специальной огнеупорной насадкой смеси природного газа с воздухом, который сгорая поднимает температуру до 1500 °C. Затем на насадке происходит пиролиз метана[13]:
![]()
Крекинг природного газа (промышленный способ)[править]
Электрокрекинг[править]
Метод заключается в пропускании метана между двумя металлическими электродами с огромной скоростью. Температура 1500—1600°С. С химической точки зрения метод аналогичен методу пиролиза, отличаясь лишь технологическим и аппаратным исполнением[14].
Термоокислительный крекинг[править]
В этом методе используется частичное окисление метана благодаря использованию теплоты, образующейся при его сгорании[14]:
![]()
Метод прямого синтеза[править]
Углерод напрямую взаимодействует с водородом при очень высоких температурах:
![]()
Этот метод имеет чисто историческое значение (получение ацетилена в 1863 году М. Бертло).
Электролиз солей непредельных карбоновых кислот[править]
В 1864 году Кекуле получил ацетилен электролизом фумарата и малеата натрия[15]:
![]()
Аналогично получается ацетилен и из акрилата натрия.
Этот метод носит чисто историческое значение.
Дегидрогалогенирование галогеналканов и галогеналкенов (лабораторный способ)[править]
Реакция дегидрогалогенирования проводят действием сильного основания на дигалогеналканы:
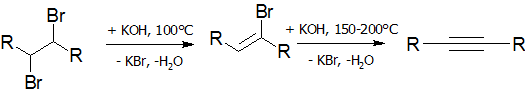
В качестве дегидрогалогенирующего агента удобно использовать амид натрия в жидком аммиаке [16]:
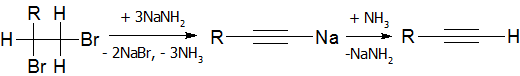
Образование алкинидов[править]
Алкины с концевой тройной связью являются С-H кислотами (сильнее чем аммиак и алкены, но слабее, чем спирты) которые с очень сильными основаниями могут образовывать соли — алкиниды[6]:
![]() (ацетиленид
динатрия)
(ацетиленид
динатрия)
![]() (ацетиленид
калия)
(ацетиленид
калия)
![]() (пропинилмагнийбромид)
(пропинилмагнийбромид)
Реакции электрофильного замещения алкинидов[править]
Алкиниды являются сильными нуклеофилами и легко вступают в реакции нуклеофильного замещения:
![]()
Это, в частности, широко используется для синтеза гомологов ацетилена:
![]()
Получение алкингалогенидов[править]
Действием галогена на монозамещенные ацетилены в щелочной среде можно получить галогеналкины[14]:
![]()
Реакция нуклеофильного замещения алкинидов[править]
![]()
В препаративном синтезе часто используют комплекс ацетиленида лития с этилендиамином как удобный источник ацетиленид-аниона[8].
Следует отметить, что в случае реакции с вторичными или третичными галогеналканами реакция во многом идет по альтернативному пути (элиминирование):
![]()
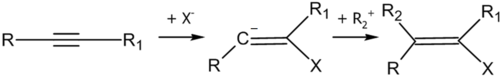
Реакции нуклеофильного присоединения[править]
Нуклеофильное присоединение к алкинам инициируется под воздействием отрицательно заряженной частицы — нуклеофила. В общем случае, катализатором таких реакций являютсяоснования. Общая схема первой стадии реакции нуклеофильного присоединения: