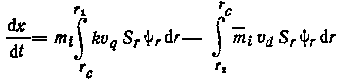- •В.Д.Нефедов е.Н.Текстер м.А.Торопова радиохимия
- •Глава 1
- •§ 1. Предмет радиохимии
- •§ 2. Краткий очерк истории развития радиохимии
- •§ 3. Особенности радиохимии
- •§ 4. Значение радиохимии
- •1 Общая радиохимия глава 2
- •§ 1. Общехимические свойства изотопных частиц
- •2. Термодинамическое поведение изотопных частиц
- •3. Кинетическое поведение изотопных частиц
- •Глава 3
- •§ 1. Классификация реакций изотопного обмена
- •§ 2. Причины протекания реакций изотопного обмена
- •3. Особенности реакций идеального изотопного обмена
- •§ 4. Основное уравнение кинетики реакций идеального изотопного обмена
- •§ 5. Основы экспериментальных методов исследования процессов изотопного обмена
- •Глава 4
- •§ 1. Состояние радиоактивных элементов [нуклидов] в жидкой фазе
- •§ 2. Процессы радиоколлоидообразования
- •§ 3. Основы экспериментальных методов исследования радиоколлоидов
- •Глава 5
- •§ 1. Закономерности процессов соосаждения с изотопными носителями
- •§ 2. Основные области применения изотопных носителей
- •§ 3. Принцип действия и закономерности процессов соосаждения со специфическими носителями
- •§ 4 Факторы, влияющие на процесс соосаждения со специфическими носителями
- •§ 5. Особенности процессов соосаждения со специфическими носителями
- •§ 6. Сокристаллизация со специфическими носителями при отсутствии изоморфизма 1 рода
- •§ 7. Основы экспериментальных методов исследования процессов соосаждения со специфическими носителями
- •§ 8. Основные области применения специфических носителей
- •Глава 6
- •§ 1. Первичная адсорбция
- •§ 2. Вторичная обменная адсорбция
- •§ 3. Закономерности процесса соосаждения с неспецифическими носителями
- •§ 4. Соосаждение с неспецифическими носителями при образовании внутренне-адсорбционных систем
- •§ 5. Основы экспериментальных методов исследования процессов соосаждения с неспецифическими носителями
- •§ 6. Основные области применения неспецифических носителей
- •§ 7. Методы разграничения различных видов соосаждения
- •Глава 7
- •§ 1. Закономерности и классификация экстракционных процессов
- •§ 3. Практическое использование процессов экстракции
- •Глава 8
- •§ 1. Основные закономерности хроматографических процессов Ионообменная хроматография.
- •Распределительная хроматография.
- •См.: Егоров е. В., Макарова с. Б. Ионный обмен в радиохимии. М., Атомиздат, 1971. § 2. Основы экспериментальных методов хроматографического исследования
- •См.: Роберте т. Радиохроматография. М., Мир, 1981. § 3. Примеры практического использования хроматографических методов в радиохимии
- •Глава 9
- •§ 1. Закономерности электрохимических процессов
- •§ 2 Особенности поведения радиоактивных элементов (нуклидов) при электрохимических процессах
- •§ 3. Основы экспериментальных методов исследования электрохимических процессов
- •§ 4. Использование электрохимических процессов в радиохимии
- •2 Химия радиоактивных элементов
- •Глава 10
- •§ 1. Технеций
- •§ 2. Прометий
- •§ 3. Полоний
- •§ 4. Астат
- •§ 5. Радон
- •§ 6. Франций
- •§ 7. Радий
- •Глава 11
- •§ 1. История открытия актиния и актиноидов
- •§ 2. Важнейшие изотопы актиния и актиноидов, методы их получения и идентификации
- •§ 3. Физические свойства актиния и актиноидов
- •§ 4. Актиний
- •§ 5. Торий
- •§ 6. Протактиний
- •§ 7. Уран, нептуний, плутоний и америций
- •§ 8. Трайсамерициевые актиноиды
- •Глава 12
- •§ 1. История открытия
- •§ 2 Методы получения и идентификации
- •3 Химические последствия радиоактивного распада
- •Глава 13
- •§ 1. История открытия ядерной изомерии
- •§ 2. Особенности явления ядерной изомерии
- •§ 3. Химические последствия изомерных переходов
- •§ 4. Практическое использование химических последствий изомерного перехода
- •Глава 14
- •§ 1. Теоретические аспекты химических последствий --распада
- •§ 2. Экспериментальные методы исследования химических последствий --распада
- •§ 3. Практическое использование химических последствий --распада
§ 5. Особенности процессов соосаждения со специфическими носителями
Наиболее важная особенность процессов соосаждения со специфическими носителями - и з б и р а т е л ь н о с т ь п о о т н о ш е н и ю к р а д и о а к т и в н о м у э л е м е н т у. Это объясняется тем, что при соосаждении со специфическим носителем происходит отбор по нескольким параметрам: по знаку и величине заряда ионов, их радиусам и поляризуемости. В случае сложных ионов к перечисленным параметрам добавляется состав, электронное и пространственное строение.
Другая особенность процессов соосаждения со специфическими носителями — о т с у т с т в и е н и ж н е й г р а н и ц ы с м е ш и в а е м о с т и. Такие процессы происходят при сколь угодно малых концентрациях соосаждающегося элемента, так как процессы соосаждения со специфическими носителями протекают в результате замещения наименьших структурных единиц кристаллической решетки вещества носителя аналогичными структурными единицами вещества радиоактивного элемента. В случае ионных кристаллов такими единицами являются простые или комплексные ионы, в молекулярных кристаллах — молекулы.
Существенной особенностью процессов соосаждения со специфическими носителями является з а в и с и м о с т ь с т е п е н и п е р е н о с а р а д и о а к т и в н о г о э л е м е н т а в т в е р д у ю ф а з у и закономерностей, описывающих этот перенос, от у с л о в и й о б р а з о в а н и я к р и с т а л л и ч е с к о й ф а з ы.
Рассмотренные нами закономерности процессов соосаждения, подчиняющиеся закону Хлопина, относятся к случаю установления равновесия между раствором и кристаллической фазой в целом в результате процессов многократной перекристаллизации последней. При этом радиоактивный элемент равномерно распределяется по всему объему кристаллов носителя (гомогенное распределение).
Если процессы образования твердой фазы происходят в условиях, исключающих ее перекристаллизацию, то мы имеем дело с так называемым гетерогенным распределением. Такое распределение наблюдается при медленном изотермическом испарении насыщенного раствора вещества носителя, содержащего радиоактивный элемент, в условиях непрерывного перемешивания. Этот случай впервые был рассмотрен Г. Дёрнером и В. Госкинсом, которые в своих теоретических выводах исходили из кинетических представлений об ионном обмене между поверхностью кристалла и раствором.
Допустим, что процесс роста кристалла происходит достаточно медленно для того, чтобы между поверхностным слоем твердой фазы и раствором могло установиться равновесие. Тогда распределение радиоактивного элемента (в отношении каждого элементарного слоя кристалла) может быть описано в соответствии с законом В. Г. Хлопина следующим уравнением:
|
(5.26) |
где — коэффициент кристаллизации для процесса соосаждения с образованием элементарного слоя твердой фазы; d(miV) и d(mnV) — массы радиоактивного элемента и носителя, переходящие в элементарный слой растущего кристалла; а и b — исходные массы радиоактивного элемента и носителя.
После того как закончится образование первого элементарного слоя, начнет образовываться следующий. Между новым элементарным слоем и раствором вновь установится истинное равновесие. При этом обмен радиоактивным элементом между отдельными слоями не имеет места вследствие отсутствия диффузии и перекристаллизации.
Интегрируя выражение (5.26) при начальных условиях t = 0, mi = 0, mn = 0, имеем
|
(5.27) |
Уравнение (5.27) описывает процесс гетерогенного распределения радиоактивного элемента между раствором и кристаллической фазой в целом. Характер распределения радиоактивного элемента в этом случае будет определяться численным значением коэффициента При значениях , отличных от единицы, кристалл будет неоднородным в отношении содержания радиоактивного элемента и иметь слоистую (луковичную) структуру. Причем если > 1, то концентрация радиоактивного элемента будет максимальной в начале кристаллизации, т. е. будет уменьшаться от центра кристалла к периферии. При < 1 будет иметь место обратная картина. И, наконец, при = 1 происходит гомогенное распределение радиоактивного элемента по всему объему кристалла (это имеет место при соосаждении с изотопными носителями).
Из рассмотрения гомогенного и гетерогенного распределений видно, что характер соосаждения определяется кинетикой процессов, протекающих при образовании смешанных кристаллов. Кинетика соосаждения прежде всего зависит от состава системы, а также от условий соосаждения (температуры, степени пересыщения, интенсивности перемешивания).
Попытка количественного описания временной зависимости соосаждения была предпринята И. В. Мелиховым с сотрудниками*. Согласно их теории скорость перехода радиоактивного элемента в кристаллическую фазу может быть выражена следующим уравнением:
|
(5.28) |
где mi и mi — концентрации радиоактивного элемента в растворе и твердой фазе соответственно; k — коэффициент распределения радиоактивного элемента между твердой фазой и слоем раствора, прилегающего к ее поверхности, в момент времени t; vq и vd— скорости роста и растворения кристаллов; Sr — поверхность кристалла; — функция распределения радиоактивного элемента по объему кристалла. Пределы интегрирования r1, r2 и rc отвечают максимальному, минимальному и критическому размерам кристалла соответственно.
Таким образом, кинетика сокристаллизации определяется двумя процессами: внедрением радиоактивного элемента в растущий кристалл и растворением смешанных кристаллов субкритического размера.
Строгое решение уравнения (5.28) невозможно, поскольку значении k, r и др. зависят от условий соосаждения. Частные решения этого уравнения были получены И. В. Мелиховым при рассмотрении некоторых идеализированных режимов процесса соосаждения. Так, если скорость роста кристаллов значительно больше скоростей их перекристаллизации и созревания, то второй член уравнения (5.28) становится ничтожно малым по сравнению с первым. Уравнение в этом случае упрощается и сравнению с первым. Уравнение принимает вид
|
(5.29) |
Однако решение этого уравнения также затруднено, поскольку величина k зависит от многих факторов: скорости переноса радиоактивного элемента из объема раствора к поверхности растущего кристалла vt, скорости внедрения радиоактивного элемента в поверхность кристалла vi, скорости миграции радиоактивного элемента внутрь кристалла vm, скорости химической реакции радиоактивного элемента в растворе vr. Результатом одновременного влияния всех этих факторов является зависимость процесса соосаждения от времени.
Для получения частных решений уравнения (5.29) И. В. Мелихов рассматривает четыре кинетических режима, в каждом из которых превалирующее значение имеет один из рассмотренных выше факторов: 1) если vt, vr >> vi >> vm 0, то скорость соосаждения определяется vi. Этот случай называется адсорбционно-кинетическим режимом, так как доминирующим фактором является кинетика адсорбции (внедрения микрокомпонента в кристаллическую поверхность); 2) если vr, vi >> vt >> vm 0, то скорость переноса (диффузии) становится доминирующим фактором. Эта ситуация определяется как режим жидкофазной диффузии. В неперемешиваемых системах зона диффузии включает практически весь объем раствора; в перемешиваемых системах она ограничивается тонким слоем раствора, адгезированного кристаллической поверхностью; 3) если vr, vt, vi >> vm >> 0, то сокристаллизация протекает в миграционном режиме, поскольку общая скорость определяется миграцией (диффузией) в твердой фазе. В миграционном режиме скорость миграции сравнима со скоростью роста кристаллов; 4) если vt, vi >> vr >> vm = 0, то все факторы, кроме vr, ничтожно малы, и соосаждение протекает в жидкофазном кинетическом (или лучше — реакционно-кинетическом) режиме. Этот случай относится к медленному образованию или диссоциации сокристаллизующегося соединения в растворе. Сравнение результатов вычислений по упрощенным моделям с экспериментальными данными на реальных системах (формальный кинетический анализ) проливает свет на механизм соосаждения.
Таким образом
в отличие от процессов соосаждения с изотопными носителями, при изоморфной сокристаллизации мы имеем дело с различными элементами. Поэтому представляется возможным отделение радиоактивного элемента от элемента-носителя, основанное на некотором различии их свойств.
См.: Мелихов И. В., Меркулова М. С. Сокристаллизация. М., Химия, 1975.