
- •Курс лекций
- •Содержание
- •Введение
- •1 Механическое движение и его виды
- •1 Механическое движение и его виды
- •2 Кинематика поступательного движения
- •3 Кинематика вращательного движения
- •4 Связь между угловыми и линейными величинами
- •Контрольные вопросы
- •1 Динамические характеристики поступательного движения
- •2 Законы Ньютона
- •3 Динамические характеристики вращательного движения
- •Моменты инерции некоторых тел
- •4 Основной закон динамики вращательного движения
- •5 Аналогия формул поступательного и вращательного движений
- •Основные характеристики и формулы кинематики
- •Контрольные вопросы
- •1 Понятие симметрии. Теорема Нетер
- •2 Закон сохранения импульса
- •3 Момент импульса. Закон сохранения момента импульса
- •4 Работа, мощность, энергия
- •5 Закон сохранения энергии
- •Контрольные вопросы
- •1 Принципы относительности Галилея и Эйнштейна
- •2 Понятие о специальной теории относительности
- •3 Основной закон релятивисткой динамики материальной точки
- •4 Закон взаимосвязи массы и энергии
- •Контрольные вопросы
- •Молекулярно-кинетическая теория идеальных газов
- •1 Основные положения молекулярно – кинетической теории
- •2 Опытные законы идеального газа. Уравнение состояния
- •3 Основное уравнение молекулярно-кинетической теории идеальных газов
- •4 Распределение Максвелла
- •5 Барометрическая формула. Распределение Больцмана
- •Контрольные вопросы
- •Основы равновесной термодинамики
- •1 Внутренняя энергия тела и идеального газа
- •2 Работа газа при изменении его объема
- •3 Первое начало термодинамики
- •4 Второе начало термодинамики
- •5 Тепловые двигатели и их кпд
- •Контрольные вопросы
- •Элементы неравновесной термодинамики
- •1 Энтропия как мера беспорядка в системе. Статистический смысл второго начала термодинамики
- •2 Третье начало термодинамики
- •3 Изменение энтропии в открытых системах
- •4 Понятие о самоорганизации
- •5 Примеры самоорганизации в природе
- •Контрольные вопросы
- •Сформулируйте расширенный вариант второго закона термодинамики для открытых систем.
- •Электростатическое поле
- •2 Электростатическое поле и его характеристики
- •3 Теорема Гаусса для электростатического поля в вакууме
- •4 Циркуляция вектора напряженности электростатического поля
- •6 Энергия электростатического поля
- •Контрольные вопросы
- •1 Магнитное поле
- •2 Силы Ампера и Лоренца
- •3 Закон Био – Савара – Лапласа. Простейшие случаи расчета магнитных полей
- •4 Работа по перемещению проводника с током в магнитном поле
- •Контрольные вопросы
- •1 Явление электромагнитной индукции
- •Явления самоиндукции и взаимной индукции
- •3 Магнитное поле в веществе
- •4 Теорема о циркуляции для магнитного поля
- •5 Энергия магнитного поля
- •Контрольные вопросы
- •2 Ток смещения
- •3 Уравнение Максвелла для электромагнитного поля
- •Контрольные вопросы
- •1 Свободные гармонические колебания
- •1 Свободные гармонические колебания
- •2 Затухающие и вынужденные колебания
- •3 Волны
- •4 Электромагнитные волны
- •Контрольные вопросы
- •Волновые свойства электромагнитного излучения
- •1 Развитие представлений и природе света
- •2 Интерференция света и методы ее наблюдения
- •1 Метод Юнга
- •2 Зеркало Ллойда
- •3 Интерференция в тонких пленках
- •3 Дифракция электромагнитных волн
- •4 Поляризация света
- •Контрольные вопросы
- •Квантовые свойства электромагнитного излучения
- •1 Тепловое излучение. Гипотеза Планка
- •2 Фотоэффект и его применение
- •3 Давление света. Фотоны
- •4 Эффект Комптона
- •5 Единство волновых и корпускулярных свойств электромагнитного излучения
- •Контрольные вопросы
- •1 Гипотеза де Бройля. Корпускулярно волновой дуализм как универсальное свойство материи
- •2 Соотношение неопределенностей
- •3 Волновая функция и ее статистический смысл
- •4 Уравнение Шредингера и его решения для ряда простейших случаев
- •1 Движение свободной частицы
- •2 Частица в одномерной прямоугольной «потенциальной яме» с бесконечно высокими стенками
- •Контрольные вопросы
- •1 Развитие представлений о строении атома
- •2 Атом водорода в квантовой механике
- •3 Многоэлектронные атомы
- •4 Атомное ядро
- •5 Радиоактивность. Радиоактивные излучения
- •Контрольные вопросы
- •Современная физическая картина мира
- •1 Агрегатные состояния вещества
- •2 Кристаллы и их симметрия. Дефекты в кристаллах
- •3 Понятие о зонной теории твердых тел
- •4 Проводимость твердых тел. Проводники, полупроводники и диэлектрики
- •Контрольные вопросы
- •2 Частицы и античастицы
- •3 Элементарные частицы и их классификация. Понятие о кварках
- •1 Основные типы физических взаимодействий в природе
- •2 Частицы и античастицы
- •3 Элементарные частицы и их классификация. Понятие о кварках
- •4 Современная физическая картина мира
- •Контрольные вопросы
- •Заключение
- •Библиографический список
- •Перечень ключевых слов
Современная физическая картина мира
Лекция № 17 Зонная теория твердых тел
1 Агрегатные состояния вещества
2 Кристаллы и их симметрия. Дефекты в кристаллах
3 Понятие о зонной теории твердых тел
4 Проводимость твердых тел. Проводники, полупроводники и диэлектрики
1 Агрегатные состояния вещества
Согласно основным положениям МКТ (лекция № 5) между молекулами вещества существуют силы притяжения Fпр и силы отталкивания Fот. Силы межмолекулярного взаимодействия являются короткодействующими: они проявляются на расстояниях r≤10-9м и быстро уменьшаются при увеличении расстояния между молекулами. На рисунке 27 представлена качественная зависимость результирующей силы взаимодействия F=Fпр+Fот от расстояния r между молекулами (силы отталкивания считаются положительными, а силы притяжения отрицательными). На расстоянии r=r0 результирующая сила равна нулю. Это расстояние соответствует равновесному расстоянию между молекулами, на котором бы они находились в отсутствие теплового движения.
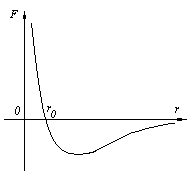
r < r0 , Fот > Fпр ,
r > r0 , Fот < Fпр ,
r , F 0.
Рисунок 27 – Зависимость силы взаимодействия между молекулами
от расстояния между ними
Равновесному расстоянию r0 соответствует Пmin – наименьшая потенциальная энергия взаимодействия молекул. Критерием различных агрегатных состояний вещества является соотношение величин Пmin и kT (k – постоянная Больцмана, T – температура). kT представляет собой меру теплового хаотического движения молекул при данной температуре.
Если Пmin << kT, то вещество находится в газообразном состоянии.
Если Пmin >> kT, то вещество находится в твердом состоянии.
Если Пmin ≈ kT, то вещество находится в жидком состоянии.
Скорость движения молекул и их средняя кинетическая энергия Tкин зависят от температуры, поэтому критерий различных агрегатных состояний вещества можно сформулировать через соотношение между кинетической энергией теплового движения молекул и потенциальной энергией их взаимодействия. В газах взаимодействие между молекулами мало, а интенсивность теплового хаотического движения велика. В твердых телах потенциальная энергия взаимодействия частиц много больше их кинетической энергии. В жидкостях потенциальная энергия взаимодействия молекул сравнима с их кинетической энергией.
2 Кристаллы и их симметрия. Дефекты в кристаллах
В твердой фазе тело может находиться в двух состояниях – аморфном и кристаллическом.
В аморфном состоянии отсутствует какой–либо порядок в расположении атомов. В кристаллическом состоянии атомы (молекулы, ионы) расположены в строгом порядке. Кристаллы существуют за счет значительных сил межмолекулярного взаимодействия и сохраняют свои объем и форму.
Структура, для которой характерно регулярное расположение частиц с периодической повторяемостью в трех измерениях, называется кристаллической решеткой. Расстояния, на которых происходят повторения, называются периодами кристаллической решетки. Средние равновесные положения, около которых частицы совершают колебания, называются узлами кристаллической решетки.
Кристаллические тела можно разделить на монокристаллы и поликристаллы. Монокристаллы – твердые тела, образующие единую кристаллическую решетку. Кристаллическая структура монокристаллов обнаруживается по их внешней форме. Поликристаллы образованы из множества беспорядочно ориентированных мелких кристаллических зерен. Характерным свойством монокристаллов является зависимость их физических свойств (упругих, механических, тепловых, электрических, оптических) от направления. Такое свойство называется анизотропностью. Свойства поликристаллов по всем направлениям в среднем одинаковы.
Для классификации кристаллов существует два признака – кристаллографический и физический.
Для кристаллографического признака кристаллов важна только пространственная периодичность в расположении частиц. В этом случае частицы рассматривают как геометрические точки.
Кристаллическая решетка может обладать различными видами симметрии (см.лекцию № 3). Советский кристаллограф Е.С. Федоров показал, что возможны 230 пространственных групп симметрии и, соответственно, 230 типов кристаллических решёток.
Всякая пространственная решетка может быть составлена многократным повторением в трех измерениях одного структурного элемента. Этот элемент называется элементарной ячейкой. Самой высокой симметрией обладает кубическая кристаллическая решетка, самой низкой симметрией - триклинная.
Некоторые вещества способны создавать различные типы кристаллов (разной симметрии). Это явление называется аллотропией. Например, углерод кристаллизуется в слоистую гексагональную структуру (графит) и тетраэдрическую (алмаз). Различие в строении кристаллических решеток объясняет различие их физических свойств. Графит является одним из самых мягких веществ, алмаз – самый твердый материал. Графит хорошо проводит электричество, алмаз проявляет свойства диэлектрика. В последние годы были открыты новые аллотропные модификации углерода – фуллерены и графен.
В зависимости от рода частиц, расположенных в узлах кристаллической решетки, и характера сил взаимодействия между ними (физический признак кристаллов) все кристаллы делятся на ионные, атомные, металлические и молекулярные.
В реальной кристаллической решетке всегда имеются отклонения от упорядоченного расположения частиц в узлах решетки. Эти отклонения называются дефектами. Дефекты делятся на макроскопические (трещины, полы, макроскопические включения) и микроскопические, обусловленные микроскопическими отклонениями от периодичности.
Микродефекты делятся на точечные и линейные. Точечные дефекты могут представлять собой вакансии (отсутствие атома в узле кристаллической решетки), внедрения (атом существует в междоузлие) и замещения (в узле решетки находится атом иного типа нежели должен быть). Точечные дефекты нарушают только ближний порядок в кристалле, не затрагивая дальнего порядка.
Линейные дефекты представляют собой нарушения дальнего порядка, при этом нарушается чередование кристаллографических плоскостей. Такие дефекты называются дислокациями. Дислокации бывают краевыми и винтовыми.
