
- •12. Що показує дослід Кантора?
- •13. Поясніть, що відображає барометричне рівняння Больцмана.
- •14. Як змінюється концентрація газу, що знаходиться під дією центральної сили?
- •При яких умовах максвеллівський розподіл швидкостей молекул справедливий?
- •Який вигляд має максвеллівський розподіл швидкостей молекул і що він показує?
- •Запишіть як виражається середня квадратична швидкість молекул газу.
- •Дайте визначення найбільш ймовірної швидкості молекул газу.
- •Що впливає на число молекул газу, що ударяються за одиницю часу в одиницю поверхні стінки ємності?
- •Дайте визначення середньої довжини вільного пробігу молекул у газі.
- •Що впливає на середню довжину вільного пробігу молекул?
- •Що називають ефузією в газі?
Запишіть як виражається середня квадратична швидкість молекул газу.
З графіка
функціі видно, що вона має максимум при
![]() ,
тобто швидкість
молекули мають частіше, ніж іншого
значення і з цієї причини її називають
найбільш ймовірною. Наприклад, швидкість,
що вдвічі більша за найбільш ймовірну
зустрічається приблизно в 0,2 рази рідше,
ніж найбільш ймовірна. Величина найбільш
ймовірної швидкості залежить від
температури і природи газу
,
тобто швидкість
молекули мають частіше, ніж іншого
значення і з цієї причини її називають
найбільш ймовірною. Наприклад, швидкість,
що вдвічі більша за найбільш ймовірну
зустрічається приблизно в 0,2 рази рідше,
ніж найбільш ймовірна. Величина найбільш
ймовірної швидкості залежить від
температури і природи газу
![]() =
=
![]() .
(2.15)
.
(2.15)
Середня квадратична швидкість молекул знаходиться за формулою
![]() =
=
![]() ,
(2.16)
,
(2.16)
а
Рис. 2-3.

Рис. 2.3
![]() =
=
![]() .
(2.17)
.
(2.17)
Якщо вираз для найбільш ймовірної швидкості (2.15) підставимо в рівняння (2.14), то отримаємо в іншому вигляді функцію розподілу молекул за швидкостями, яка ще називається функцією Максвелла – Больцмана:
 .
(2.18)
.
(2.18)
При врахуванні, що кінетична енергія молекули це –
![]() ,
,
отримаємо з (2.18) рівняння розподілу кінетичної енергії молекул:
![]() .
.
Дайте визначення найбільш ймовірної швидкості молекул газу.
З графіка функціі видно, що вона має максимум при , тобто швидкість молекули мають частіше, ніж іншого значення і з цієї причини її називають найбільш ймовірною. Наприклад, швидкість, що вдвічі більша за найбільш ймовірну зустрічається приблизно в 0,2 рази рідше, ніж найбільш ймовірна. Величина найбільш ймовірної швидкості залежить від температури і природи газу
= . (2.15)
Середня квадратична швидкість молекул знаходиться за формулою
= , (2.16)
а
Рис. 2-3.
Рис. 2.3
= . (2.17)
Якщо вираз для найбільш ймовірної швидкості (2.15) підставимо в рівняння (2.14), то отримаємо в іншому вигляді функцію розподілу молекул за швидкостями, яка ще називається функцією Максвелла – Больцмана:
. (2.18)
При врахуванні, що кінетична енергія молекули це –
,
отримаємо з (2.18) рівняння розподілу кінетичної енергії молекул:
.
Що впливає на число молекул газу, що ударяються за одиницю часу в одиницю поверхні стінки ємності?
У вакуумній техніці в багатьох випадках необхідно визначити кількість молекул газу, що проникнуть за одиницю часу через якийсь отвір у стінці ємності, в якій знаходиться газ. Для цього необхідно знати кількість молекул газу, що ударяються за одиницю часу в одиницю площини стінки ємності, в якій знаходиться газ.
Р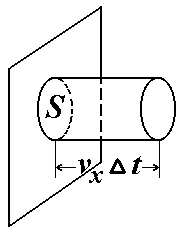 озглянемо
циліндр з площею основи S
і довжиною
озглянемо
циліндр з площею основи S
і довжиною
![]() t,
що дорівнює відстані, яку пробігає одна
молекула за проміжок часу
t,
що дорівнює відстані, яку пробігає одна
молекула за проміжок часу
![]() t,
маючи на увазі, що вона ударяється в
стінку (основу S).
Тоді число молекул, що ударяється в
основу S
дорівнюватиме
t,
маючи на увазі, що вона ударяється в
стінку (основу S).
Тоді число молекул, що ударяється в
основу S
дорівнюватиме
![]() .
.
Д
Рис. 3.1
Оскільки
![]() ,
то за одиницю часу
,
то за одиницю часу
![]()
Замінимо середню квадратичну швидкість на середню арифметичну, тоді отримаємо
![]() .
.
Якщо враховувати, що не всі молекули спрямляються до основи перпендикулярно, а частина буде ударятися під всілякими кутами, то необхідно підкореневий вираз замінити на одиницю і остаточно отримаємо число молекул газу, що ударяються за одиницю часу в одиницю площини стінки
![]() .
(3.1)
.
(3.1)
Використовуючи рівняння Больцмана і формулу (2.20) матимемо, що ця кількість прямопропорційно залежить від тиску
![]() (3.2)
(3.2)
і маса молекул газу, що ударяються за одиницю часу у одиницю поверхні стінки ємності, в якій знаходиться газ буде дорівнювати
![]() .
.
