
- •Введение
- •Часть I строение и физиология микроорганизмов
- •Глава I. Строение и принципы систематики микроорганизмов
- •Бактерии
- •Неклеточные формы жизни
- •Водоросли и водные грибы
- •Простейшие
- •Глава II. Химический состав клетки
- •Вода и минеральные соли
- •Органические вещества клетки
- •Синтез белка
- •Мутагенез
- •Глава. III. Ферменты
- •Ферменты—биологические катализаторы
- •Строение и свойства ферментов
- •Принципы классификации ферментов
- •Окислительно-восстановительные ферменты (оксиредуктазы)
- •Регуляция синтеза ферментов
- •Глава IV. Получение энергии микроорганизмами Энергетический и конструктивный обмены
- •Получение энергии литотрофами
- •Получение энергии органотрофами
- •Взаимосвязь процессов обмена в организме
- •Глава V. Закономерности роста и развития микробных культур Рост, развитие, размножение
- •Понятие об абсолютной и относительной скорости роста
- •Особенности выращивания микроорганизмов в проточных культурах
- •Фазы развития микробной культуры
- •Влияние лимитирующих факторов на скорость роста
- •Скорость роста и физиологическая активность
- •Глава VI. Влияние внешних факторов на микроорганизмы Влияние температуры
- •Влияние влажности
- •Влияние лучистой энергии
- •Влияние осмотического давления
- •Активная реакция среды и окислительно-восстановительный потенциал
- •Часть II участие микроорганизмов в превращении веществ
- •Глава VII. Круговорот углерода
- •Распространение микроорганизмов в природе
- •Круговорот углерода и участие в нем микроорганизмов
- •Глава VIIII. Расщепление органических соединений в анаэробных условиях
- •Сбраживание углеводов
- •Маслянокислое брожение
- •Cбраживание жиров
- •Анаэробное расщепление белков
- •Глава IX. Расщепление органинеских соединений в аэробных условиях
- •Окисление углеводов
- •Окисление этанола. Получение уксусной кислоты
- •Окисление жиров
- •Окисление углеводородов
- •Расщепление азотсодержащих соединений
- •Глава X. Превращение соединений азота микроорганизмами Нитрификация
- •Денитрификация
- •Фиксация молекулярного азота
- •Глава XI. Превращение соединений серы микроорганизмами
- •Окисление соединений серы
- •Восстановление соединений серы
- •Глава XIII. Превращение соединений металлов микроорганизмами
- •Окисление соединений записного железа
- •Окисление соединений марганца
- •Выщелачивание металлов из руд
- •Часть III загрязнение и самоочищение водоемов
- •Глава XIIII. Экологические системы пресных водоемов Понятие экосистемы
- •Роль окружающей среды в формировании экосистемы
- •Особенности речных экосистем
- •Особенности озерных экосистем
- •Особенности экосистем водохранилищ
- •Глава XIV. Загрязнение водоемов
- •Характеристика основных видов загрязнения
- •Виды воздействия сточных вод на водоемы
- •Глава XV. Загрязнение водоемов и распространение водных инфекций
- •Понятие инфекции
- •Распространение инфекции
- •Водные инфекции
- •Понятие иммунитета
- •Противоэпидемические мероприятия
- •Глава XVI. Круговорот веществ и энергии в водоемах. Самоочищение водоемов
- •Поступление органических веществ в водоем с водосборной площади
- •Cинтез первичной продукции в водоеме
- •Превращение и деструкция органического вещества
- •Роль отдельных групп гидробионтов в самоочищении водоемов
- •Глава XVIII. Оценка степени загрязненности водоема Классификация водоемов по степени загрязненности
- •Санитарно-бактериологический анализ
- •Часть IV биологические процессы в системах Глава XVIII. Биологические помехи в водоснабжении
- •Помехи, вызываеалые аллохтонными организмами
- •Помехи, вызываемые автохтонными организмами
- •Влияние обрастаний на качество воды и материал труб
- •Меры борьбы с биологическими помехами
- •Глава XIX. Население очистных сооружений канализации
- •Глава XX. Экологические системы очистных сооружений канализации
- •Экосистемы искусственных аэрационных очистных сооружений
- •Экологические системы естественных аэрационных очистных сооружений
- •Экосистемы анаэробных очистных сооружений
- •Литература
- •Оглавление
Глава X. Превращение соединений азота микроорганизмами Нитрификация
В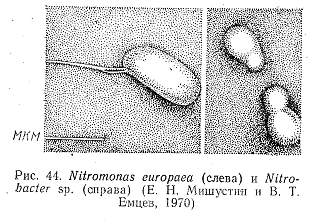 результате расщепления азотсодержащих
органических соединений в большом
количестве выделяется аммиак. В. природных
условиях, в почве и в воде водоема этот
аммиак потребляется растениями в
процессе роста или подвергается
воздействию особой группы микроорганизмов,
окисляющих его с образованием азотистой
и азотной кислот. Процесс называется
нитрификацией, а микроорганизмы—соответственно
нитрификаторами, или нитрифицирующими
бактериями.
результате расщепления азотсодержащих
органических соединений в большом
количестве выделяется аммиак. В. природных
условиях, в почве и в воде водоема этот
аммиак потребляется растениями в
процессе роста или подвергается
воздействию особой группы микроорганизмов,
окисляющих его с образованием азотистой
и азотной кислот. Процесс называется
нитрификацией, а микроорганизмы—соответственно
нитрификаторами, или нитрифицирующими
бактериями.
Нитрификаторы относятся к литоавтотрофным организмам и не нуждаются в органических веществах. Более того, присутствие в среде органических соединений часто пагубно отражается на их развитии. По этой причине нитрификаторы долгое время ускользали от внимания исследователей. Несмотря на то, что образование селитры из мочевой кислоты и мочи известно очень давно, биологическая природа нитрификации была установлена только в конце прошлого века С. Н. Виноградским. Изучая процесс нитрификации, он заметил, что окисление аммиака идет в две фазы, причем каждая фаза имеет своего возбудителя.
Первая фаза нитрификации—окисление солей аммония в нитриты—протекает по уравнению:
![]()
Типичный возбудитель первой фазы нитрификации—Nitrosomonas europaea (рис. 44). Эта бактерия имеет форму укороченного овала, размером 0,6—1,0х0,9—2 мкм, спор не образует. Организм изменяется по фазам развития:, первые 3—4 суток бактерии ведут неподвижный образ жизни, затем развивают жгутики, расположенные на одном конце тела, и становятся подвижными; через 8—9 дней клетки начинают образовывать зооглейные скопления. Замечено, что образование зооглей связано с повышением концентрации нитритов в среде. Оно начинается при содержании нитритов 800 мг/л, а при концентрации 1100 мг/л бактерии переходят в стационарную фазу развития, и рост клеток прекращается. Зооглейные скопления более устойчивы к неблагоприятным воздействиям среды, чем одиночные клетки Nitrosotnonas.
Среди штаммов Nitrosomonas существуют формы с различным температурным оптимумом. Помимо мезофилов, среди них известны термофилы (оптимум 40 °С) и психрофилы (оптимум 4 °С,). Наиболее благоприятная реакция среды для нитрифицирующих бактерий находится в интервале рН 7,0—8,6. Некоторые штаммы нитрификаторов устойчивы к повышенной концентрации солей.
В
качестве окисляемого субстрата
Nitrosomonas
способен использовать аммиак, мочевину,
мочевую кислоту, гуанин. При этом
органическую часть молекулы бактерия
не потребляет. Всю энергию, необходимую
для процессов жизнедеятельности,
Nitrosonionas
получает, окисляя соли аммония, который
выступает при этом в качестве донора
водорода. Конечным акцептором водорода
служит молекулярный кислород. Процесс
аналогичен дыханию. Перенос электронов
осуществляется теми же ферментами, что
и при дыхании. При окислении 1 г/моль NН3
до
![]() выделяется 332 кДж. На восстановление 1
г/моль СO2
требуется 483 кДж: Коэффициент использования
энергии у Nitrosomonas
составляет 5—10 %, и для восстановления
одной молекулы СО2
Nitrosomonas
должен окислить примерно 35 молекул
аммиака. По этой причине у Nitrosomonas
энергетический обмен преобладает над
конструктивным. Клетки Nitrosomonas
размножаются очень медленно и об их
развитии легче судить по результатам
химических анализов.
выделяется 332 кДж. На восстановление 1
г/моль СO2
требуется 483 кДж: Коэффициент использования
энергии у Nitrosomonas
составляет 5—10 %, и для восстановления
одной молекулы СО2
Nitrosomonas
должен окислить примерно 35 молекул
аммиака. По этой причине у Nitrosomonas
энергетический обмен преобладает над
конструктивным. Клетки Nitrosomonas
размножаются очень медленно и об их
развитии легче судить по результатам
химических анализов.
В присутствии органических веществ обычно наблюдается угнетение роста нитрифицирующих бактерий, но в то же время в природных условиях, на полях орошения и фильтрации наблюдается интенсивная нитрификация.
Вторая стадия нитрификации заключается в окислении образовавшихся в первую фазу солей азотистой кислоты в соли азотной кислоты. Процесс протекает в соответствии с уравнением:
![]()
Возбудитель второй фазы нитрификации Nitrobacler winogradskyi (см. рис. 44). Nitrobacter представляет собой мелкие, длиной около 1 мкм, клетки овальной и клиновидной формы. Размножается организм почкованием. Форма клеток связана с циклом развития: отпочковавшиеся клетки имеют округлую форму, а перед началом почкования—грушевидную. Скоплений клеток Nitrobacter не образует.
Единственный субстрат окисления для Nitrobacter—нитриты. Полученная в процессе окисления энергия расходуется на восстановление углекислоты и построение собственного тела. Nitrobacter весьма чувствителен к неблагоприятным условиям среды. Концентрация нитрита натрия 5 г/л тормозит рост бактерии. Особенно сильно токсичность NaNO2 для Nitrobacter проявляется при недостатке кислорода.
В кислой среде Nitrobacter не развивается, так как недиссоциированная молекула азотной кислоты ядовита. В щелочной среде на Nitrobacter отрицательно влияет недиссоциированный аммиак. По этой причине Nitrobacter развивается в узких пределах нейтральных значений рН.
В природных условиях нитрифицирующие бактерии способны поглощать только тот аммиак, который не использовался другими организмами. Поэтому на интенсивность нитрификации влияет соотношение углерода и азота в среде. Пока есть избыток органических веществ, аммиак расходуется конкурентами нитрификаторов в процессах конструктивного обмена. Гетеротрофные микроорганизмы к тому же усиленно поглощают необходимый нитрифицирующим бактериям кислород. После того как органические вещества минерализуются и накапливается аммиак, создаются благоприятные условия для развития, Nitrosomonas. В то же время избыток аммиака препятствует развитию Nitrobacter, которое начинается только после окисления избытка аммиака.
Отношение нитрифицирующих бактерий к органическим веществам дало возможность использовать их в качестве индикаторов окончания процесса биологической очистки на очистных сооружениях. До тех пор, пока в очищаемой жидкости присутствуют органические соединения и интенсивно развиваются гетеротрофные бактерии, нитрификация подавлена, появление же нитритов свидетельствует о том, что основная часть органических веществ уже минерализована. Следует иметь в виду, что при достаточной концентрации солей аммония или аммиака процессы нитрификации могут осуществляться в весьма загрязненной жидкости или почве. Так, на полях орошения и фильтрации обычно наблюдается интенсивная нитрификация.
