
- •Введение
- •Часть I строение и физиология микроорганизмов
- •Глава I. Строение и принципы систематики микроорганизмов
- •Бактерии
- •Неклеточные формы жизни
- •Водоросли и водные грибы
- •Простейшие
- •Глава II. Химический состав клетки
- •Вода и минеральные соли
- •Органические вещества клетки
- •Синтез белка
- •Мутагенез
- •Глава. III. Ферменты
- •Ферменты—биологические катализаторы
- •Строение и свойства ферментов
- •Принципы классификации ферментов
- •Окислительно-восстановительные ферменты (оксиредуктазы)
- •Регуляция синтеза ферментов
- •Глава IV. Получение энергии микроорганизмами Энергетический и конструктивный обмены
- •Получение энергии литотрофами
- •Получение энергии органотрофами
- •Взаимосвязь процессов обмена в организме
- •Глава V. Закономерности роста и развития микробных культур Рост, развитие, размножение
- •Понятие об абсолютной и относительной скорости роста
- •Особенности выращивания микроорганизмов в проточных культурах
- •Фазы развития микробной культуры
- •Влияние лимитирующих факторов на скорость роста
- •Скорость роста и физиологическая активность
- •Глава VI. Влияние внешних факторов на микроорганизмы Влияние температуры
- •Влияние влажности
- •Влияние лучистой энергии
- •Влияние осмотического давления
- •Активная реакция среды и окислительно-восстановительный потенциал
- •Часть II участие микроорганизмов в превращении веществ
- •Глава VII. Круговорот углерода
- •Распространение микроорганизмов в природе
- •Круговорот углерода и участие в нем микроорганизмов
- •Глава VIIII. Расщепление органических соединений в анаэробных условиях
- •Сбраживание углеводов
- •Маслянокислое брожение
- •Cбраживание жиров
- •Анаэробное расщепление белков
- •Глава IX. Расщепление органинеских соединений в аэробных условиях
- •Окисление углеводов
- •Окисление этанола. Получение уксусной кислоты
- •Окисление жиров
- •Окисление углеводородов
- •Расщепление азотсодержащих соединений
- •Глава X. Превращение соединений азота микроорганизмами Нитрификация
- •Денитрификация
- •Фиксация молекулярного азота
- •Глава XI. Превращение соединений серы микроорганизмами
- •Окисление соединений серы
- •Восстановление соединений серы
- •Глава XIII. Превращение соединений металлов микроорганизмами
- •Окисление соединений записного железа
- •Окисление соединений марганца
- •Выщелачивание металлов из руд
- •Часть III загрязнение и самоочищение водоемов
- •Глава XIIII. Экологические системы пресных водоемов Понятие экосистемы
- •Роль окружающей среды в формировании экосистемы
- •Особенности речных экосистем
- •Особенности озерных экосистем
- •Особенности экосистем водохранилищ
- •Глава XIV. Загрязнение водоемов
- •Характеристика основных видов загрязнения
- •Виды воздействия сточных вод на водоемы
- •Глава XV. Загрязнение водоемов и распространение водных инфекций
- •Понятие инфекции
- •Распространение инфекции
- •Водные инфекции
- •Понятие иммунитета
- •Противоэпидемические мероприятия
- •Глава XVI. Круговорот веществ и энергии в водоемах. Самоочищение водоемов
- •Поступление органических веществ в водоем с водосборной площади
- •Cинтез первичной продукции в водоеме
- •Превращение и деструкция органического вещества
- •Роль отдельных групп гидробионтов в самоочищении водоемов
- •Глава XVIII. Оценка степени загрязненности водоема Классификация водоемов по степени загрязненности
- •Санитарно-бактериологический анализ
- •Часть IV биологические процессы в системах Глава XVIII. Биологические помехи в водоснабжении
- •Помехи, вызываеалые аллохтонными организмами
- •Помехи, вызываемые автохтонными организмами
- •Влияние обрастаний на качество воды и материал труб
- •Меры борьбы с биологическими помехами
- •Глава XIX. Население очистных сооружений канализации
- •Глава XX. Экологические системы очистных сооружений канализации
- •Экосистемы искусственных аэрационных очистных сооружений
- •Экологические системы естественных аэрационных очистных сооружений
- •Экосистемы анаэробных очистных сооружений
- •Литература
- •Оглавление
Анаэробное расщепление белков
Первым этапом расщепления белков является их гидролиз с помощью протеолитических ферментов—так называемый протеолиз. В результате протеолиза белки распадаются на отдельные аминокислоты. Протеолитическими ферментами обладают многие виды рода Closlridium: Cl. sporogenes, С1. botulinum, Cl. putrificum и др. Эти бактерии сбраживают аминокислоты в соответствии с реакцией Стикленда. Стикленд установил, что некоторые аминокислоты могут играть роль донора водорода, а другие—его акцептора. Так, строгий анаэроб Cl. sporogenes может развиваться при отсутствии углеводов на смеси аминокислот аланина и глицина. Но каждую из них аминокислот в отдельности микроорганизм использовать не в состоянии. В дальнейшем было установлено, что аминокислоты аланин, лейцин, налип, фенилаланин, серии, гистидин, изолейцин, метионин, орнитин, цистеин, аспарагиновая кислота и глутаминовая кислота являются донорами водорода, а глицин, пролин и аргинин—акцепторами. Реакции Стикленда протекают и соответствии с уравнениями:
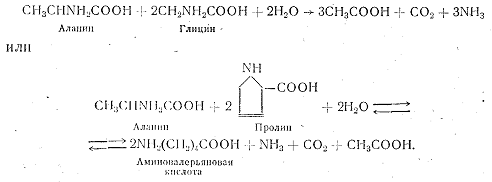
Некоторые аминокислоты, такие, как глутаминовая кислота, тирозин, орнитин и триптофан, способны выступать и в роли донора, и в роли акцептора водорода. Они могут сбраживаться и поодиночке:
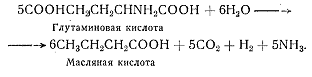
В результате дезаминирования аминокислоты превращаются в органические кислоты жирного ряда.
Другая группа клостридиев не обладает протеолитическими ферментами. Эти микроорганизмы расщепление аминокислот начинают с разрыва связей между углеродными атомами. Так, С/, meta-nomorphum расщепляет глутаминовую кислоту
![]()
В дальнейшем пировиноградная кислота превращается в масляную кислоту (см. рис. 36).
Глава IX. Расщепление органинеских соединений в аэробных условиях
Особенность дыхания по сравнению с брожением состоит в том, что в процесс дегидрирования включаются аэробные дегидрогеназы, способные передавать водород кислороду воздуха (гл. III). Расщепление органических соединений в процессе дыхания заканчивается полной минерализацией с образованием углекислоты и воды.
Окисление углеводов
Все без исключения организмы хорошо усваивают глюкозу. В клетке постоянно присутствуют ферменты, расщепляющие ее. Это и понятно, так как глюкоза—промежуточный продукт расщепления и синтеза различных соединений. Другие гексозы различными видами микроорганизмов усваиваются по-разному. Например, галактоза используется не всеми микроорганизмами. Ферменты, необходимые для ее расщепления, относятся к числу индуцировайных. Пентозы также используются не всеми видами, причем ксилоза усваивается лучше, чем арабиноза. При одновременном присутствии в среде различных Сахаров они извлекаются микроорганизмами поочередно.
Полисахариды расщепляются специализированными группами микроорганизмов. Механизм расщепления углеводов на первой стадии большей частью такой же, как и в анаэробных условиях. Конечный продукт расщепления анаэробной стадии—пировиноградная кислота, которая в процессах дыхания подвергается окислительному декарбоксилированию, осуществляемому группой ферментов. При этом выделяется энергия, запасаемая в макроэргических связях, образуется уксусная кислота и выделяется СО2.
![]()
Другая молекула пировиноградной кислоты под действием ферментов конденсируется с молекулой СО2 и образует щавелевоуксусную кислоту. Эта реакция обратима, и щавелевоуксусная кислота, теряя СО2, может вновь превращаться в пировиноградную (рис.40).
Фермент цитратсинтетаза переносит остаток уксусной кислоты на щавелевоуксусную кислоту, в результате чего образуется лимонная кислота. Активной группой цитратсинтетазы служит кофермент А (КоА). Образовавшаяся лимонная кислота включается в цикл превращений, в результате которых вновь образуется щавелевоуксусная кислота, реагирующая с уксусной кислотой. Цикл замыкается. В течение цикла высвобождаются две молекулы СО2, а всего при расщеплении глюкозы выделяются три молекулы СО2. Три остальных атома углерода, входивших в молекулу глюкозы, вступают в следующий цикл в составе щавелевоуксусной кислоты. В результате все атомы углерода, содержащиеся в глюкозе, оказываются окисленными до СО2.
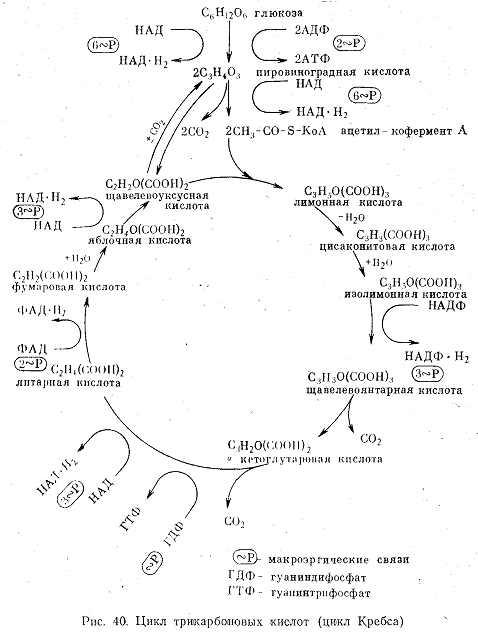
Энергетический баланс позволяет сравнить эффективность анаэробного и аэробного окисления глюкозы. При расщеплении 1 г/моль глюкозы до пировиноградной кислоты в анаэробных условиях образуются две молекулы АТФ и две молекулы НАД восстанавливаются в НАД·Н2. На каждую пару электронов, прошедших от НАД до кислорода, образуются три макроэргические связи. Таким образом, 2НАД·Н2 дали еще 6 молекул АТФ. 2НАД·Н2 образовалось при превращении пировиноградной кислоты в ацетил-КоА. Это еще 6 АТФ. В цикле Кребса дегидрирование имело место в четырех реакциях. В трех случаях Н+ присоединился к НАД, это давало 3х3=9 АТФ. В четвертом случае акцептором служил ФАД. Передача водорода от ФАД·Н2 к кислороду соответствует по выделению энергии двум макроэргическим связям. Кроме того, при декарбоксилировании α-кетоглутаровой кислоты выделилась энергия, позволившая гуаниндифосфату (ГДФ) присоединить одну молекулу фосфорной кислоты и превратиться в гуанинтрифосфат ГТФ—еще одна макроэргическая связь. Всего в цикле Кребса при расщеплении 1 г/моль ацетил-КоА выделяется энергия, соответствующая 12 макроэргическим связям, а так как из молекулы глюкозы получаются 2 молекулы пировиноградной кислоты и соответственно 2 молекулы ацетил-КоА, то, следовательно, 12АТФ·2=24АТФ. Таким образом, при полном окислении 1 г/моль глюкозы до СО2 и Н2О выделилась энергия, соответствующая 38 макроэргическим связям, что эквивалентно 1100÷1600 кДж. Из них только две молекулы АТФ приходятся на анаэробную стадию окисления. Отсюда следует, что аэробное окисление, или дыхание, энергетически намного эффективнее анаэробного. Как видно из рис. 40, в цикле превращений большую роль играют трикарбоновые и дикарбоновые кислоты, поэтому цикл аэробного окисления называется циклом трикарбоновых и дикарбоновых кислот, или циклом Кребса.
Наряду с циклом трикарбоновых кислот микроорганизмы способны превращать пировиноградную кислоту и другим путем. Процесс происходит с участием глиоксилевой кислоты и поэтому называется циклом глиоксилевой кислоты. В этом цикле также участвуют трикарбоновые кислоты и образуется щавелевоуксусная кислота, но если первый цикл приводит к выделению свободной углекислоты, то второй способствует синтезу янтарной кислоты. Оба цикла тесно связаны друг с другом, и соединения, образовавшиеся в одном из циклов, могут участвовать и в другом.
ОКИСЛЕНИЕ КЛЕТЧАТКИ
В аэробных условиях клетчатка расщепляется бактериями, грибами и актиномицетами. Среди бактерий основную роль, играют скользящие бактерии, отнесенные к порядкам Myxobacteriales и Cytophagales. Представители порядка Myxobacteriales обладают некоторыми особенностями, отличающими их от всех других бактерий: они имеют оформленное ядро. Оболочка их клеток более гонкая, чем у других бактерий, и слабее окрашивается красителями. У миксобактерий есть ряд особенностей в процессе размножения. Они делятся перетяжкой, а не образуют перегородку, как другие бактерии. Цикл развития у них более сложен. В зрелом, возрасте клетки имеют форму палочек. По мере старения они сжимаются и образуют шарики, называемые, микроцистами. Микроцисты менее устойчивы, чем бактериальные споры. Миксобактерии не обладают жгутиками и передвигаются ползанием. По-видимому, такое движение следствие неравномерного выделения слизи поверхностью клетки.
В отличие от многих микроорганизмов миксобактерии способны окислить целлюлозу кислородом, минуя анаэробную стадию. В результате воздействия миксобактерии на клетчатку образуются углекислота, вода и накапливается слизистая масса, содержащая продукты неполного окисления.
Миксобактерии предпочитают целлюлозу всем другим органическим источникам питания. Для усвоения ее необходимы экзоферменты, гидролизующие сложные молекулы полимера. У миксобактерий, по-видимому, такие ферменты имеются, но в окружающую среду они не выделяются. Клетчатка расщепляется только при непосредственном, контакте миксобактерии с клетками. При этом они не образуют колоний на поверхности фильтровальной бумаги пли других субстратов, содержащих целлюлозу, но располагаются непосредственно на волокнах (рис. 41). Среди бактерий, окисляющих целлюлозу, преобладают представители трех родов: Cytophaga, Sporocytophaga и Sorangium. Первые два организма представляют собой топкие палочки с заостренными концами (см. рис. 41). Отличие между ними заключается в том, что первый род не образует микроцист. Представители рода Sorangium имеют вид палочек с закругленными концами. Они способны к образованию микроцист. Несколько десятков микроцист, покрываясь общей слизистой оболочкой, формируют цисты. Представители родов Cytophaga и Sporocytophaga цист не образуют,
Cytophaga и Sporocyiophaga в основном используют клетчатку. Sorangium усваивает и другие органические соединения.
Помимо миксобактерии, активно используют клетчатку вибрионы из рода Cellvibrio. Они образуют на клетчатке обширные зоны желто-зеленых тонов. Другие виды бактерий, например из рода Pseudomonas, способны окислять клетчатку при отсутствии более простых органических соединений.
Г рибы
родов Fusarium,
Trichoderma
и др. также интенсивно разлагают
целлюлозу. В отличие от миксобактерий
грибы выделяют ферменты, гидролизующие
целлюлозу, в окружающую среду.
рибы
родов Fusarium,
Trichoderma
и др. также интенсивно разлагают
целлюлозу. В отличие от миксобактерий
грибы выделяют ферменты, гидролизующие
целлюлозу, в окружающую среду.
Процессы разложения целлюлозы играют очень большую роль в круговороте углерода. В природных условиях благодаря деятельности целлюлозоразлагающих микроорганизмов древесина и растительные остатки вовлекаются в круговорот веществ. На сооружениях биологической очистки эти же микроорганизмы окисляют целлюлозное волокно, содержащееся в стоках целлюлозно-бумажных предприятий, бумажных фабрик и других производств.
Отрицательная роль целлюлозоразрушающих микроорганизмов и особенно грибов заключается в порче обмоток радиоаппаратуры и кабелей, мачт, шпал (обычно в тропических странах), в порче книг. Для борьбы с целлюлозными микроорганизмами применяют различные антисептики.
ОКИСЛЕНИЕ ГЕМИЦЕЛЛЮЛОЗЫ
В состав древесины и растительных остатков наряду с клетчаткой входят гемицеллюлозы и лигнины. В природных условиях гемицеллюлозы окисляются даже более активно, чем целлюлоза. Способностью к расщеплению гемицеллюлоз обладают многие виды: среди бактерий—Bacillus, Cytophaga, Sporocytophaga, среди грибов—Aspergillus, Polyporus и др. В почвах состав микроорганизмов, расщепляющих гемицеллюлозу, определяется реакцией среды: в кислой почве преобладают грибы, в нейтральной и щелочной—бактерии.
Бактерии, расщепляющие гемицеллюлозы, в большом количестве обнаружены в аэротенках, очищающих сточные воды целлюлозно-бумажных комбинатов.
ОКИСЛЕНИЕ КРАХМАЛА
Крахмал откладывается в растительных клетках в качестве запасного питательного вещества. Клубни картофеля, зерна злаков в основном содержат крахмал. Крахмал состоит из амилозы и амилопектина. Амилоза представляет собой неразветвленный полисахарид, образуемый молекулами D-глюкозы. Амилопектин состоит из молекул D-глюкозы, образующих разветвленную цепь, кроме того в него входят остатки фосфорной кислоты, ионы магния и кальция. Амилоза растворяется в горячей воде без набухания. Характерное синее окрашивание, которое дает крахмал при взаимодействии с иодом,— результат присутствия в крахмале амилозы. Амилопектин в горячей воде набухает, в результате чего образуется крахмалистый клейстер. Крахмалы разного происхождения отличаются друг от друга степенью разветвленности и числом молекул глюкозы, входящих в полисахарид.
Крахмал расщепляется под влиянием фермента амилазы. Этот фермент есть у многих микроорганизмов, и потому расщепление крахмала не специфично для какой-либо группы бактерий или грибов.
Технические препараты амилазы получают с помощью грибов Aspergillus oryzae. Амилазу активно продуцируют многие бактерии из родов Bacillus, Pseudomonas и др. Не образуют амилазы дрожжи, и поэтому при производстве пива из ячменя крахмал предварительно осахаривают.
В результате воздействия амилаз на крахмал из него высвобождаются молекулы глюкозы, которые в дальнейшем окисляются обычным путем.
ОКИСЛЕНИЕ УГЛЕВОДОВ В ЛИМОННУЮ КИСЛОТУ
Окисление углеводов в цикле трикарбоновых кислот может идти не до конца. Если при полном окислении конечными продуктами являются углекислота и вода, то при частичном осуществлении цикла Кребса процесс может остановиться раньше, например на стадии образования лимонной, янтарной или яблочной кислот. Такие реакции особенно характерны для грибов. Некоторые из этих процессов Имеют промышленное значение. Например, с помощью гриба Aspergillus niger на отходах сахарного производства получают лимонную кислоту, применяющуюся в медицине (для консервирования кропи), в парфюмерии, кондитерской промышленности и других отраслях хозяйства. Лимонная кислота накапливается грибом в строго определенных условиях. Имеет значение рН среды, обеспеченность питательными веществами и микроэлементами. Лимонная кислота образуется при рН 2, в.нейтральной среде образуется щавелевая кислота, а при переокислении процесс идет до образования СО2. Продуцировать кислоты способны многие представители мукоровых грибов. Они образуют глюконовую, фумаровую, янтарную, молочную и другие кислоты.
