
- •Введение
- •Часть I строение и физиология микроорганизмов
- •Глава I. Строение и принципы систематики микроорганизмов
- •Бактерии
- •Неклеточные формы жизни
- •Водоросли и водные грибы
- •Простейшие
- •Глава II. Химический состав клетки
- •Вода и минеральные соли
- •Органические вещества клетки
- •Синтез белка
- •Мутагенез
- •Глава. III. Ферменты
- •Ферменты—биологические катализаторы
- •Строение и свойства ферментов
- •Принципы классификации ферментов
- •Окислительно-восстановительные ферменты (оксиредуктазы)
- •Регуляция синтеза ферментов
- •Глава IV. Получение энергии микроорганизмами Энергетический и конструктивный обмены
- •Получение энергии литотрофами
- •Получение энергии органотрофами
- •Взаимосвязь процессов обмена в организме
- •Глава V. Закономерности роста и развития микробных культур Рост, развитие, размножение
- •Понятие об абсолютной и относительной скорости роста
- •Особенности выращивания микроорганизмов в проточных культурах
- •Фазы развития микробной культуры
- •Влияние лимитирующих факторов на скорость роста
- •Скорость роста и физиологическая активность
- •Глава VI. Влияние внешних факторов на микроорганизмы Влияние температуры
- •Влияние влажности
- •Влияние лучистой энергии
- •Влияние осмотического давления
- •Активная реакция среды и окислительно-восстановительный потенциал
- •Часть II участие микроорганизмов в превращении веществ
- •Глава VII. Круговорот углерода
- •Распространение микроорганизмов в природе
- •Круговорот углерода и участие в нем микроорганизмов
- •Глава VIIII. Расщепление органических соединений в анаэробных условиях
- •Сбраживание углеводов
- •Маслянокислое брожение
- •Cбраживание жиров
- •Анаэробное расщепление белков
- •Глава IX. Расщепление органинеских соединений в аэробных условиях
- •Окисление углеводов
- •Окисление этанола. Получение уксусной кислоты
- •Окисление жиров
- •Окисление углеводородов
- •Расщепление азотсодержащих соединений
- •Глава X. Превращение соединений азота микроорганизмами Нитрификация
- •Денитрификация
- •Фиксация молекулярного азота
- •Глава XI. Превращение соединений серы микроорганизмами
- •Окисление соединений серы
- •Восстановление соединений серы
- •Глава XIII. Превращение соединений металлов микроорганизмами
- •Окисление соединений записного железа
- •Окисление соединений марганца
- •Выщелачивание металлов из руд
- •Часть III загрязнение и самоочищение водоемов
- •Глава XIIII. Экологические системы пресных водоемов Понятие экосистемы
- •Роль окружающей среды в формировании экосистемы
- •Особенности речных экосистем
- •Особенности озерных экосистем
- •Особенности экосистем водохранилищ
- •Глава XIV. Загрязнение водоемов
- •Характеристика основных видов загрязнения
- •Виды воздействия сточных вод на водоемы
- •Глава XV. Загрязнение водоемов и распространение водных инфекций
- •Понятие инфекции
- •Распространение инфекции
- •Водные инфекции
- •Понятие иммунитета
- •Противоэпидемические мероприятия
- •Глава XVI. Круговорот веществ и энергии в водоемах. Самоочищение водоемов
- •Поступление органических веществ в водоем с водосборной площади
- •Cинтез первичной продукции в водоеме
- •Превращение и деструкция органического вещества
- •Роль отдельных групп гидробионтов в самоочищении водоемов
- •Глава XVIII. Оценка степени загрязненности водоема Классификация водоемов по степени загрязненности
- •Санитарно-бактериологический анализ
- •Часть IV биологические процессы в системах Глава XVIII. Биологические помехи в водоснабжении
- •Помехи, вызываеалые аллохтонными организмами
- •Помехи, вызываемые автохтонными организмами
- •Влияние обрастаний на качество воды и материал труб
- •Меры борьбы с биологическими помехами
- •Глава XIX. Население очистных сооружений канализации
- •Глава XX. Экологические системы очистных сооружений канализации
- •Экосистемы искусственных аэрационных очистных сооружений
- •Экологические системы естественных аэрационных очистных сооружений
- •Экосистемы анаэробных очистных сооружений
- •Литература
- •Оглавление
Принципы классификации ферментов
Название ферментов большей частью образуется из названия того субстрата, на который действует фермент. Сахароза расщепляется, сахаразой, мочевина—уреазой, крахмал (амилоид)—амилазой и т. д. Кроме того, существуют исторически сложившиеся названия: пепсин, трипсин, птиалин (фермент, содержащийся в слюне) и др.
Некоторые ферменты получают название от реакций, которые они катализируют. Таковы гидролазы, дегидрогеназы (отнимающие водород) и т. д. Коферменты обычно называются сокращенно по первым буквам основных компонентов. Например, уже упоминавшийся никотинамидадениндинуклеотид сокращенно называется НАД. Он состоит как бы из двух нуклеотидов и потому называется динуклеотидом.
Международный биохимический союз предложил ввести четырехцифровой шифр для обозначения ферментов. Первая цифра обозначает порядковый номер класса фермента, вторая и третья—более мелкие подразделения, а четвертая—порядковый номер данного фермента в своей группе. Известные в настоящее время ферменты делятся на 6 классов:
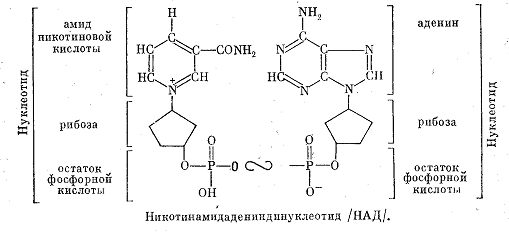
Оксиредуктазы, или окислительно-восстановительные ферменты, осуществляют перенос водорода или электронов и катализируют окислительно-восстановительные реакции, протекающие при дыхании и брожении.
Трансферазы, или ферменты переноса, катализируют перенос целых атомных группировок, например, остатков фосфорной кислоты, остатков аминокислот и т. д. от одного соединения к другому. Пример катализируемой реакции:
![]()
Гидролазы катализируют гидролиз, т. е. расщепление при участии воды сложных органических соединений на более простые. Основной тип катализируемой реакции:
![]()
4. Лиазы катализируют негидролитическое отщепление каких-либо групп от субстратов по типу:
![]()
Пример:
![]()
5. Изомеразы катализируют превращение органических соединений в их изомеры. Пример реакции:
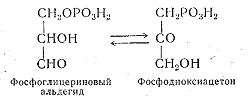
6. Лигазы, или синтетазы, катализируют соединение двух молекул, протекающее с поглощением энергии и сопровождающееся превращением АТФ в АДФ. При этом фосфорная кислота выделяется в свободном состоянии. Пример реакции, катализируемой лигазой (пируваткарбоксилазой);
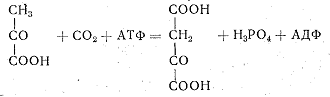
К этой группе относятся ферменты, катализирующие присоединение остатков аминокислот к транспортной рибонуклеиновой кислоте при синтезе белка.
Все перечисленные группы ферментов играют очень важную роль в жизни любого организма, но для процессов окисления органических соединений особенно важны оксиредуктазы, поэтому им необходимо уделить особое внимание.
Окислительно-восстановительные ферменты (оксиредуктазы)
К этой группе ферментов относятся: 1) дегидрогеназы, отнимающие водород от окисляемого субстрата, 2) каталазы, расщепляющие перекись водорода, 3) пероксидазы, использующие перекиси для окисления различных соединений.
Окисление субстрата путем дегидрирования представляет собой самый распространенный в живой природе способ окисления. Схематически реакция дегидрирования может быть показана уравнением:
![]()
Субстрат (S), отдающий водород, называется донатором, или донором, а фермент, принимающий водород,— его акцептором. Фермент, принявший водород, передает его другим акцепторам: соответствующим ферментам—дегидрогеназам, различным органическим веществам или кислороду воздуха. В любом случае окисление субстрата непременно сопровождается сопряженным восстановлением какого-либо соединения, т. е. реакция является окислительно-восстановительной.
Дегидрогеназы, как все ферменты, специфичны и называются по имени окисляемого субстрата: дегидрирующие этиловый спирт—алкогольдегидрогеназой, изолимонную кислоту—изоцитратдегидрогеназой и т. д.
Все известные дегидрогеназы делятся на две большие группы: анаэробные, не способные использовать в качестве акцептора водорода кислород воздуха, и аэробные, способные передавать водород кислороду воздуха.
Анаэробные дегидрогеназы представляют собой двухкомпонентные ферменты. Их кофермент обладает высокой реакционной способностью. Он отнимает водород от окисляемого субстрата и превращается в восстановленную форму НАД·Н2.
![]()
Кофермент других анаэробных дегидрогеназ отличается от НАД тем, что имеет на один остаток фосфорной кислоты больше. В соответствии с этим он называется никотинамидадениндинуклеотидфосфат или сокращенно НАДФ. Так же, как НАД, НАДФ отнимает водород от окисляемого субстрата и превращается в восстановленную форму НАДФ·Н2.
Свой водород анаэробные дегидрогеназы передают аэробным дегидрогеназам или различным органическим соединениям. НАД·Н2, например, способен передать водород уксусному альдегиду, который при этом превращается в этиловый спирт, а фермент переходит в окисленную форму и снова может вступить в реакцию с субстратом. Анаэробные дегидрогеназы, отнимающие водород от окисляемого субстрата, называются первичными деги-дрогеназами. Первичные дегидрогеназы НАД и НАДФ в клетке находятся в состоянии динамического равновесия. Под влиянием специального фермента они способны превращаться друг в друга:
![]()
К аэробным дегидрогеназам в числе других относятся ферменты, содержащие в своей активной группе рибофлавин, витамин В2. Эти ферменты называются флавопротеидами (флавус—желтый). В окисленной форме они имеют желтый цвет, в восстановленной—бесцветны. Среди флавиновых коферментов наибольшее распространение имеют флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД).
ФМН входит в состав очень широко распространенного и хорошо изученного желтого дыхательного фермента, который играет важную роль в окислении углеводов. Субстратом для желтого фермента служит исключительно анаэробная дегидрогеназа и поэтому он называется дегидрогеназой восстановленного НАДФ. Он стоит вторым в последовательной цепочке дегидрогеыаз.
![]()
ФАД—это активная группа ферментов, катализирующих окисление аминокислот. Восстановленные формы некоторых флавиновых ферментов способны передавать водород кислороду воздуха, но большинство передает его другим аэробным дегидрогеназам.
Аэробные дегидрогеназы, которые в качестве акцептора водорода используют исключительно кислород, называются оксидазами. При восстановлении оксидазами кислорода образуются вода или перекись водорода. Субстратом для оксидаз служат восстановленные формы анаэробных и аэробных дегидрогеназ, а также различные органические соединения. Среди оксидаз особенно большое значение имеют полифенолоксидаза—компонент полифенольной системы и цитохромоксидаза, образующая вместе с цитохромами цитохромную систему.
Полифенольная система состоит из хинона, полифенола и полифенолоксидазы. Хинон может служить акцептором водорода для дегидрогеназ. При этом он восстанавливается в полифенол. Полифенолоксидаза отнимает водород от полифенола и передает его кислороду воздуха. Полифенол при этом превращается в хинон и снова воспринимает водород от дегидрогеназы, Путь атомов водорода в полифенольной системе можно представить следующей схемой:
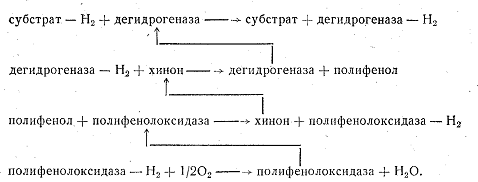
Полифенолоксидаза обнаружена в грибах, высших растениях и некоторых бактериях. Она способна окислять моно-, ди- и трифенолы. Полифенольная система имеет важное значение в процессах дыхания растений.
Цитохромной системе принадлежит основная роль в передаче водорода от анаэробных и флавиновых дегидрогеназ молекулярному кислороду воздуха. В состав цитохромной системы входят убихиноны (жирорастворимые хиноны) и четыре цитохрома, представляющие собой протеиды, простетическая группа которых содержит железо. Железо цитохромов легко принимает и отдает электроны, т. е. легко переходит из окисной формы в закисную и обратно. Суть окислительно-восстановительных реакций, осуществляемых цитохромами, заключается в том, что один из них отнимает электрон от атома водорода, удерживаемого восстановленными формами анаэробных или флавиновых дегидрогеназ, и передает его другим цитохромам. Последний в цепочке цитохромов—фермент цитохромоксидаза. Он передает электрон кислороду воздуха и тем самым активирует его. Такой активированный кислород вступает в реакцию с ионизированным атомом водорода, образуя воду или перекись водорода. Таким образом, цитохромы не участвуют в переносе атомов водорода, а передают только электроны, меняя при этом свою валентность.
Роль цитохромов в окислительных процессах иллюстрируется следующей схемой:
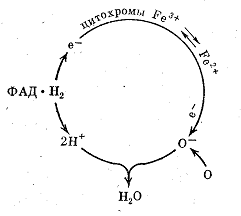
Цитохромы, по-видимому, являются универсальной ферментативной системой. Они обнаружены в клетках животных, растений и бактерий. Они участвуют в процессах дыхания, фотосинтеза и хемосинтеза.
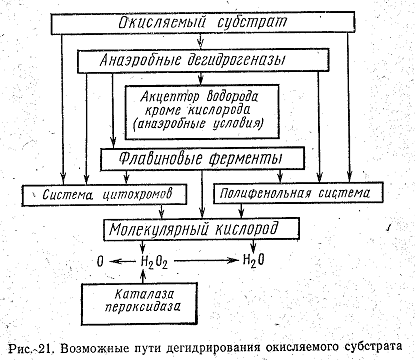
На рис. 21 показаны возможные пути переноса атомов водорода, осуществляемые дегидрогеназами. Как видно из схемы, путь атома водорода от субстрата до кислорода воздуха может быть различным. Рассматривая схему, следует иметь в виду специфичность ферментов и что один и тот же субстрат не всегда окисляется всеми представленными на схеме ферментами. Из схемы видно, что конечным акцептором водорода может быть не только кислород воздуха, но и органические соединения. Следует обратить внимание также на то, что даже в аэробных процессах первая стадия окисления может осуществляться анаэробными дегидрогеназами. Этот путь окисления у большинства микроорганизмов преобладает над всеми другими.
Помимо дегидрогеназ к оксиредуктазам относятся ферменты пероксидаза и каталаза. Обе они представляют собой двухкомпонентные ферменты, в активную группу которых входит трехвалентное железо. Различия в их каталитической функции связаны с особенностями белков-носителей.
Пероксидаза способна окислять различные органические соединения, используя кислород перекиси водорода или органических перекисей. Пероксидаза окисляет полифенолы, ароматические амины и играет важную роль в окислительных процессах,
протекающих в организме. Каталаза расщепляет перекись водорода на воду и молекулярный кислород:
![]()
препятствуя накоплению в организме ядовитой перекиси водорода и тем самым предохраняя клетки от отравления.
