- •1)Классификация орг. Соед.
- •2)Гибридизация ао.
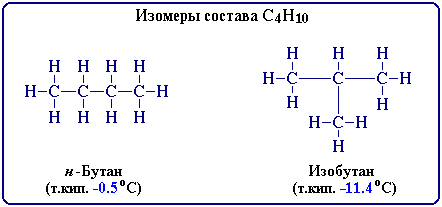
- •3)Изомерия
- •4)Алканы. Строение св.
- •5)Алкены
- •6)Алкины
- •7)Алкадиены
- •Реакция электрофильного присоединения(ае) более характерна для алкадиенов.
- •Полимеризация диеновых углеводородов (см. Полимеризация).
- •8)Циклоалканы
- •1. Циклопропан и циклобутан способны присоединять бром :
- •2. Циклопропан, циклобутан и циклопентан могут присоединять водород, давая соответствующие нормальные алканы. Присоединение происходит при нагревании в присутствии никелевого катализатора :
- •9)Циклоалканы и терпены. Свойства применение
- •10)Арены.
- •11)Галогенпроизводные ув.
- •12)Механизмы реакций в орг.Химии
- •13)Классификация реагентов.
- •2. Структурообразующие коллоиды — материалы, придающие тиксо-тропные свойства раствору. Это неорганические коллоиды — глины (бентонит, палыгорскнт, асбест), а для растворов на нефтяной основе—
- •14)Эффекты заместителей.Индуктивный метожд
- •15)Нефть-природный источник ув
- •16)Основные теории происхождения нефти
- •18)Фракционный состав нефти
- •19)Бензин. Октановое число
- •20)Крекинг
- •21)Общее представление о механизмах термичского и кат крекинга.
- •22)Риформинг. Виды
- •23)Пиролиз. Назначение пиролиза
- •24)Полимеризация
- •26)Полимеры на основе алкенов
1)Классификация орг. Соед.
В зависимости от строения углеродной цепи органические соединения делят на ациклические и циклические.
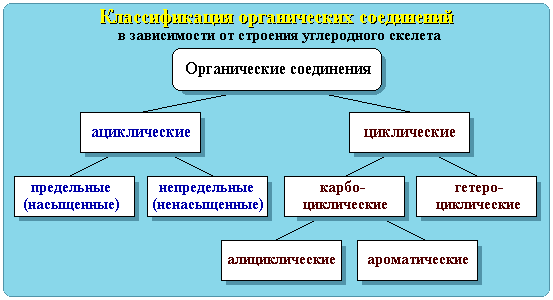 Ациклические
соединения - соединения с открытой
(незамкнутой) углеродной цепью. Эти
соединения называются также алифатическими.
Ациклические
соединения - соединения с открытой
(незамкнутой) углеродной цепью. Эти
соединения называются также алифатическими.
Среди
ациклических соединений различают
предельные
(насыщенные),
содержащие в скелете только одинарные
связи C-C и непредельные
(ненасыщенные), включающие кратные связи
C=C и C![]() C.
C.
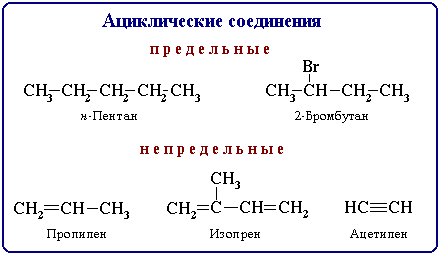
Ациклические соединения подразделяют также на соединения с неразветвленной и разветвленной цепью. В этом случае учитывается число связей атома углерода с другими углеродными атомами.
Циклические соединения - соединения с замкнутой углеродной цепью.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения. Карбоциклические соединения содержат в цикле только атомы углерода. Они делятся на две существенно различающихся по химическим свойствам группы: алифатические циклические - сокращенно алициклические - и ароматические соединения.
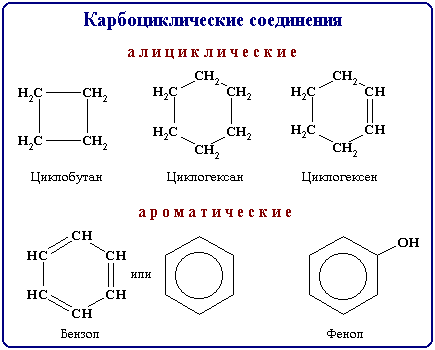
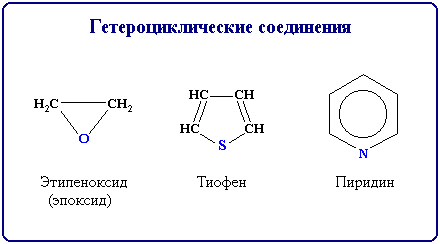
Гетероциклические соединения содержат в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (от греч. heteros - другой, иной) - кислород, азот, серу и др.
2)Гибридизация ао.
ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ - выравнивание длин хим. связей и валентных углов при образовании хим. связей валентными s-, p-, d- и т.д. электронами (атомными орбиталями) одного атома. Г. а. о. описывает возбуждённые состояния атома в хим. соединении.
sp-гибридизация
Происходит при смешивании одной s- и одной p-орбиталей. Образуется две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра атома углерода. Две оставшиеся негибридные p-орбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются неподелёнными парами электронов
sp2-гибридизация
Происходит при смешивании одной s- и двух p-орбиталей. Образуется три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей
sp3-гибридизация
Происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp3-гибридные орбитали. Могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.
Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28', что соответствует наименьшей энергии отталкивания электронов. Так же sp3-орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов
3)Изомерия
Изомерия (от др.-греч. ἴσος — «равный», и μέρος — «доля, часть») — явление, заключающееся в существовании химических соединений (изомеров), одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам.
В зависимости от характера отличий в строении изомеров различают структурную и пространственную изомерию.