
Вода властивості та функції
Які властивості води?
Серед неорганічних сполук живих організмів особлива роль належить воді. Вода є основним середовищем, у якому відбуваються процеси обміну речовин та перетворення енергії. Вміст води в більшості живих організмів становить 60-70%, а в деяких (наприклад, у медуз) до 98%. Вода утворює основу внутрішнього середовища живих організмів (крові, лімфи, міжклітинної рідини). Які функції води в клітині?
Вода визначає внутрішньоклітинний тиск (тургор) та об'єм клітин. Вона здатна формувати водну оболонку навколо певних сполук (наприклад, білків), що запобігає їхній взаємодії між собою. Таку воду називають зв'язаною (структурованою). її частка становить 4-5% від загальної кількості води в організмі. Іншу частину води (95-96%), не зв'язану з іншими сполуками, називають вільною. Саме вільна вода є універсальним розчинником, кращим, ніж більшість інших рідин.
Залежно від того, розчиняються певні сполуки у воді чи ні, їх умовно поділяють на гідрофільні, або полярні, та гідрофобні, або неполярні. До гідрофільних (від грец. хідор - вода та філіа - люблю) сполук, здатних розчинятись у воді, належить більшість солей, наприклад, кухонна сіль (NаСІ). Вода розчиняє більшість речовин, які містять групи (-ОН, -СООН та ін.), здатні іонізуватися (тобто розпадатися на електрично заряджені частинки) під час взаємодії з нею.
Гідрофобні (від грец. фобос - страх) сполуки (майже всі жири, деякі білки та ін.) містять неполярні групи (-СН, -СН2СН3 та ін.), які не взаємодіють з водою, тому в ній не розчиняються.
Вода як універсальний розчинник відіграє надзвичайно важливу роль у живих організмах, оскільки більшість біохімічних реакцій відбувається у водних розчинах. Надходять речовини у клітини та виводяться з них продукти життєдіяльності також переважно в розчиненому вигляді. Вода бере безпосередню участь у реакціях гідролізу (від грец. лізіс - розкладання) - розщеплення органічних сполук з приєднанням до місця розриву іонів молекули води (Н+ та ОН-).
Основні положення клітинної теорії
2. Положення клітинної теорії Шлейдена-Шванна
Всі тварини й рослини складаються з клітин.
Ростуть і розвиваються рослини і тварини шляхом виникнення нових клітин.
Клітина є найменшою одиницею живого, а цілий організм - це сукупність клітин.
3. Основні положення сучасної клітинної теорії
Клітина - одиниця будови, життєдіяльності, росту і розвитку живих організмів, поза клітиною життя немає.
Клітина - єдина система, що складається з безлічі закономірно пов'язаних один з одним елементів, що представляють собою певне цілісне утворення.
Ядро - головна складова частина клітини (еукаріот).
Нові клітини утворюються тільки в результаті поділу вихідних клітин.
Клітини багатоклітинних організмів утворюють тканини, тканини утворюють органи. Життя організму в цілому обумовлена взаємодією складових його клітин.
Солі їх функція….
Фторид кальцію - Складова частина всіх сполучних тканин організму. Дисбаланс може бути причиною варикозного розширення вен, пізнього прорізування зубів, розтягувань м'язових сухожиль, карбункулів і тріщин на шкірі. Фосфат кальцію - виявлений у всіх клітинах ірідинах організму, важливий елемент шлункового соку, а також кісток і зубів. Його дисбаланс або дефіцит можуть ви кликати почуття холоду в руках і ногах, оніміння, водянку оболонок яєчок, запалення молочних залоз і пітливість ночами. Сульфат кальцію - У вигляді найдрібніших частинокє складовою частиною всіх сполучних тканин, а також клітин печінки. Дисбаланс або дефіцит можуть бути причиною висипань на шкірі, глибоких наривів або хронічних мокли виразок. Фосфат заліза - Складова частина крові та інших клітин організму, за винятком нервів. Дисбаланс або дефіцит його можуть викликати тривалий пронос або, як не дивно, запори. Застосовується також як засіб при носових кровотечах і рясних менструаціях. Хлорид калію - Виявляється в покривах і під поверхневими клітинам тіла. Дисбаланс або дефіцит можуть викликати утворення грануляції на повіках, екзему з бульбашками і бородавки. Сульфат калію - З цією сіллю взаємодіють клітини, які утворюють шкіру і вистилку внутрішніх органів. Дисбаланс або дефіцит можуть бути причиною висипань на шкірі, появи жовтого нальоту на задній поверхні язика, відчуття тяжкості і болю в кінцівках. Фосфат калію - Виявляється у всіх тканинах організму, особливо в нервових і мозкових клітинах і клітинах крові. Дисбаланс або дефіцит могуг бути причиною неправильного засвоєння жиру, погіршення пам'яті, тривоги, безсоння, слабкого і частого пульсу. Фосфат магнію - Ще один мінеральний елемент кісток, зубів, мозкових, нервових, кров'яних і м'язових клітин. Дисбаланс або дефіцит можуть бути причиною судом, невралгій, прострілів і колік. Хлорид натрію - Регулює кількість вологи в організмі і переносить воду клітинам. Дисбаланс або дефіцит можуть викликати сильне бажання солі, сінну лихоманку, водянисті виділення з очей і носа. Фосфат натрію - Емульгує жирні кислоти і утримує сечову кислоту в крові у розчиненому вигляді. Дисбаланс або дефіцит можуть викликати жовтяницю, кислий запах з рота, кислий чи мідний присмак у роті Сульфат натрію - Легкий подразник для тканин я функцій, як стимулятор природних виділень. Дисбаланс або дефіцит можуть бути причиною помірно вираженого гарячкового стану, набряків, депресії і порушень функції жовчного міхура. Кремнієва кислота - Складова частина клітин всіх сполучних тканин, а також волосся, нігтів і шкіри. Дисбаланс або дефіцит можуть бути причиною поганої пам'яті. карбункулів, випадіння волосся і ребристих вростають нігтів. Вживання продуктів із неочищених злакових забезпечує нормальну потребу в цій тканинної солі.
Трансляція (біосинтез білка)
Трансляція (біосинтез білка)
Це переклад генетичної інформації, що зберігається в м-РНК у вигляді певної послідовності кодонів, в лінійну послідовність амінокислот п / п ланцюга білка. Цей процес можна розділити на 5 стадій:
активування амінокислоти та освіта аміноацил-т-РНК (відбувається в цитоплазмі клітин);
освіта ініціюючого комплексу;
елонгація, тобто подовження п / п ланцюга;
термінация (закінчення росту п / п ланцюга) і відділення її від рибосоми.
Освіта нативної структури білка.
Активування амінокислоти відбувається в цитозолі постійно, для цього необхідні: набір амінокислот, т-РНК, специфічні для кожної амінокислоти аміноацил-т-РНКсінтетази (АРС-ази) та іони магнію як активатори цих ферментів. Процес активації складається з 2-х реакцій:
освіта аміноаціладенілата за рахунок енергії АТФ
Для цієї реакції потрібна відповідна АРСаз, яка має три ділянки в активному центрі. 1-ий ділянка не має специфічністю, він однаковий для всіх ферментів, це місце приєднання АТФ
П-ої ділянка має суворої специфічністю, сюди приєднується певна АК, по якій і називається АРСаз, наприклад, якщо вона приєднує метіонін, то називається метіоніл-т-РНК-синтетазу
Ш-й ділянка також є строго специфічним ділянкою, може з'єднатися тільки з опеределения т-РНК.
Т.О. фермент необхідний для впізнавання АК і т-РНК.
2) утворення транспорт-активованої форми амінокислоти - аміноацил-т-РНК
Сумарне рівняння реакції:
Така активна форма амінокислоти за допомогою т-РНК доставляється до рибосоми, де йде біосинтез білка. Місце кожної амінокислоти в цьому ланцюзі визначається за допомогою антикодону т-РНК.
Другий етап-освіта ініціюючого комплексу.
Для утворення ініціюючого комплексу необхідні: м-РНК, рибосома, аміноацил-т-РНК, ГТФ, іони магнію, ферменти ініціації. м-РНК з'єднується з малою субодиницею рибосоми так, що в ділянці "Р" встановлюється ініціює кодон, частіше АУГ, який кодує метіонін. Метіоніл-т-РНК приєднується до АУГ водневими зв'язками,
т-РНК своїм 4-тим центром прикріплюється до великої субодиниці рибосоми. Т.ч., створюється умова, необхідна для біосинтезу білка - цілісність рибосоми. Структура, що включає обидві субодиниці рибосоми, м-РНК з який ініціює кодоном і пов'язану з ним метіоніл-т-РНК називають ініціюючим комплексом.
Третій етап - елонгація. Ця стадія протікає стільки разів, скільки потрібно приєднати залишків амінокислот. До другого кодону, що знаходиться в ділянці "А", підходить комплементарна аміноацил-т-РНК. Антикодон т-РНК приєднується до другого кодону м-РНК. Під дією пептіділтрансферази розривається макроергічних зв'язків між АК-1 і Т-РНК-1. За рахунок цієї енергії відбувається утворення пептидного зв'язку між вуглецем карбонільної групи метіоніну і іміногрупи АК-2. Потім рибосома робить один крок по м-РНК і в ділянці "Р" виявляється дипептид. Вільна т-РНК опиняється за межами рибосоми і може знову використовуватися для транспорту своєї амінокислоти. До ділянки "А" підходить чергова аміноацил-т-РНК і якщо її антикодон відповідає кодону в цій ділянці, то відбувається приєднання аміноацил-т-РНК до антикодон і всі реакції повторяться. Так, рибосома робить крок за кроком по м-РНК, поки не буде лічена вся інформація даної м-РНК.
Четвертий етап - термінация. Вона настає тоді, коли на ділянці "А" встановлюється стоп-кодон (УАА, УАГ, УГА). Цим кодонам не відповідає ні одна амінокислота. Тому за допомогою факторів термінації відбувається відщеплення синтезованого поліпептиду від кінцевої т-РНК, відбувається дисоціація рибосоми. Якщо клітці необхідно кілька білків з однаковою структурою, то на одну м-РНК нанизується декілька рибосом, утворюючи поліс. М-РНК, відокремившись від рибосоми, гідролізується рібонуклеазою, тому тривалість життя у них невелика, але за час життя вони інтенсивно працюють, поєднуючи за 1 секунду близько 20 амінокислот.
П'ятий етап - утворення нативної структури білка (фолдінг). Утворився білок теж є незрілою молекулою і піддається дозріванню. Цей процес носить назву Посттрансляційні зміни молекули білка.
Відщепляється ініціює АК, іноді навіть пептид, який називається сигнальний. Потім дозріла молекула піддається фолдінг (придбання вторинної, третинної і четвертинної структури), тобто АК можуть гідроксильованого, якщо синтезується складний білок, то можливі реакції глікозилювання, сульфатування, приєднання металів, вітамінів і тільки після цього відбувається скручування пп ланцюгів, освіта глобули і т.д..
Матоди цитологічних досліджень
Як досліджують клітини?
Як вам уже відомо, першим приладом, за допомогою якого вивчають клітини, був світловий (оптичний) мікроскоп (мал.26). Раніше ви вже мали змогу ознайомитися з будовою і правилами роботи з цим приладом.
Методи досліджень за допомогою цього мікроскопа називають світловою мікроскопією. Так можна вивчати загальний план будови клітин та їхні окремі органели, розміром не менше ніж 200 нм.
Пригадаймо: світлова мікроскопія ґрунтується на тому, що через прозорий чи напівпрозорий об'єкт дослідження проходять промені світла, які згодом потрапляють на систему лінз об'єктива та окуляра. Лінзи зорово збільшують об'єкт дослідження. Кратність збільшення можна визначити як добуток збільшень об'єктива і окуляра. Наприклад, якщо лінзи окуляра забезпечують збільшення в 10 разів, а об'єктива - в 40, то загальне збільшення об'єкта досліджень становитиме 400 разів. Сучасні світлові мікроскопи можуть забезпечувати збільшення об'єктів у 2-3 тис. разів.
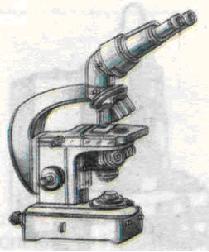
Мал. 26. Світловий мікроскоп
Клітинні структури дрібніших розмірів (наприклад, клітинні мембрани) відкрито й досліджено за допомогою електронного мікроскопа (мал. 28), винайденого у першій половині XX століття.

Мал. 28. Електронний мікроскоп
За конструкцією електронний мікроскоп нагадує світловий, але замість потоку променів світла в ньому застосовують потік електронів, які рухаються в магнітному полі. Цей потік прискорюється високою різницею потенціалів, що створюється між різними полюсами (катодом і анодом). Роль лінз виконують електромагніти, здатні змінювати напрямок руху електронів, збирати їх у пучок (фокусувати) і спрямовувати його на об'єкт дослідження. Частина електронів, проходячи через об'єкт, може відхилятись, розсіюватись, поглинатись, взаємодіяти з об'єктом дослідження або проходить крізь нього без змін. Пройшовши через досліджуваний об'єкт, електрони потрапляють на люмінісцен-тний екран, спричиняючи його свічення, або на особливий фотоматеріал, за допомогою якого зображення можна фотографувати.
Електронний мікроскоп здатний збільшувати зображення об'єктів дослідження в сотні тисяч разів (до 500 000 і більше).
Живі клітини досліджують як за допомогою методу прижиттєвого вивчення, так і в зафіксованому стані. У першому випадку можна вивчати певні процеси життєдіяльності клітини (рух цитоплазми, процес поділу тощо).
Щоб з'ясувати місце або перебіг тих чи інших біохімічних процесів у клітині, застосовують метод мічених атомів: у клітину вводять речовину, в якій один з атомів певного хімічного елемента заміщений його радіоактивним ізотопом. За допомогою спеціальних приладів, здатних фіксувати ці ізотопи, можна простежити за міграцією цих речовин у клітині та їхнім перетворенням.
Вивчаючи тонку структуру клітин, їх потрібно попередньо зафіксувати, застосовуючи особливі речовини (спирт, формалін тощо), швидке заморожування або висушування. Деякі структури фіксованих клітин зафарбовують спеціальними барвниками.
Для вивчення окремих клітинних структур застосовують метод центрифугування (від лат. центрум - центр та фуга - втеча). При цьому клітини попередньо подрібнюють і в особливих пробірках уміщують у центрифугу - прилад, здатний розвивати швидкі колові оберти. Оскільки різні клітинні структури мають неоднакову щільність, вони під час роботи центрифуги осідатимуть неодночасно й утворюватимуть шари: щільніші - швидше, і тому опиняться знизу, а менш щільні - повільніше, вони розташуються зверху. Шари, що утворилися, розділяють і досліджують окремо.
Денатурація білків
Денатурація білків (від лат. de- - Приставка, що означає відділення, видалення і лат. nature - Природа, не плутати з лат. denaturatus - Позбавлений природних властивостей) - термін біологічної хімії, що означає втрату білками їх природних властивостей ( розчинності, гідрофільності та ін) внаслідок порушення просторової структури їх молекул.
Процес денатурації окремої білкової молекули, що приводить до розпаду її "жорсткої" тривимірної структури, іноді називають плавленням молекули.
