
- •В химическом производстве. План лекции
- •1.Введение. 2.Химическое производство
- •3.Иерархическая организация процессов в химическом производстве. 3.Классификации и категории эффективности химических производств.
- •Эффективности химических производств План лекции
- •План лекции
- •1.Сырье
- •2. Классификация химического сырья
- •3. Подготовка химического сырья к переработке
- •Классификация химического сырья
- •План лекции
- •Виды использования вторичных энергетических ресурсов
- •План лекции
- •Виды типовых технологических операторов хтс
- •Классификация и условные изображения типовых технологических операторов хтс
- •Понятие идентификации хтс план лекции
- •Понятия анализа, оптимизации и синтеза хтс
- •Лекция 7 Эксергетический баланс. Классификация химических реакторов план лекции
- •Классификация химических реакторов
- •Для реализации нулевого порядка из уравнения получают
- •Уравнение материального баланса для рис-н
- •Лекция 5
- •Реактор идеального вытеснения (рив)
- •Сравнение эффективности проточных реакторов идеального смешения и идеальног вытеснения
- •Модели реакторов с неидеалной структурой потоков
- •Скорость простой необратимой реакции n-го порядка
- •Сравнение эффективности хтп при использовании
- •Модели реакторов с неидеалной структурой потоков
- •Реакторы с различным тепловым режимом
- •Лекция 6
- •Тепловая устойчивость химических реакторов
- •Лекция 7
- •1.Гетерогенные некаталитические процессы
- •2.Лимитирующая стадия. Способы определения лимитирующей стадии
- •3.Кинетические модели системы газ - твердое вещество
- •Кинетические модели гетерогенных процессов в системе «газ- твердое вещество».
- •Внешняя диффузия. В результате протекания химической реакции
- •Константа скорости гетерогенного процесса. Лимитирующая стадия
- •Лекция 8
- •1.Лимитирующая стадия – внутренняя диффузия (газ- твердое)
- •2.Способы определения лимитирующей стадии
- •3.Гетерогенные процессы «газ- жидкость»
- •Гетерогенные процессы «газ—жидкость»
- •Массопередача между газом и жидкостью
- •Кинетические модели газожидкостных реакций
- •Лекция 9
- •1.Общие представления о катализе
- •2.Технологические характеристики твердых катализаторов
- •3.Стадийность гетерогенно каталитических процессов
- •Технологические характеристики твердых катализаторов
- •Лекция 10
- •Промышленные химико-технологические процессы
- •Классификация сточных вод
- •Лекция 11
- •1.Технология связанного азота
- •2.Синтез аммиака
- •Лекция 12
- •1.Технология азотной кислоты
- •Лекция 14
- •1.Производство метанола
- •2.Синтез этанола
- •Синтез этанола
- •План лекции
- •Производство бутадиена-1,3 дегидрированием н-бутана
- •Производство фенола кумольным методом
Лекция 14
ПЛАН ЛЕКЦИИ
1.Производство метанола
2.Синтез этанола
Метиловый спирт широко применяют как растворитель, как высокооктановую добавку к моторному топливу, в производстве лаков, красителей. Кроме того, его используют в каче стве сырья для многих важных органических продуктов, показанных на схеме

Главный метод получения метанола - синтез на основе оксида углерода и водорода. Рассмотрение способа и выбор технологического режима проведены на основе классификации ХТС и ХТП. Процесс получения метанола квалифицирован как сложный, экзотермический, гетерогенно-каталитичес-кий, двусторонний, несмещаемый с химическим торможением, протекающий с уменьшением объема системы [уравнение (1)].
Из протекающих семи химических превращений - одно целевое и шесть побочных, часть из них может быть использована Для получения сопутствующих продуктов, прежде всего метана [уравнения (1) и (2)]:
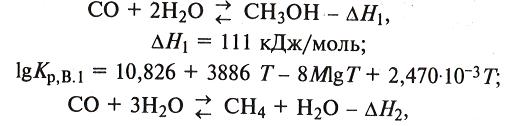
![]()
Для обеспечения высокой селективности процесс организован по циклическому методу с небольшим выходом за один проход по технологической схеме, но с высокой производительностью установки.
Процесс проводят с применением цинк-хромового катализатора (ВХпО-СггОз-СгОз), предложенным Б.Н. Долговым и А.З. Карповым [1, 10], с выходом за один проход около 4% при селективности примерно 35-95%. Синтез ведут при температуре 350-400°С и давлении 20-30 МПа, объемная скорость (35-40)-103 ч-1.
Повышение объемной скорости приводит к некоторому изменению степени превращения (X) сырья в метаны, но снижение происходит медленнее, нежели увеличение объемной скорости.
Для синтеза используют смесь с соотношением СО:Н2 1,0:1,5 или 1,0:2,5, очищенную от пентакарбонила железа в фильтре-адсорбере, заполненном активным углем. Скорость реакции определяется адсорбцией водорода на втором этапе каталитического процесса и может быть вычислена по уравнению Темкина:
![]()
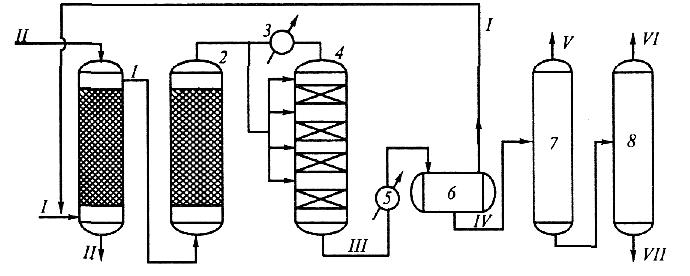
Схема 1. установка синтеза метанола:
1 - скруббер; 2 - адсорбер; 3 - теплообменник; 4 - колонна синтеза; 5 - холодильник; 6- сепаратор; 7, 8- ректификационные колонны; /- синтез-газ; //- вода; Щ- реакционные газы; IV- метанол-сырец; V'- диме-тиловый эфир; VI-метанол; УП- высшие спирты
Р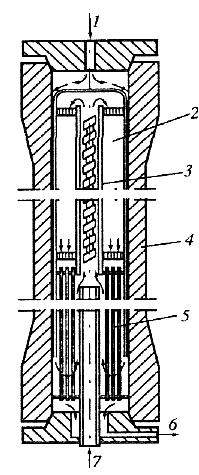 еакцию
проводят в адиабатическом реакторе
на четвертой-пятой ступенях, постепенно
снижая температуру для смещения
равновесия системы в сторону образования
метанола. Схема установки показана на
схеме 1.
еакцию
проводят в адиабатическом реакторе
на четвертой-пятой ступенях, постепенно
снижая температуру для смещения
равновесия системы в сторону образования
метанола. Схема установки показана на
схеме 1.
Синтез под давлением 1-2 МПа поступает в скруббер 1 на водную очистку от диоксида углерода, затем газ дожимают до нужного давления, очищают от пентакарбонила железа [Ре(СО)5] в адсорбере 2 и разделяют на два потока. Один поток подогревают до 400-450 °С и направляют на первую ступень синтеза (см. рис. 1 и 2). Дальнейшее охлаждение системы и образование метанола идет после добавления холодного синтез-газа, по снижающейся температуре при высокой селективности процесса на остальных трех ступенях взаимодействия. Каждая ступень работает в адиабатическом режиме.
Рис. 2. Схема колонны синтеза метанола:
1 - вход основного газа; 2 - катализатор-ная коробка; 3 - электроподогреватель; 4 -корпус колонны; 5 -теплообменник; 6 - выход газа; 7 - вход байпасного газа
Реакционные газы охлаждаются в холодильнике 5 и поступают в сепаратор 6, где конденсат отделяют от непрореагировавших газов, которые возвращают в процесс. Конденсат (метанол-сырец) направляют в ректификационную колонну 7, с верха которой отделяется диметиловый эфир. Кубовая жидкость поступает в колонну 8. В качестве дистиллята отбирают метанол с водой. Далее метанол отгоняют от воды острым паром. Из куба колонны 8 отводят смесь высших спиртов. Общий выход метанола - 85-95%. Газовые выбросы в основном составляют топливо, которое сжигают в котельных установках для получения пара. Сточные воды содержат < 3% метанола, и их направляют на биологическую очистку в аэротенках с активным илом.
