
- •8) Химические свойства алкенов. Реакции элетрофильного …..
- •1.Присоединение водорода
- •16. Химические свойства альдегидов и кетонов. Строение карбонильной группы, ее полярность, поляризуемость.Кето-енольная таутомерия в ряду жирно-ароматических и алифатических альдегидов
- •2.Присоединение водорода
- •24. Диазосоединения.Строение ароматических диазосоединений. Основные методы синтеза алифатических и ароматических диазосоединений. Синтезы с участием ароматических
- •32. Как можно разделить смесь этана, этилена и ацетилена.?
- •39. Какая реакция, характерная для альдегидов, не свойственна глюкозе?
- •50. C2h6→b→c3h6→c→ацетон
24. Диазосоединения.Строение ароматических диазосоединений. Основные методы синтеза алифатических и ароматических диазосоединений. Синтезы с участием ароматических
Диазосоединения – общее название органических веществ, содержащих группировку из двух атомов азота, связанную с одним атомом углерода. Выделяют две группы диазосоединений: ароматические диазосоединения и диазоалканы. Ароматические диазосоединения – класс органических соединений общей формулы RN2X, содержащих группировку из двух ато-
мов
азота (-N2 или -N2-), связанную только с
одним углеводородным радикалом.
Ароматические диазосоединения существуют
в виде катионов и нейтральных молекул.
Фрагмент Х
может
быть анионом сильной кислоты (Cl-, Br-,
HSO4-,BF4-, PF6-) или ковалентно-связанной
группой (-OH, -O-, -CN, CH3COO-, I-) Реакции
с выделением азота.
1.
Замещение на гидроксигруппу
Соли
диазония медленно реагируют с водой с
образованием фенолов. Реация протекает
даже в ледяном растворе солей диазония,
а при повышенных температурах является
главной реакцией солей диазония:
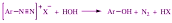 Чтобы
исключить реакции взаимодействия
образовавшегося фенола с солью диазония
(реакция азосочетания) для получения
фенола соль диазония медленно добавляют
к кипящему раствору разбавленной серной
кислоты.
2.
Замещение на галоген.
Замещение
диазогруппы на йод протекает легко при
смешении соли диазония с раствором
йодида калия:
Чтобы
исключить реакции взаимодействия
образовавшегося фенола с солью диазония
(реакция азосочетания) для получения
фенола соль диазония медленно добавляют
к кипящему раствору разбавленной серной
кислоты.
2.
Замещение на галоген.
Замещение
диазогруппы на йод протекает легко при
смешении соли диазония с раствором
йодида калия:

Реакцию
замещения диазогруппы на хлор и бром
проводят с использованием галогенидов
одновалентной меди (редокс – катализатор)
– реакция Зандмейера – и свежеприготовленных
солей диазония:
 Реакция
проходит при комнатной температуре или
при нагревании. Иногда реакцию проводят,
используя медный порошок и галогеноводород
(реакция Гаттермана). Схема реакции
предусматривает образование
радикалоподобных частиц или свободных
арильных радикалов:
Реакция
проходит при комнатной температуре или
при нагревании. Иногда реакцию проводят,
используя медный порошок и галогеноводород
(реакция Гаттермана). Схема реакции
предусматривает образование
радикалоподобных частиц или свободных
арильных радикалов:
 Методом
введения фтора в ароматическое кольцо
является реакция Шимана – нагревание
фторборатных солей диазония:
Методом
введения фтора в ароматическое кольцо
является реакция Шимана – нагревание
фторборатных солей диазония:
 3.
Замещение на CN
Замещение
диазогруппы на цианогруппу проходит
при взаимодействии солей диазония с
цианидом одновалентной меди:
3.
Замещение на CN
Замещение
диазогруппы на цианогруппу проходит
при взаимодействии солей диазония с
цианидом одновалентной меди:
 4.
Замещение на водород (дезаминирование)
Замещение
диазогруппы на водород можно провести
при восстановлении солей диазония.
Наиболее часто для восстановления
используют фосфорноватистую кислоту
Н3РО2:
4.
Замещение на водород (дезаминирование)
Замещение
диазогруппы на водород можно провести
при восстановлении солей диазония.
Наиболее часто для восстановления
используют фосфорноватистую кислоту
Н3РО2:
 Восстановление
можно проводить и используя этиловый
спирт:
Восстановление
можно проводить и используя этиловый
спирт:
 5.
Замещение на Ar.
Одним
из способов получения производных
дифенила является реакция Гомберга,
заключающаяся во взаимодействии соли
диазония с ароматическими углеводородами
в присутствии щелочи:
5.
Замещение на Ar.
Одним
из способов получения производных
дифенила является реакция Гомберга,
заключающаяся во взаимодействии соли
диазония с ароматическими углеводородами
в присутствии щелочи:
 Реакции
без выделения азота.
1.
Восстановление солей диазония в
арилгидразины
При
восстановлении солей диазония рассчитанным
количеством хлорида олова (II) при низкой
температуре или избытком сульфита
натрия при нагревании образуются
арилгидразины:
Реакции
без выделения азота.
1.
Восстановление солей диазония в
арилгидразины
При
восстановлении солей диазония рассчитанным
количеством хлорида олова (II) при низкой
температуре или избытком сульфита
натрия при нагревании образуются
арилгидразины:
 2.
Реакции сочетания.
В
соответствующих условиях соли диазония
легко реагируют с фенолами и ароматическими
аминами с образованием соединений, в
которых атомы азота диазогруппы
сохраняются. Такие соединения называют
азосоединениями, а реакцию их получения
– азосочетанием.
2.
Реакции сочетания.
В
соответствующих условиях соли диазония
легко реагируют с фенолами и ароматическими
аминами с образованием соединений, в
которых атомы азота диазогруппы
сохраняются. Такие соединения называют
азосоединениями, а реакцию их получения
– азосочетанием.
 Реакция
азосочетания протекает по механизму
реакций электрофильного замещения,
атакующим агентом является катион
диазония. Поскольку диазоний-катион
слабый электрофил, то он атакует лишь
реакционноспособные кольца, содержащие
электронодонорные группы (ОН, NH2,
NHR, NR2).
Замещение обычно происходит в п-положение
к активирующей группе, а если оно занято,
то в о-положение:
Реакция
азосочетания протекает по механизму
реакций электрофильного замещения,
атакующим агентом является катион
диазония. Поскольку диазоний-катион
слабый электрофил, то он атакует лишь
реакционноспособные кольца, содержащие
электронодонорные группы (ОН, NH2,
NHR, NR2).
Замещение обычно происходит в п-положение
к активирующей группе, а если оно занято,
то в о-положение:
 Понятие
об азокрасителях.
Азосоединения
окрашены, поскольку содержат хромофорную группу
(азогруппа), которая способствует
поглощению света в видимой области
спектра, а также ауксохромные
группы
(ОН, NH2 и
т.д.), которые углубляют цвет и способствуют
связыванию красителя с волокном. Такие
азосоединения относят к красителям.
Примерно половина используемых в
промышленности красителей относится
к азокрасителям. Они могут быть моно-,
ди-, полиазокрасителями в зависимости
от количества азогрупп, иметь окраску
от красного до зеленого цвета (зеленый,
желтый, оранжевый, красный).
Понятие
об азокрасителях.
Азосоединения
окрашены, поскольку содержат хромофорную группу
(азогруппа), которая способствует
поглощению света в видимой области
спектра, а также ауксохромные
группы
(ОН, NH2 и
т.д.), которые углубляют цвет и способствуют
связыванию красителя с волокном. Такие
азосоединения относят к красителям.
Примерно половина используемых в
промышленности красителей относится
к азокрасителям. Они могут быть моно-,
ди-, полиазокрасителями в зависимости
от количества азогрупп, иметь окраску
от красного до зеленого цвета (зеленый,
желтый, оранжевый, красный).
 Азокрасители
используются и в качестве кислотно –
основных индикаторов, например:
Метиловый
оранжевый:
Азокрасители
используются и в качестве кислотно –
основных индикаторов, например:
Метиловый
оранжевый:
 Конго
красный:
Конго
красный:

