
Растительные фенолы.
Растения способны синтезировать много тысяч соединений, содержащих один или более фенольных остатков. Эти соединения можно подразделить на несколько групп по числу атомов в углеродном скелете. Практически все фенольные соединения синтезируются по единому биосинтетичеекому пути через ключевое соединение – шикимовую кислоту (исключения: из остатков СНСО-КоА по поликетидному пути синтезируются антрахиноны и одно из ароматических колец в молекуле флавоноидов).


Простые фенолы, фенилметаноиды, фенилэтаноиды,
1. Простые фенолы (пирокатехин, пирогаллол, гидрохинон)
Простые фенолы относительно не широко распространены в природе, чаще других встречается
гидрохинон, иногда катехол (пирокатехин).

Является основным действующим веществом листьев брусники и толокнянки, в значительных количествах накапливается в листьях бадана, груши.
2 Подгруппа фенилметаноидов представлена большей частью гидроксибензойными к-ми, широко распространенных в растениях, в основном в качестве промежуточных продуктов на биосинтеческих путях, но некоторые накапливаются в растениях в значительных количествах.

Салициловая кислота и ее производные известны как противовосполительные, жаропонижающие и болеутоляющие средства (плоды малины). Из восстановленных: форм фенилметаноидов приведем в качестве примеров:

Салицин - действующее начало вытяжки из коры ивы белой, которая используется в народной медицине как противовосполительное и жаропонижающее средство.
3. Подгруппа фенилэтаноидов (С6-С2) представлена подгруппой фенилуксусных кислот, распространенных значительно меньше.
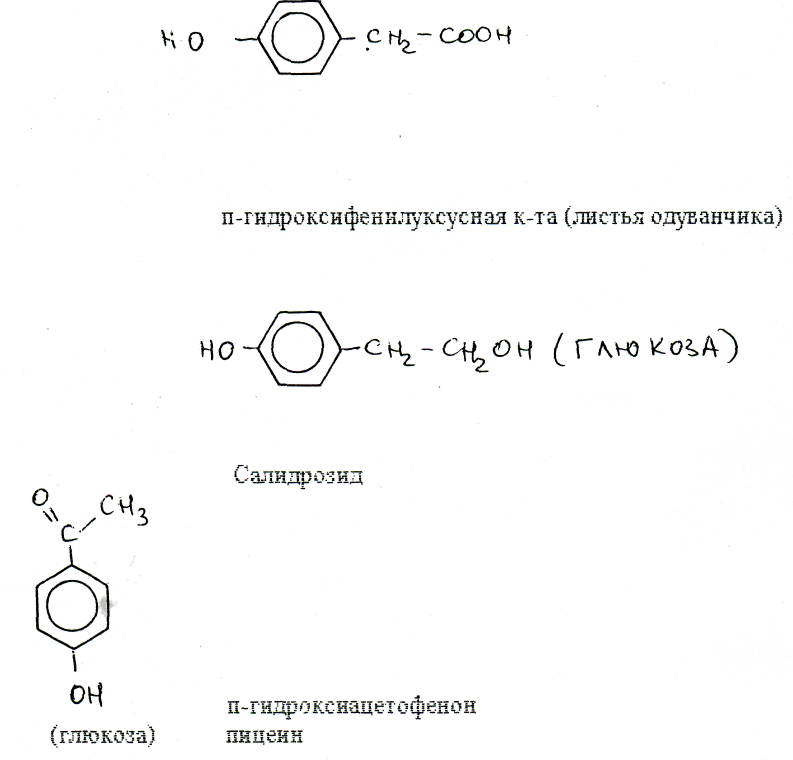
Сумма ацетофенонов в хвое ели сибирской достигает 6% с преобладанием п-гидроксиацетофенона.
Физико-химические свойства.
Свободные фенольные соединения и их гликозидные формы в индивидуальном состоянии представляют собой кристаллы, растворимые в воде, этиловом и метиловом спиртах, этилацетате, а также в водных растворах щелочей. Под действием минеральных кислот и ферментов фенологликозиды расщепляются на углевод и агликон. Гликозидные формы обладают оптической активностью.
Методы выделения из сырья.
Фенольные гликозиды извлекают из растительного материала водой и этиловым (метиловым) спиртом (96%, 70%, 40%).
Дальнейшую очистку фенолгликозидов ведут общепринятыми методами. Очистку от липофильных примесей проводят, обрабатывая водные растворы органическим растворителем (хлороформ, эфир). Сопутствующие вещества переводят в осадки. Например, так освобождаются от дубильных веществ и их флавоноидов, переводя их в осадки ацетатом свинца в фармакопейных методиках количественного определения арбутина в листьях толокнянки и брусники, и салидрозида в корнях радиолы розовой.
Для очистки фенольных соединений и выделения индивидуальных соединений используют хроматографию на силикагеле, полиамиде, целлюлозе.
Качественные реакции.
В основе, как качественных реакций, так и методов количественного определения лежат химические свойства фенольных соединений. Первое - это способность окисляться.
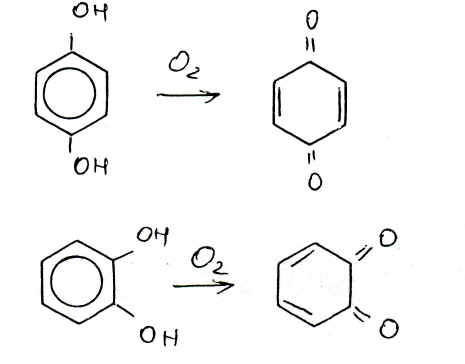
Второе - это реакции фенольного гидроксила с сульфатом закисного железа, с солями тяжелых металлов с образованием комплексных соединений и реакции диазотирования.
Реакции могут проводиться как капельно (например, с железоаммонийными квасцами в листьях толокнянки и брусники (ГФХГ)) или на хроматограммах (обнаружение салидразида по реакции с диазотированным сульфацилом (ГФХГ)). Используются и специфические реакции, например, реакция с раствором фосфорномолибденокислого Nа (синее окрашивание) или с сульфатом закисного железа (темно-фиолетовый осадок) реакция на арбутин в листьях толокнянки и брусники по ГФ XI.
Количественное определение.
Для количественного определения фенольных соединений чаще всего используют методы ФЭК, СФ и методы окислительно-восстановительного титрования (йодометрию).
Так содержание арбутина в листьях толокнянки и брусники по ГФ XI определяют йодометрическим методом, основанном на окислении йодом гидрохинона, полученного после извлечения и гидролиза арбутина.
Для фотоколориметрических определений чаще других используется реакция диазотирования. Так определяют салидрозид в корневищах с корнями родиолы розовой.
Метод СФ основан на том, что ароматическое фенольное кольцо поглощает в ближней УФ - области (при 280 нм). Так предложено определять арбутин в листьях бадана после очистки спиртового извлечения колоночной хроматографией на окиси алюминия прямой СФ при 285 км.
