
- •Лекция № 10, 11 по дисциплине «Химическая технология теплоносителя»
- •Литература:
- •1. Необходимость и этапы очистки воды
- •2. Очистка воды методом коагуляции
- •2.1. Сущность и механизм коагуляции
- •2.2. Факторы, влияющие на процесс коагуляции
- •2.3 Флокуляция
- •3. Очистка воды методом осаждения
- •3.1. Известкование воды
- •3.2. Расчет дозы извести для практического использования
- •Минимальная доза извести определяется кол-вом ионов он-, требуемых на реакции (2), (3) и (6).
- •3.3. Содоизвесткование
- •3.4. Обработка едким натром
- •4. Методы осветления воды
- •Принципиальная схема предочистки
2.2. Факторы, влияющие на процесс коагуляции
рН (особенно для Аl2(SО4)3)
Для полного гидролиза Аl2(SО4)3 необходимо рН = 5,5 – 7,5.
Если рН меньше 5,5 (кислая среда), то равновесие реакции гидролиза смещено влево.
Если рН больше 7,5, то Аl(ОН)3 начинает вести себя как кислота:
Аl(ОН)3 + ОН- АlО2- + 2Н2О
алюминат – ион
Fе(ОН)3 – не амфотерен, образуется при рН = 6 – 6,5 и может быть использован в щелочной среде. Это обусловливает использование именно FеSО4 при совмещении процессов коагуляции и известкования.
Температура: оптимальная температура для процесса коагуляции – 25 – 300С. При низких температурах происходит вялая коагуляция, причинами которой являются замедленное тепловое движение молекул, повышенная вязкость среды, уменьшение числа взаимных столкновений.
Солевой состав – особенно характер присутствующих в воде анионов. Влияние анионов проявляется в том, что с некоторыми из них положительно заряженные частицы АlОН2+, Аl(ОН)2+ , FеОН+ образуют трудно растворимые осадки. Вследствие этого концентрация этих частиц снижается, что, с одной стороны, смещает равновесие реакций гидролиза вправо, а с другой стороны, может привести к снижению процесса коагуляции.
Наименее растворимые соли дают SО4 – ионы, соли Сl- – ионов более растворимы, НСО- - осадков не образуют.
Доза коагулянта зависит от физико-химических свойств примесей воды, температуры и способа осуществления коагуляции. Определяется опытным путем.
Проводится ряд экспериментов.
при определенной температуре и заданной рН в 5 – 6 колбах помещают разные количества коагулянта; через 10 минут оценивают эффективность хлопьеобразования.
при оптимальной дозе коагулянта устанавливают оптимальное значение рН.
в третьей серии опытов определяют дозу флокулянта при оптимальных дозах коагулянта и значении рН.
Обычно
![]() =
0,5 – 1,2 мг-экв/кг
=
0,5 – 1,2 мг-экв/кг
![]() =
0,1 – 5,5 мг-экв/кг
=
0,1 – 5,5 мг-экв/кг
2.3 Флокуляция
Процесс флокуляции применяется для интенсификации процессов хлопьебразования и осаждения.
Флокуляция – процесс агрегации частиц за счет их адсорбционного взаимодействия с флокулянтами.
Флокулянты – это вещества, ускоряющие слипание агрегативно неустойчивых частиц в обрабатываемой воде, интенсифицирующие процесс образования хлопьев и увеличивающие их размеры. Сорбируясь частицами осадка, флокулянты как бы «сшивают» их и образуют сетчатую структуру, способствуя образованию крупных флокул, более тяжелых и оседающих быстрее.
Флокулянты:
а) природные:
неорганические (Н2SiО3)
органические (крахмал, карбоксилметилцеллюлоза)
б) синтетические высокомолекулярные флокулянты (ВМФ) – органические полимеры или сополимеры с разнообразными функциональными группами.
Синтетические ВМФ подразделяют на неионные, катионные и анионные соединения.
К неионным флокулянтам относится полиоксиэтилен (ПЭО), состав его элементарного звена: СН2 – СН2 – О – (М = 4 · 104 – 5 · 107).
Преимущество – индифферентность к рН раствора; недостаток – малая прочность флоккул и легкая разрушаемость при интенсивном перемешивании.
Анионные флокулянты.
Наиболее известен полиакриламид (ПАА) – полимер акриламида:
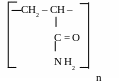
(М = 1-6 · 106)
П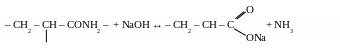 АА
гидролизуется водой, щелочами и кислотами
с образованием акриловой кислоты и ее
солей. Щелочной гидролиз протекает по
схеме:
АА
гидролизуется водой, щелочами и кислотами
с образованием акриловой кислоты и ее
солей. Щелочной гидролиз протекает по
схеме:
При этом образуются карбоксильные группы, придающие молекулам ПАА отрицательный заряд.
П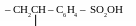 олистиролсульфокислота
– сильнокислотный анионный полиэлектролит:
олистиролсульфокислота
– сильнокислотный анионный полиэлектролит:
Катионные флокулянты.
Полиэтиленимин (ПЭИ) – состоит из звеньев двух типов:

– СН2
– СН2
– NH
–
(М = 4-11 · 104)
Полиэлектролит ВА – 2 (соли на основе поливинилтолуола). Сам вызывает коагуляцию отрицательно заряженных частиц (даже без добавления коагулянта).
Эффективность флокуляции зависит от продолжительности и интенсивности перемешивания.
Кратковременное и не очень интенсивное перемешивание способствует соединению макромолекулярных частиц дисперсной фазы, в результате чего образуются флокулы, длительное и интенсивное перемешивание вызывает сжатие флокул.
Для водоочистки более перспективными являются катионные флокулянты:
они эффективнее, чем анионные и неионные;
не требуют корректировки рН обрабатываемой воды и сами не изменяют ее рН;
не требуют дополнительного введения электролитов;
при обработке образуют более плотный осадок с невысокой влажностью.
Доза флокулянта подбирается экспериментально в зависимости от химического состава воды, концентрации органических веществ, рН, температуры, концентрации ГДП в воде. Обычно доза флокулянта – 0,1-0,2 мг/дм3
Выводы:
1. Процесс коагуляции происходит в результате нарушения агрегативной устойчивости коллоидной системы.
2. Способы нарушения агрегативной устойчивости – добавление электролитов и взаимная коагуляция.
3. На процесс коагуляции влияют рН, температура, солевой состав и доза коагулянта.
4. Для интенсификации хлопьеобразования при коагуляции применяют флокулянты.
5. Наиболее эффективными являются катионные флокулянты.
