
- •2. Гидросфера земли: история, границы, структура, свойства воды
- •2.1. Районирование мирового океана
- •2.2. Тепловой баланс земли
- •2.3. Круговороты воды в природе
- •2.4. Водный баланс земли
- •2.1. Аномалии физических свойств воды и их экологические последствия
- •II. Теплоемкость воды в 5-30 раз выше, чем у других веществ (кроме водорода и аммиака).
- •Фото. 2.1. Несмотря на сокращение ледников последние 30 лет, «Всемирный потоп» Земле не грозит благодаря высокой удельной теплоте плавления льда.
- •V. Точки замерзания (00с) и кипения (1000с) воды также оказываются аномальными – не соответствуют молекулярной массе.
- •Фото.2.2. Обитатели больших глубин выживут даже в случае наступления на планете «ядерной зимы».
- •Фото.2.4. Гигантские (до 110 м) секвои растут благодаря «адгезии»
- •2.2. Причины аномалий физических свойств воды: строение, структура и геометрия молекулы воды.
- •2.3. Геометрия молекулы воды и золотая пропорция
- •Фото.2.6. Храм Афины - Парфенон
- •Фото.2.7. Храм Василия Блаженного.
- •2.4. Химические свойства воды и ее химический состав в океане
- •Фото.2.8. Первый артезианский источник в провинции Артуа (Франция)
- •Фото.2.9. Ламантины помогли а. Гумбольдту обнаружить в океане «колодцы» с пресной водой – выходы артезианских вод.
- •2.5. Природа солености морских вод
- •Литература
- •Вопросы для закрепления материала
2.4. Химические свойства воды и ее химический состав в океане
Не секрет, что морская вода существенно отличается от пресной. Попытавшись закипятить воду, взятую, например, из Черного, Мертвого и Средиземного морей, нетрудно убедиться, что закипает она при разных температурах, далеких от 1000С. Эффект от купания в этих морях вызовет не меньшее удивление, так как усилия, которые приходится затратить, чтобы удержаться на плаву во всех трех случаях, оказываются совершенно различными. Измерение же температуры в водах, например, Антарктики, показало, что величина этой характеристики здесь значительно ниже 00С - точки замерзания для пресной воды. В отличие от пресной воды морская вода замерзает не при 0°С, а при минус 1,8-2,1°С - в зависимости от концентрации растворенных в ней солей. Имеет максимальную плотность не при + 4°С, а при -3,5°С. Таким образом она превращается в лед, не достигая наибольшей плотности. Если вертикальное перемешивание в пресных водоемах прекращается при охлаждении всей массы воды до +4°С, то в морской воде вертикальная циркуляция происходит даже при температуре ниже 0°С. Процесс обмена между верхними и нижними слоями идет непрерывно, создавая благоприятные условия для развития животных и растительных организмов.
Попробовав пить морскую воду, мы рискуем получить не только расстройство желудка, а можем “доиграться” и до летального исхода по причине, как ни странно, обезвоживания организма. В тоже время, применяя компрессы, ванны, полоскания и другие процедуры с использованием морской воды можно излечиться от множества болезней.
Наконец, еще один пример загадочного явления, связанного с водой. В селе Новая Покровка в Приазовье на Украине в 1929 г. по вечерам наблюдалась фантастическая картина. Из скважины через изогнутую трубу мощная струя воды поступала в каскад наклонных желобов, расположенных на высоких опорах, а по ним стекала к конюшне. Все бы хорошо, но вот незадач! В первых от скважины желобах вода горела в сумерках голубым пламенем как бензин, а внизу… ее пили лошади.
Все эти “чудеса” определяются прежде всего удивительной способностью воды растворять различные вещества. В этом плане с ней не может сравниться ни одна жидкость. В природе практически нет веществ совсем нерастворимых в воде. В случае с лошадиным водопоем из скважины била вода, насыщенная метаном. На поверхности при снижении давления газ выходил из жидкости, местные шутники-ковбои его поджигали, а оставшуюся после сгорания газа чистую воду спокойненько пили животные.
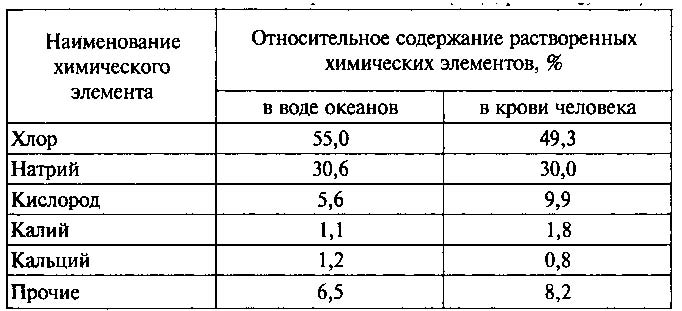
Это качество воды (растворять) определило тот факт, что в морях она, оказывается, имеет специфический химический состав, т.е. содержит определенный набор и количество растворенных солей, находящихся здесь в виде ионов (табл.2.1).
Таблица 2.1. Основные элементы солевого состав морской воды и крови человека.
Любопытно, что еще в средние века алхимики за способность растворять вещества приписывали воде совершенство и обозначали ее в виде перевернутого равностороннего треугольника . При этом считали, что «тела не действуют, если не растворены» - положение, справедливое и сегодня. Кстати, такие способности воды еще 2500 лет назад использовал персидский царь Кир, храня во время своих постоянных походов воду в серебряных сосудах. В древней Индии для дезинфекции воды в неё погружали раскаленное серебро. Многовековой опыт показал, что проникающие в процессе растворения в воду ионы этого металла подавляют размножение бактерий, сохраняя ее качество. Сегодня, так называемая серебряная вода, применяется в Японии и США для обеззараживания плавательных бассейнов, в Китае – для производства прохладительных напитков, а во многих других странах мира – при консервирования различных пищевых продуктов, лечения воспалительных и гнойных процессов.
Таким образом, морская вода представляет из себя очень разбавленный, а потому почти полностью ионизированный, нейтральный раствор практически всех известных природных твердых химических веществ. Кроме того, в ней также растворены газы - кислород, азот, углекислый газ, инертные газы и в некоторых застойных районах - сероводород. И, наконец, в морской воде содержится растворенное органическое вещество.
В этом природном “коктейле” непрерывно протекают сложные физико-химические, биологические и другие процессы, направленные на изменение его общего солевого состава (концентрации), а также соотношения между отдельными ионами. Итогом таких преобразований явилось то, что основными катионами в воде Мирового океана являются Na, Mg, Ca. Их здесь содержится соответственно 14130, 1721 и 5531012т. Преобладающие же анионы в океане представлены прежде всего хлоридами и сульфатами, количество которых (25538 и 35531012т) на порядки превышает содержание других отрицательных ионов.
Кстати, соотношение основных химических компонентов в морской воде и в крови человека практически одинаковы (см. табл.2.1). Оно сохраняется постоянным на протяжении миллионов лет. Этот факт интерпретируется многими учеными как доказательство океанического происхождения жизни на Земле. Из 92-х существующих в природе химических элементов в морской воде обнаружено 73. Однако, только 14 из них имеют концентрации выше чем 1 часть на миллион. Меньше всего в морской воде радона – 1600 атомов в одном литре.
В 70-х годах XVII столетия соавтор известного закона Р. Бойль выполнил первые достоверные измерения содержания суммы солей в воде, взятой с разных глубин океана у побережья Англии, после чего им впервые было высказано предположение о постоянстве солевого состава морской воды.
На протяжении XVII-XIX вв. усилиями ученых многих стран эта мысль получила убедительное подтверждение. В 1819 г. в сборнике научных трудов Лондонского Королевского общества были опубликованы результаты анализов вод открытых районов Ледовитого и Атлантического океанов, а также семи морей, расположенных в противоположных частях Мирового океана. Их автор - морской исследователь А.Марсет, также пришел к выводу, что “пробы морской воды во всех районах земного шара содержат одни и те же компоненты в очень близких пропорциях... различия в химическом составе вод различных морей состоят только в общем количестве присутствующих солей”. В дальнейшем к аналогичному заключению пришли французский ученый Жозеф Луи Гей-Люссак (1778-1850), русский физик Эмилий Христианович Ленц (1804-1865), американский моревед Мэтью Фонтен Мори (1806-1873). Оно было подтверждено и профессором У. Дитмаром после кругосветного плаванья первого научно-исследовательского судна “Челенджер” (1873-1876гг), положившего начало регулярным крупномасштабным исследованиям Мирового океана.
Постоянство соотношения главных ионов в морской воде позволяет, зная содержание в конкретной пробе одного из основных элементов, определить ее общую соленость - концентрацию всех растворенных твердых веществ. «Приоритетными» элементам для расчета общей солености морской воды выбрали сумму галогенов - хлора, брома, фтора, пересчитанную на концентрацию хлора. Так сделали потому, что массовая доля галогенов в общем количестве солей морской воды превышает 55%, к тому же они легко и точно определяются химическим путем в полевых условиях. Эта величина называется хлорностью морской воды, а ее производная, соленость является условной величиной, рассчитанной по сумме галогенов. Она отражает вес в граммах всех солей, растворенных в 1000 г морской воды, измеряется в десятых процента и обозначается - ‰ - промилле.
Изменение содержания солей в морской воде происходит под действием многих факторов, которые можно разделить на три группы: - речной сток, осадки, испарение, образование и таяние морских льдов; - жизнедеятельность морских организмов, формирование и трансформация донных отложений; - дыхание морских организмов, фотосинтез растений, деятельность бактерий.
Средняя соленость на поверхности Мирового океана равна 34,84‰. В Тихом океане она составляет 34,56, в Индийском – 34,68 и в Атлантическом, самом соленом, - 35,30‰. Средняя соленость толщи вод Мирового океана (без Арктического бассейна) - 34,71‰. По этому показателю самым соленым также является Атлантический океан (34,87‰), затем следуют Индийский (34,78‰) и Тихий (34,63‰) океаны. В северном полушарии средняя соленость на 0,13‰ выше, чем в южном. При этом средняя соленость толщи вод Атлантического океана в северном полушарии (35.06‰) выше, чем в южном (34.74‰), а в Тихом океане – наоборот (34.58 и 34.66‰ соответственно) (рис.2.22).
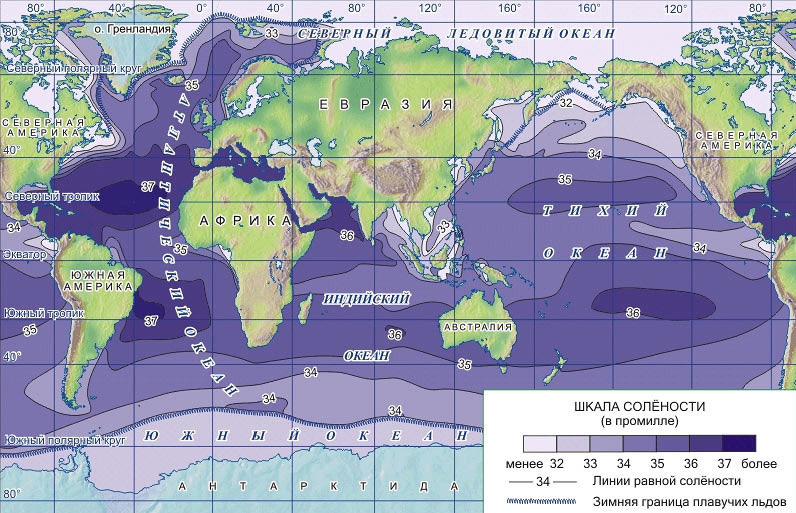
Рис.2.22. Среднегодовое поле солености поверхностных вод Мирового океана.
Именно из-за различий в солености поверхностных вод Черного (17-18 ‰), Средиземного (36-37 ‰) и Мертвого (260-270, а иногда и 310‰) морей их плотность также значительно отличается и плавание в них требует затраты разных усилий. Именно из-за солености температура кипения морской воды превышает 1000С, а температура замерзания - ниже нуля.
Именно соли морской воды делают ее питье опасным для здоровья: чтобы вывести избыточную соль, организм начинает использовать воду из клеток тканей. Это влечет за собой обезвоживание и гибель. А из-за содержания в морской воде положительно и отрицательно заряженных ионов она является целебной для человека.
Наконец, наличие вод с различной соленостью в различных районах Мирового океана и на разных глубинах определяет развитие и интенсивность многих физико-динамических процессов – вертикальной и горизонтальной циркуляции вод, конвективного и турбулентного перемешивания, ответственных за снабжение океана веществом и энергией - то есть за поддержание жизни.
Говоря о значимости солей, растворенных в морской воде, для жизни обитателей океана, нельзя не упомянуть о некоторых феноменальных явлениях природы, связанных с этим ее свойством. После того как в 1126 г. во французской провинции Артуа пробурили первую в Европе скважину для добычи воды, такие ее источники на поверхности суши, во всем мире стали называть артезианскими (фото.2.8).

