
- •Л.В. Кольцов, м.А. Лосева
- •Глава 1.1
- •Глава 1.2 Молекулярно-кинетические свойства дисперсных систем
- •Тема 1.2.1.Броуновское движение
- •Тема 1.1.2. Диффузия
- •Тема 1.2.3. Осмотическое давление
- •Глава 1.3 Оптические свойства и методы исследования дисперсных систем
- •Глава 2.1 Термодинамика поверхностного слоя
- •Тема 2.1.1. Термодинамическая характеристика дисперсных систем. Термодинамический метод избыточных величин Гиббса и метод «слоя конечной толщины
- •Тема 2.1.2. Поверхностное натяжение. Методы измерения поверхностного натяжения. Зависимость поверхностного натяжения от температуры и концентрации. Уравнение Шишковского
- •Тема 2.1.3. Уравнение Гиббса-Гельмгольца для поверхностной энергии. Полная поверхностная энергия
- •Глава 2.2 Адсорбция
- •Тема 2.2.2. Фундаментальное уравнение Гиббса. Определение Гиббсовской адсорбции. Адсорбционное уравнение Гиббса
- •Тема 2.2.3. Поверхностная активность. Поверхностно-активные и поверхностно-инактивные вещества. Анализ уравнения Гиббса. Пав. Эффект Ребиндера. Правило Дюкло-Траубе
- •Глава 2.3 Адсорбционные равновесия
- •Тема 2.3.3. Адсорбция на границе «твердое тело – жидкость». Молекулярная адсорбция. Правило выравнивания полярностей Ребиндера
- •Глава 2.4 Адгезия. Когезия. Смачивание и растекание жидкости
- •Тема 2.4.1. Понятие когезии и адгезии. Смачивание и растекание. Работа адгезии и когезии. Уравнение Дюпре. Краевой угол смачивания. Закон Юнга. Гидрофобные и гидрофильные поверхности
- •Тема 2.4.2. Коэффициент растекания по Гаркинсу. Условие растекания и смачивания. Эффект Марангони. Правило Антонова
- •Глава 2.5 Адсорбция ионов на кристалле. Электрокинетические явления
- •Тема 2.5.1. Образование и строение дэс. Электрокинетический потенциал. Правила написания мицелл
- •Тема 2.5.2. Обменная адсорбция. Иониты. Уравнение Никольского
- •Тема 2.5.3. Электрокинетические явления. Электрофорез. Электроосмос. Расчет -потенциала по скорости электрофореза и электроосмоса. Понятие поверхностной проводимости
- •Глава 3.1 Стабилизация и коагуляция дисперсных систем
- •Тема 3.1.1. Виды устойчивости дисперсных систем. Лиофобные и лиофильные золи
- •Правила коагуляции:
- •Тема 3.1.3. Теория длфо
- •Тема 3.1.4. Виды коагуляции: концентрационная и нейтрализационная. Коагуляция смесями электролитов. Явление «неправильные ряды». Механизм и кинетика коагуляции
- •При коагуляции смесью электролитов различают два типа процессов:
- •Тема 3.1.5. Седиментация и диффузия. Гипсометрический закон. Седиментационно-диффузионное равновесие. Скорость седиментации
- •Глава 4.1 Теория структурообразования Управление структурно-механическими свойствами материалов
- •Тема 4.1.2. Классификация дисперсных систем по структурно-механическим свойствам. Возникновение объемных структур в различных дисперсных системах
- •Глава 5.1 Свойства растворов высокомолекулярных соединений
- •Тема 5.1.1. Свойства вмс. Мембранное равновесие Доннана. Набухание вмс. Их растворение. Давление набухания. Степень набухания. Пластификаторы. Уравнение Хаггинса
- •Тема 5.1.2. Белки как полиэлектролиты.
- •Тема 5.1.3. Вязкость дисперсных систем и растворов вмс. Уравнение Бингама. Удельная, характеристическая, относительная вязкости. Методы измерения вязкости. Тиксотропия
- •Рассмотрим три наиболее распространенных метода измерения вязкости:
- •Капиллярный метод (вискозиметр Оствальда).
- •Метод падающего шарика.
- •Метод вращающегося цилиндра.
- •Глава 6.1 суспензии
- •Глава 6.2 пасты
- •Глава 6.3 эмульсии
- •По концентрации:
- •Глава 6.4 пены
- •Глава 6.5 аэрозоли
- •Классификация аэрозолей
- •Глава 6.6 порошки
|
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «САМАРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» |
Л.В. Кольцов, м.А. Лосева
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ
В ДИСПЕРСНЫХ СИСТЕМАХ
УЧЕБНОЕ ПОСОБИЕ
Самара 2005
УДК 543
Поверхностные явления в дисперсных системах: Учеб. пособие/Л.В. Кольцов, М.А. Лосева; Самар. гос. техн. ун-т. Самара, 2005. 131 с.
Кратко рассмотрены основные разделы курса «Поверхностные явления в дисперсных системах». Предназначено студентам заочного факультета химических специальностей для самостоятельного изучения теоретических основ курса.
ISBN 5-7964-0746-5
Ил. 40. Табл. 2. Библиогр: 7 назв.
Печатается по решению редакционно-издательского совета Самарского государственного технического университета
Рецензенты: д-р хим. наук И.К. Г а р к у ш и н
канд. хим. наук Н.А. Р а с щ е п к и н а
I |
© Л.В. Кольцов, М.А. Лосева, 2005 © Самарский государственный технический университет, 2005 |
|
Раздел 1. |
СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ |
|
Глава 1.1
Предмет курса. Основные понятия. Шкала дисперсности.
Удельная поверхность. Степень дисперсности. Классификация
дисперсных систем. Понятия: дисперсная фаза и дисперсионная
среда. Методы получения дисперсных систем
Предмет курса «Поверхностные явления в дисперсных системах» (коллоидной химии) - изучение дисперсных систем и явлений, происходящих на поверхности раздела фаз.
Дисперсной называют систему, в которой одно вещество распределено в среде другого, причем между частицами и дисперсионной средой есть граница раздела фаз. Дисперсные системы состоят из дисперсной фазы и дисперсионной среды.
Дисперсная фаза - это частицы, распределенные в среде. Ее признаки: дисперсность и прерывистость (рис. 1.1.1.1).
Дисперсионная среда - материальная среда, в которой находится дисперсная фаза. Ее признак - непрерывность.
Поверхность раздела фаз характеризуется раздробленностью и гетерогенностью. Раздробленность характеризуется:
1)
степенью дисперсности:
![]() ,
[см-1;
м-1],
где В
- суммарная межфазная поверхность или
поверхность всех частиц дисперсной
фазы; V
- объем частиц дисперсной фазы.
,
[см-1;
м-1],
где В
- суммарная межфазная поверхность или
поверхность всех частиц дисперсной
фазы; V
- объем частиц дисперсной фазы.
2) дисперсностью - величиной, обратной минимальному размеру а:
![]() [
[![]() ;
;![]() ];
];
3)удельной
поверхностью:
![]() ,
[м2/кг;
см2/г];
,
[м2/кг;
см2/г];
![]() где
m
- масса частиц дисперсной фазы.
где
m
- масса частиц дисперсной фазы.
4)
кривизной
поверхности:
![]() .
Для частицы неправильной формы
.
Для частицы неправильной формы ![]() ,
,
где r1 и r2 - радиусы окружностей при прохождении через поверхность и нормаль к ней в данной точке двух перпендикулярных плоскостей.
Дисперсная
система










Дисперсная фаза



Дисперсионная
среда
Поверхность раздела
фаз




Непрерывность



Гетерогенность
Раздробленность









dx


dx






dy
dy










dz



dх
“Плёнка”
dx
10-7 см,
dy,
dz
10-2
см




“Нить” dx,
dy
10-7 см
dz
10-2
см

“Суспензия”
(золь) dx,
dy,
dz![]() 10-7
см
10-7
см
Р
и с. 1.1.1.1. Характеристики дисперсной
системы
5) размером тела по трем осям, причем определяющим является размер по той оси, где он минимальный. В зависимости от размеров частиц они имеют свои исторические названия (см. рис. 1.1.1.1).
6) приведенным (эквивалентным, эффективным) радиусом - радиусом воображаемых идеально сферических частиц, обладающих той же массой и оседающих с той же скоростью, что и частицы дисперсной системы.
Классификация дисперсных систем осуществляется по нескольким признакам (рис. 1.1.1.2).

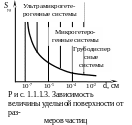
По дисперсности различают:
а) грубодисперсные системы, для них D < 103 [1/см] (рис. 1.1.1.3);
б) микрогетерогенные системы, для них D = 103 - 105 [1/см];
в) ультрамикрогетерогенные системы, для них D = 105 - 107 [1/см].
По агрегатному состоянию дисперсной фазы и дисперсионной среды. Эта классификация была предложена Оствальдом (см. табл. 1.1.1.1).
По структуре дисперсные системы различают:
свободные дисперсные системы, когда частицы обеих составляющих системы могут свободно перемещаться друг относительно друга (золь);
связанные дисперсные системы, когда одна из составляющих системы представляет собой структурированную систему, т.е. частицы фазы жестко связаны между собой (студень, композиты).
Таблица 1.1.1.1
Классификация по агрегатному состоянию фаз
Агрегатное состояние дисперсной фазы |
Агрегатное состояние дисперсион-ной среды |
Условное обозначение фаза/среда |
Название системы |
Примеры |
г |
г |
г/г ж/г тв/г |
Аэрозоли |
атмосфера Земли |
ж |
г |
туман, слоистые облака |
||
тв |
г |
дымы, пыли, перистые облака |
||
г |
ж |
г/ж |
Газовые эму-льсии, пены |
газированная вода, мыльная и пивная пены |
ж |
ж |
ж/ж |
Эмульсии |
молоко, масло сливочное, кремы и т.д. |
тв |
ж |
тв/ж |
Лиозоли, суспензии |
лиофобные коллоидные растворы, суспензии, пасты, краски и т.д. |
г |
тв |
г/тв |
Твердые пены |
пемза, пенопласт, активированный уголь, хлеб, пенобетон и т.д. |
ж |
тв |
ж/тв |
Твердые эмульсии |
вода в парафине, минералы с жидкими включениями, пористые тела в жидкости |
тв |
тв |
тв/тв |
Твердые золи |
сталь, чугун, цветные стекла, драгоценные камни |
По межфазному взаимодействию - лиофильные и лиофобные системы (предложено Г. Фрейндлихом). Классификация пригодна только для систем с жидкой дисперсионной средой.
Лиофильные системы – в них дисперсная фаза взаимодействует с дисперсионной средой и при определенных условиях способна в ней растворяться – растворы коллоидных ПАВ, растворы ВМС. Свободная энергия системы F < 0.
F = U – TdS; Sсмешения > 0;
U = Wког - Wсольв,
где Wког - работа когезии;
Wсольв - работа сольватации.
При U > 0, U < 0 TdS >U. Эта группа характеризуется малым значением поверхностного натяжения на границе раздела фаз.
Лиофобные системы – в них дисперсная фаза не способна взаимодействовать с дисперсионной средой и растворяться в ней.
Существует две группы способов получения дисперсных систем:
Способы диспергирования заключаются в раздроблении тела до коллоидного состояния (мукомольное производство).
Способы конденсации заключаются в укрупнении частиц, атомов, молекул до частиц коллоидных размеров (химическая реакция с образованием осадка).

