
- •Поняття ісе. Хімічний сенсор. Будова типового хімічного сенсора.
- •Принцип роботи іСе. Електрохімічна комірка. Поняття про гальванічний елемент. Рівняння Нікольського-Ейзенмана.
- •Класифікація ісе за природою та агрегатним станом.
- •Основні характеристики ісе. Селективність. Межа визначення.
- •Основні характеристики ісе. Калібрувальна характеристика ісе (лінійність електродної функції). Час відгуку.
- •Загальна характеристика сенсорів зі скляними мембранами.
- •Загальна характеристика сенсорів із твердими мембранами.
- •Загальна характеристика сенсорів із полімерними мембранами.
- •Загальна характеристика сенсорів з рідкими мембранами.
Основні характеристики ісе. Селективність. Межа визначення.
Ефективність роботи ІСЕ визначають наступні його характеристики.
Селективність.
Спочатку ІСЕ називали специфічними
іонними електродами. Хімічну рівновагу
на поверхні сенсора можуть зміщувати
інші іони. Тому більш правильним буде
термін «селективний». Селективність є
найважливішою характеристикою мембранних
електродів. Її характеризують константою
селективності. Вона залежить від
рухливості іонів в розчині та мембрани,
константи гетерогенних рівноваг іонного
обміну, екстракції, дисоціації, асоціації.
Експериментальне визначення цих
параметрів є доволі складним завданням.
Тому для характеристики ІСЕ використовують
умовні коефіцієнти селективності. За
рекомендацією ІЮПАК в якості кількісної
характеристики селективності
використовують потенціометричний
коефіцієнт селективності
![]() ,
який визначає здатність іонселективного
електроду розрізняти різноманітні іони
в змішаному розчині. Чим меншою є величина
для пнари іонів А і В, тим більш чутливий
даний електрод до зміни концентрації
іонів А порівняно з іонами В.
,
який визначає здатність іонселективного
електроду розрізняти різноманітні іони
в змішаному розчині. Чим меншою є величина
для пнари іонів А і В, тим більш чутливий
даний електрод до зміни концентрації
іонів А порівняно з іонами В.
Метрологічною основою для розрахунку коефіцієнтів селективності є рівняння, яке пов’язує потенціал ІСЕ із концентрацією іонів А, В і С в розчині, які конкурують
![]()

Це рівняння можна реалізувати двома способами:
Вимірюванням потенціалу в розчинах, які містять іони А, В та С.
Вимірюванням потенціалу в розчинах, які мстять суміш іонів А + В, А + С і т.д.
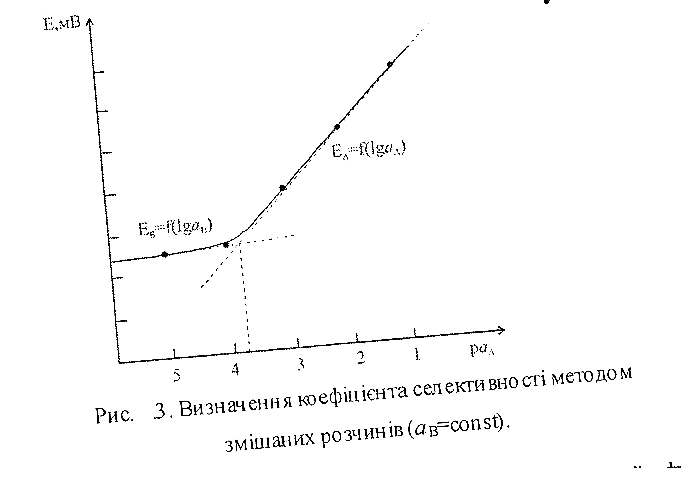
Найчастіше використовують метод змішаних розчинів, який базується на вимірюванні потенціалу розчинів із постійною концентрацією заважаючого іона В і змінною концентрацією досліджуваного іоюна А. За точкою перетину лінійних ділянок отриманої залежності знаходять величину аА і розраховують за знайденим значенням коефіцієнт селекгивності (рис.3)

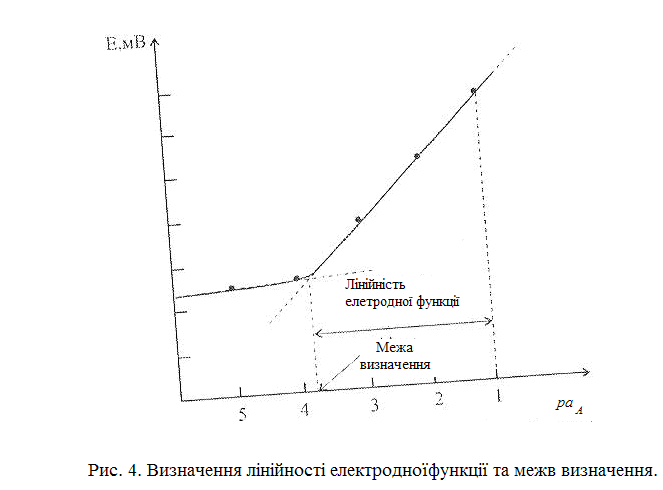
Межа визначення - активність (концентрація) досліджуваного іона, за якої аналітичний сигнал є в два рази вищиме фонового. Межу визначення знаходять як точку перетину лінійної ділянки калібрувальної залежності та базової лінії, яка відповідає тій області концентрацій, в якій сигнал не виникає (рис. 4).
Межа визначення ІСЕ залежить від багатьох факторів. У присутності заважаючих іонів межа визначення погіршується, також негативно на межу визначення впливає розбавлення розчинів та необернена адсорбція іонів.
Основні характеристики ісе. Калібрувальна характеристика ісе (лінійність електродної функції). Час відгуку.
Калібрувальна характеристика ІСЕ (лінійність електродної функції) -
залежність ЕРС електрохімічного ланцюга, що містить ІСЕ та електрод порівняння, від логарифму активності потенціал визначального іона. Діапазон концентрації, в якому залежність потенціалу електрода від логарифму активності іону, який визначають, є лінійною міститься у межах 10-5 – 10-1 М (рис. 4). Даний діапазон концентрацій є оптимальним для ефективної робота іон селективного електроду. Вимоги до робочого діапазону визначають конкретною задачею. Поза межами лінійності (у випадку низьких концентрацій досліджуваного іону) сенсор втрачає чутливість до іону,який визначають.
Час відгуку - це час необхідний для того, щоб в аналітичній системі встановилась рівновага з досліджуваною речовиною. Чим менший час відгуку, тим кращий електрод. Час відгуку може коливатися від декількох секунд до декількох хвилин. Для більшості електродів потенціал електроду за одну хвилину досягає >90% від кінцевої величини. Час відгуку залежить від заважаючих іонів, температури, збільшення чи зменшення концентрації. Також на час відгуку впли ають наступні чинники:
дифузія досліджуваного іона через шар мембрани;
швидкість реакції переносу заряду через межу розділу фаз мембрана-розчин;
швидкість обмінної реакції між досліджуваним іоном та заважаючим іоном в розчині;
швидкість встановлення дифузійного внутрішньо мембранного потенціалу;
дифузія досліджуваного іона в мембрану;
розчинення електродо активної речовини мембрани в досліджуваному розчині.
Основні характеристики ІСЕ. Крутизна калібрувальної хар-ки або кутовий коефіцієнт нахилу, час життя, дрейф потенціалу.
Крутизна калібрувальної характеристики або кутовий коефіцієнт нахилу це відношення з міни ЕРС системи до зміни активності іона в одиницях рХ
S = ΔЕ/ΔрХ. (1)
Теоретично крутизна калібрувальної характеристики рівна коефіцієнту Нернста:
S = 2,3RT/ZF. (2)
В аналітичній хімії значення коефіцієнта Нернста подають у мілівольтах і з температури 298К для однозарядних іонів S = 59,16 мВ, для двозарядних S =29,58 мВ. для тризарядних S =19,72 мВ. Чим ближче значення крутизни до теоретичного, тим кращий електрод. Прийнято вважати, що відгук потенціометричного сенсора є нернстівським або близьким до нього, якщо нахил калібрувальної функції відрізняється від теоретичного на 1- 2 мВ. Нижче цього інтервалу залежність називають субнерстівською, а вище - гіпернерстівською.
Час життя. Потенціометричні сенсори можуть експлуатуватись лише протягом обмеженого часу. Під часом життя розуміють максимальний термін зберігання сенсора готового до експлуатації. Деколи за час життя приймають той термін експлуатації сенсора, після якого його відгук падає на задану величину (близько 5%).
Дрейф потенціалу - постійна немонотонна зміна потенціалу елекгроду з часом у розчині з постійним складом за сталої температури. Дане явище зумовлене зміною в структурі поверхні електроду та розчиненням іонів іонообмінника чи іонофору в досліджуваному розчині. Зазвичай дрейф потенціалу складає менше ± 2 мВ за добу. Чим менший дрейф потенціалу,тим кращий електрод.
