
- •Федеральное агентство по образованию
- •Рецензенты:
- •Предисловие
- •Введение
- •Часть I. Основные классы химических соединений, входящие в состав живой материи глава 1. Белки
- •1.1. Функции белков
- •1.2. Аминокислотный состав белков
- •1.3.Структурная организация белков
- •1.4. Физико-химические свойства белков
- •1.5. Классификация белков
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 2. Нуклеиновые кислоты
- •2.1. Химический состав нуклеиновых кислот
- •2.2. Структура нуклеиновых кислот
- •2.2.1. Структура днк
- •2.2.2. Структура рнк
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 3. Ферменты
- •3.1. Классификация ферментов и номенклатура
- •3.2. Активный центр ферментов
- •3.3. Механизм действия ферментов
- •3.4. Кинетика ферментативных реакций
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 4. Витамины
- •4.1. Классификация витаминов
- •4.2. Витамины, растворимые в жирах
- •4.3. Витамины, растворимые в воде
- •4.4. Витаминоподобные вещества
- •4.5. Антивитамины
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 5. Углеводы
- •5.1. Классификация углеводов
- •5.2. Моносахариды
- •Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 6. Липиды
- •6.1. Классификация липидов
- •6.2. Жирные кислоты
- •6.3. Глицериды
- •6.4. Воска
- •6.5. Фосфолипиды
- •6.6. Гликолипиды (гликосфинголипиды)
- •6.7. Стероиды
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 7. Гормоны
- •7.1. Классификация гормонов
- •7.2. Гормоны гипоталамуса
- •7.3. Гормоны гипофиза
- •7.3.3. Гормоны передней доли гипофиза.
- •7.4. Гормоны паращитовидных желез (паратгормоны)
- •7.5. Гормоны щитовидной железы
- •7.6. Гормоны поджелудочной железы
- •7.7. Гормоны надпочечников
- •7.8. Половые гормоны
- •7.9. Гормоны вилочковой железы
- •7.10. Гормоны насекомых
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 8. Молекулярные механизмы гормонального сигнала
- •8.1. Механизм действия стероидных гормонов
- •8.2. Механизм действия гормонов пептидной природы
- •Вопросы и задачи
- •Рекомендуемая литература
- •Часть II. Обмен веществ и энергии в организме
- •Глава 9. Обмен нуклеиновых кислот
- •9.1. Синтез пуриновых нуклеотидов.
- •9.2. Синтез пиримидиновых нуклеотидов
- •9.3. Биосинтез нуклеиновых кислот (биосинтез днк)
- •Распад нуклеиновых кислот
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 11. Обмен белков
- •10.1. Пути распада белков
- •10.2. Судьба всосавшихся аминокислот
- •10.3. Обезвреживание аммиака в организме
- •10.4. Биосинтез белка
- •Генетический кодовый «словарь»
- •10.4.1. Этапы синтеза белка
- •10.5. Регуляция синтеза белка
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 11. Обмен углеводов
- •11.1. Переваривание и всасывание углеводов
- •11.2. Синтез и распад гликогена
- •11.3. Окисление глюкозы
- •11.3.1. Гликолиз
- •Глюкоза Молочная кислота (2 мол)
- •11.3.2. Цикл Кребса
- •11.3.3. Цепь переноса электронов
- •11.4. Глюконеогенез
- •11.5. Пентозофосфатный путь окисления глюкозы
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 12. Обмен липидов
- •12.1. Переваривание и всасывание липидов
- •12.2. Окисление жирных кислот
- •12.3. Биосинтез жирных кислот
- •12.3.1. Биосинтез насыщенных жирных кислот
- •12.3.2. Биосинтез ненасыщенных жирных кислот
- •12.3.3. Синтез триглицеридов
- •12.3.4. Биосинтез холестерина
- •12.4. Нарушения липидного обмена
- •12.4.1. Ожирение
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 13. Биологическое окисление
- •13.1. Ферменты, катализирующие окислительно-восстановительные реакции
- •13.2. Классификация процессов биологического окисления
- •13.2.1. Свободное окисление
- •13.2.2. Окисление, сопряженное с фосфорилированием адф
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 14. Взаимосвязь процессов обмена веществ
- •Вопросы и задачи
- •Рекомендуемая литература
- •Библиографический список
- •Глава12. Обмен липидов 127
- •Глава13 . Биологическое окисление 141
- •Глава14. Взаимосвязь обмена веществ 145
2.2.2. Структура рнк
РНК – это линейная полинуклеотидная молекула, отличающаяся от ДНК рядом особенностей. Моносахаридом в РНК является рибоза, а вместо тимина содержится урацил. Соответственно? в РНК азотистые основания следующие: аденин (А), цитозин(С), гуанин (Г), урацил (У). Спаривание оснований происходит таким же образом, как и в ДНК, за исключением того, что вместо пары А-Т образуется А-У.
Гидроксильная группа во 2/-положении делает молекулу РНК химически более нестабильной по сравнению с ДНК. В разбавленном растворе щелочи РНК разрушается при комнатной температуре, а молекула ДНК устойчива.
Большинство молекул РНК одноцепочечные, хотя часто в них имеются взаимокомплементраные участки, образующие двуцепочечные структуры – «шпильки».
Существуют три основные типа РНК: информационная (матричная) – мРНК, рибосомная – рРНК, и транспортная – тРНК. Все они играют важную роль в процессе расшифровки генетической информации.
Роль мРНК заключается в переносе информации от ДНК в ядре до цитоплазмы, где она соединяется с рибосомами и служит матрицей, на которой осуществляется синтез белка.
мРНК разнообразны по молекулярной массе (от 0,05х106 до 4х106) и составляют около 2% от общего количества РНК в клетке. Каждую молекулу мРНК кодирует один ген или группа генов. В клетке постоянно образуется множество различных мРНК в соответствии с числом активных в данный момент генов. Время полужизни мРНК у эукариот от двадцати минут до нескольких часов, а у бактерий около двух минут.
Зрелая мРНК содержит 5/- и 3/-концевые нетранслируемые последовательности, длина которых варьирует у разных мРНК. На 5/-конце имеется «кэп»-структура (метилированный по 7/-положению гуанозин, связанный 5 /, 5/-трифосфатной связью со следующим основанием), на 3/- конце находится поли А-«хвост», содержащий от 20 до 250 нуклеотидов (рис. 10).
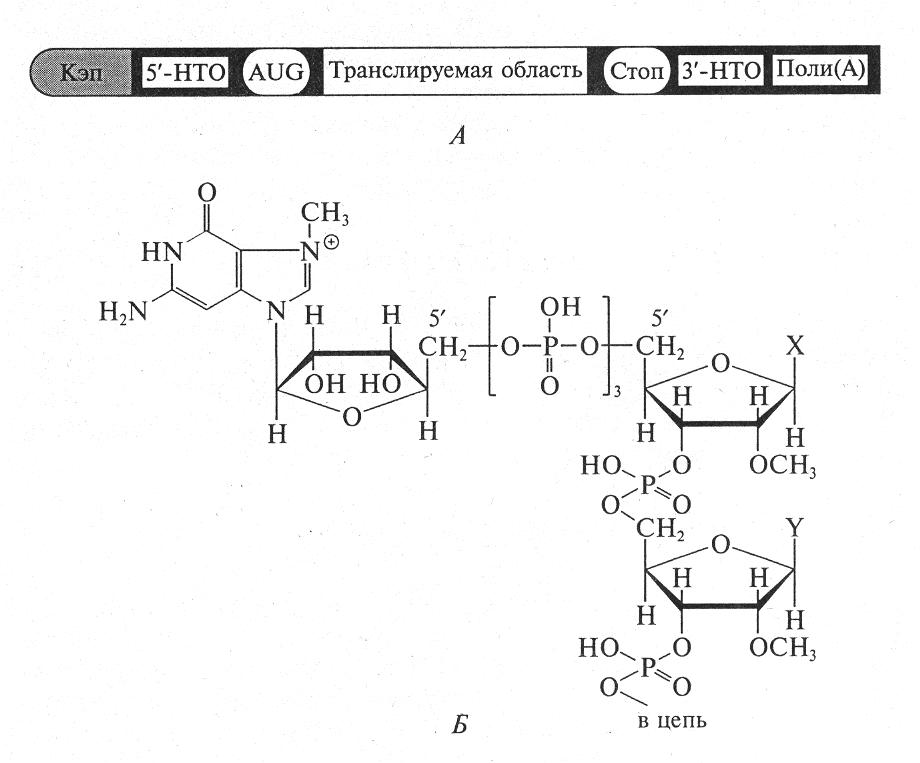
Рис. 10. Структура мРНК (А) и кэп-структура на 5/-конце мРНК эукариот (Б)
Считается, 5/-кэп и поли-А «хвост» защищают мРНК от быстрой деградации. 5/-кэп, кроме того, соединяясь со специфическим белком, принимает участие в связывании мРНК с рибосомами, способствует инициации синтеза белка, влияет на транспорт, трансляцию и распад мРНК. Считается, что не все мРНК содержат поли-А «хвост» (у мРНК гистонов их нет).
рРНК высокомолекулярны и составляют около 80% всех клеточных РНК. В клетках эукариот синтез РНК идет в ядрышке и осуществляется ферментом РНК-полимеразой I. Геном содержит от 50 до 1000 идентичных генов, кодирующих рРНК. Связываясь с определенными белками, рРНК организует важнейший аппарат клет- ки – рибосомы, обеспечивающие синтез всех клеточных белков. На рРНК приходится около 60% массы рибосомы.
тРНК низкомолекулярны (мол.м. около 25000). На долю тРНК приходится 10-15% от общего количества тРНК. Основная функция тРНК – связывание соответствующих аминокислот и перенос их на рибосому с помощью фермента аминоацилсинтетазы. Для каждой аминокислоты существует специфическая аминоацилсинтетаза и тРНК. В настоящее время открыто около шестидесяти различных тРНК (для ряда аминокислот имеется более одной). Аминокислота присоединяется к свободной 3/ ОН-группе. Все тРНК обладают сходной структурой и напоминают клеверный лист (рис. 11).
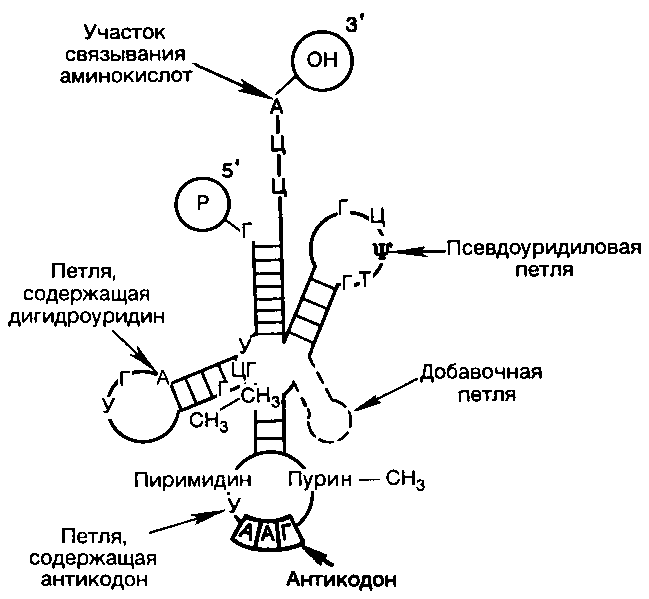
Рис. 11. Структура тРНК
