
- •Федеральное агентство по образованию
- •Рецензенты:
- •Предисловие
- •Введение
- •Часть I. Основные классы химических соединений, входящие в состав живой материи глава 1. Белки
- •1.1. Функции белков
- •1.2. Аминокислотный состав белков
- •1.3.Структурная организация белков
- •1.4. Физико-химические свойства белков
- •1.5. Классификация белков
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 2. Нуклеиновые кислоты
- •2.1. Химический состав нуклеиновых кислот
- •2.2. Структура нуклеиновых кислот
- •2.2.1. Структура днк
- •2.2.2. Структура рнк
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 3. Ферменты
- •3.1. Классификация ферментов и номенклатура
- •3.2. Активный центр ферментов
- •3.3. Механизм действия ферментов
- •3.4. Кинетика ферментативных реакций
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 4. Витамины
- •4.1. Классификация витаминов
- •4.2. Витамины, растворимые в жирах
- •4.3. Витамины, растворимые в воде
- •4.4. Витаминоподобные вещества
- •4.5. Антивитамины
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 5. Углеводы
- •5.1. Классификация углеводов
- •5.2. Моносахариды
- •Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 6. Липиды
- •6.1. Классификация липидов
- •6.2. Жирные кислоты
- •6.3. Глицериды
- •6.4. Воска
- •6.5. Фосфолипиды
- •6.6. Гликолипиды (гликосфинголипиды)
- •6.7. Стероиды
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 7. Гормоны
- •7.1. Классификация гормонов
- •7.2. Гормоны гипоталамуса
- •7.3. Гормоны гипофиза
- •7.3.3. Гормоны передней доли гипофиза.
- •7.4. Гормоны паращитовидных желез (паратгормоны)
- •7.5. Гормоны щитовидной железы
- •7.6. Гормоны поджелудочной железы
- •7.7. Гормоны надпочечников
- •7.8. Половые гормоны
- •7.9. Гормоны вилочковой железы
- •7.10. Гормоны насекомых
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 8. Молекулярные механизмы гормонального сигнала
- •8.1. Механизм действия стероидных гормонов
- •8.2. Механизм действия гормонов пептидной природы
- •Вопросы и задачи
- •Рекомендуемая литература
- •Часть II. Обмен веществ и энергии в организме
- •Глава 9. Обмен нуклеиновых кислот
- •9.1. Синтез пуриновых нуклеотидов.
- •9.2. Синтез пиримидиновых нуклеотидов
- •9.3. Биосинтез нуклеиновых кислот (биосинтез днк)
- •Распад нуклеиновых кислот
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 11. Обмен белков
- •10.1. Пути распада белков
- •10.2. Судьба всосавшихся аминокислот
- •10.3. Обезвреживание аммиака в организме
- •10.4. Биосинтез белка
- •Генетический кодовый «словарь»
- •10.4.1. Этапы синтеза белка
- •10.5. Регуляция синтеза белка
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 11. Обмен углеводов
- •11.1. Переваривание и всасывание углеводов
- •11.2. Синтез и распад гликогена
- •11.3. Окисление глюкозы
- •11.3.1. Гликолиз
- •Глюкоза Молочная кислота (2 мол)
- •11.3.2. Цикл Кребса
- •11.3.3. Цепь переноса электронов
- •11.4. Глюконеогенез
- •11.5. Пентозофосфатный путь окисления глюкозы
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 12. Обмен липидов
- •12.1. Переваривание и всасывание липидов
- •12.2. Окисление жирных кислот
- •12.3. Биосинтез жирных кислот
- •12.3.1. Биосинтез насыщенных жирных кислот
- •12.3.2. Биосинтез ненасыщенных жирных кислот
- •12.3.3. Синтез триглицеридов
- •12.3.4. Биосинтез холестерина
- •12.4. Нарушения липидного обмена
- •12.4.1. Ожирение
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 13. Биологическое окисление
- •13.1. Ферменты, катализирующие окислительно-восстановительные реакции
- •13.2. Классификация процессов биологического окисления
- •13.2.1. Свободное окисление
- •13.2.2. Окисление, сопряженное с фосфорилированием адф
- •Вопросы и задачи
- •Рекомендуемая литература
- •Глава 14. Взаимосвязь процессов обмена веществ
- •Вопросы и задачи
- •Рекомендуемая литература
- •Библиографический список
- •Глава12. Обмен липидов 127
- •Глава13 . Биологическое окисление 141
- •Глава14. Взаимосвязь обмена веществ 145
Рекомендуемая литература
Биохимия. Краткий курс с упражнениями и задачами / Под ред. Члена-корреспондента РАН, проф. Е.С. Северина, проф. А.Я.Николаева. – М.: ГЭОТАР- МЕД, 2001. – 448 с.
Березов Т.Т., Коровкин Б.Ф. Биологическая химия: Учебник.– М.: Медицина, 1998. – 704 с.
Красильникова Л.А., Авксентьева О.А., Жмурков В.В., Садовниченко Ю.А. Биохимия растений / Под ред. Л.А. Красильниковой. – Ростов н/Д.: «Феникс»; Харьков: Торсинг, 2004. – 224 с.
Овчинников Ю.А. Биоорганическая химия. – М.: Просвещение, 1987. – 816 с.
Филлипович Ю.Б. Основы биохимии: Учебник для хим. и биол. спец. ун-тов и ин-тов.– М. :Изд-во «Агар», 1999. – 512 с.
Эллиот В. Биохимия и молекулярная биология / В.Эллиот, Д. Эллиот; Под ред. А.И.Арчакова, М.П. Кирпичникова, А.Е. Медведева, В.П. Скулачева. – Пер. с англ. О.В. Добрыниной, И.С. Севериной, Е.Д. Скоцеляс и др. – М.: МАИК «Наука / Интерпериодика», 2002. – 446 с.
Глава 13. Биологическое окисление
Процесс биологического окисления представляет систему окислительно-восстановительных реакций, роль которых состоит в обеспечении организма энергией и метаболитами, получаемыми за счет восстановленных органических соединений. Посредством реакций биологического окисления разрушаются также вредные продукты обмена веществ и проникшие в организм чужеродные соединения. Различные органические соединения, поступающие в организм, обладают определенным уровнем потенциальной энергии («свободной энергией»). Основными экзогенными источниками энергии в организме являются углеводы, жиры, белки. Используя тот или иной субстрат, организм обеспечивает себя энергией в форме АТФ или фосфатсодержащих соединений.
13.1. Ферменты, катализирующие окислительно-восстановительные реакции
Ферменты, катализирующие окислительно-восстановительные реакции, называют оксидоредуктазами. Их разделяют на 5 групп.
1. Оксидазы. Они катализируют удаление водорода из субстрата, используя при этом в качестве акцептора водорода только кислород (рис. 42).
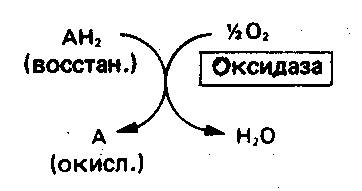
Рис. 42. Окисление метаболита, катализируемое оксидазой
Оксидазы содержат медь, продуктом реакции является вода. Широко распространена в растительных животных тканях цитохромоксидаза (цитохром а3). Она служит конечным компонентом цепи дыхательных переносчиков, локализованных в митохондриях, и катализирует реакцию, в результате которой электроны, высвобождающиеся из молекул субстрата при их окислении дегидрогеназами, переносятся на кислород.
Фенолаза катализирует превращение монофенола в о-фенол; уриказа, катализирует окисление мочевой кислоты в аллантоин; моноаминоксидаза окисляет адреналин и тиамин в митохондриях.
2. Аэробные дегидрогеназы – ферменты, катализирующие удаление водорода из субстрата; в отличие от оксидаз они могут использовать в качестве акцептора водорода не только кислород, но и искусственные акцепторы, такие как метиленовый синий (рис. 44).

Рис. 44. Окисление метаболита, катализируемое аэробной дегидрогеназой
Эти дегидрогеназы относятся к флавопротеинам, и продуктом катализируемой ими реакции является перекись водорода, а не вода. Аэробные дегидрогеназы содержат в качестве простетической группы флавинмононкулеотид (ФМН) или флавнадениндинуклеотид (FФАД). (ФМН) и (ФАД) образуются в организме из рибофлавина (витамин В2). Многие флавопротеиновые ферменты содержат один или несколько ионов металлов, выполняющих роль кофакторов; такие флавопротеиновые ферменты называют флавопротеинами.
К ферментам группы аэробных дегидрогеназ относятся также дегидрогеназа (ФМН-содержащий фермент) L-аминокислот, катализирующая окислительное дезаминирование природных L-аминокислот. Широко распространена ксантиндегидрогеназа (ксантиноксидаза), она обнаружена в молоке, тонком кишечнике, почках и печени. Ксантиндегидрогеназа содержит молибден; играет важную роль в превращении пуриновых оснований в мочевую кислоту как главный конечный азотофиксирующий продукт метаболизма пуринов, а также катаболизма белков и аминокислот.
Альдегиддегидрогеназа – FAD-содержащий фермент, находящийся в печени млекопитающих. Это – металлофлавопротеин, содержащий молибден и негемовое железо, окисляющий альдегиды и N-гетероциклические субстраты.
Глюкозооксидаза – FAD-специфичный фермент, получаемый из грибов; используется при определении глюкозы.
3. Анаэробные дегидрогеназы – ферменты, катализирующие удаление водорода из субстрата, но не способные использовать кислород в качестве акцептора водорода (рис. 45).
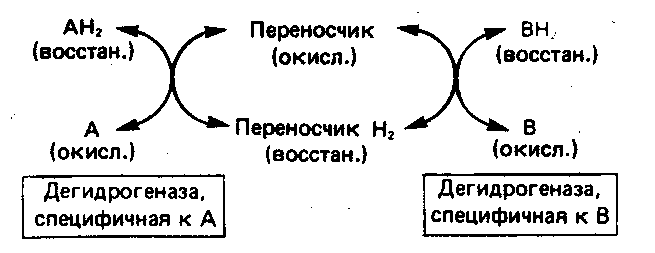
Рис. 45. Окисление метаболита, катализируемое анаэробной дегидрогеназой
Эти ферменты выполняют две главные функции:
а) Перенос водорода с одного субстрата на другой в сопряженной окислительно-восстановительной реакции. Эти дегидрогеназы специфичны к субстратам, но часто используют один и тот же фермент или переносчик водорода.
б) Функцию компонентов дыхательной цепи, обеспечивающих транспорт электоронов от субстрата на кислород (рис.46).
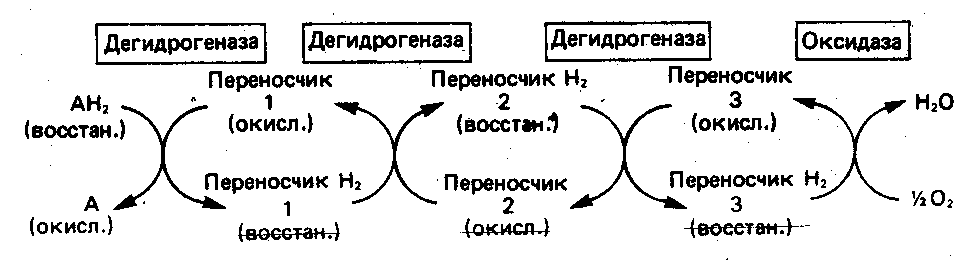
Рис. 46. Окисление метаболита анаэробными дегидрогеназами и на завершающей стадии – истинной оксидазой дыхательной цепи
Среди анаэробных дегидрогеназ различают дегидрогеназы, зависимые от никотинамидных коферментов, рибофлавиновые дегидрогеназы, цитохромы. NAD-зависимые дегидрогеназы катализируют окислительно-восстановительные реакции окислительных путей метаболизма – гликолиза, цикла лимонной кислоты, дыхательной цепи митохондрий. NADP-зависимые дегидрогеназы участвуют в процессах восстановительного синтеза, в частности, во внемитохондриальном синтезе жирных кислот и стероидов; они также являются коферментами дегидрогеназ пентозофосфатного пути.
Большинство раибофлавин-зависимых аэробных дегидрогеназ либо участвуют в транспорте электронов по дыхательной цепи, либо поставляют электроны для этой цепи. NADН-дегидрогеназа – компонент дыхательной цепи, переносящий электроны от NADH к более электроположительным компонентам. Другие дегидрогеназы, например, сукцинатдегидрогеназа, ацил-СоА-дегидрогеназа и митохондриальная глицерол-3-фосфат-дегидрогеназа, переносят восстановительные эквиваленты от субстрата непосредственно на дыхательную цепь.
Цитохромы служат переносчиками электронов от флавопротеинов к цитохромоксидазе. Помимо дыхательной цепи цитохромы имеются в эндоплазматическом ретикулуме (цитохромы Р-450 и b5 ), в растительных клетках, бактериях и дрожжах.
4. Гидроксипероксидазы – ферменты, использующие в качестве субстрата перекись водорода или органические перекиси. К этой категории относятся два типа ферментов: пероксидазы, находящиеся в составе молока, в растениях, лейкоцитах, тромбоцитах, эритроцитах и т.д., и каталаза, функционирующая в тканях животных и растений.
5. Оксигеназы – катализирующие прямое введение кислорода в молекулу субстрата. Оксигеназы не относятся к ферментам, катализирующим реакции, снабжающие клетку энергией; они участвуют в синтезе и деградации многих типов метаболитов. Ферменты этой группы делятся на две подгруппы:
а) Диоксигеназы (кислород-трансферазы, истинные оксигеназы). Эти ферменты катализируют включение в молекулу субстрата обоих атомов молекулы кислорода:
А + О2 АО2
Примером служат железосерные ферменты гомогентизатдиоксигеназа и 3-гидроксиантранилат-диоксигеназа, а также гемсодержащие ферменты, в частности L-триптофандиоксигеназа (триптофанпирролаза).
б) Монооксигеназы (оксидаза со смешанной функцией, гидроксилазы). Эти ферменты катализируют включение в субстрат только одного из атомов молекулы кислорода. Другой атом кислорода восстанавливается до воды; для этой цели необходим дополнительный донор электронов (косубстрат):
А – Н + О2 + ZН2 А – ОН + Н2О + Z
