
- •Вопрос 3. Понятие о полярности и поляризуемости ковалентной связи. Взаимосвязь полярности связи с поляризуемостью атома (молекулы или иона). Мягкие и жесткие атомы, их способность к поляризации.
- •5.Сопряжение (π-π-сопряжение и ρ-π-сопряжение). Сопряженные системы с открытой цепью: 1,3-диены, α, β-ненасыщенные карбонильные соединения, карбоксильная группа как сопряженная система.
- •Реакции, доказывающие наличие двух таутомерных форм в растворе.
- •Кислотно-основные свойства пррола, имидазола, пиридина.
- •Вопрос 10. Хиральность, ахиральность. Плоскость и ось симметрии. Стереоизомерия с двумя и более центрами хиральности: энантиомерия и диастереомерия; привести формулы веществ. Мезоформы и рацематы.
- •Вопрос 14.Реакции элиминирования. Повышенная сн-кислотность как причина реакции элиминирования, конкурентных реакциям нуклеофильного замещения у sp3-гибридизованного атома углерода.
- •Вопрос 15.Особенности реакций электрофильного присоединения у алкадиенов, алкинов, малых циклов, α,β-ненасыщенных альдегидов и карбоновых кислот (гидратация, гидрогалогенирование).
- •Вопрос 22.Строение, химические и физические свойства винной кислоты-оптическая активность, мезоформы. Строение, свойства и значение двухосновных кислот: щавелевой, янтарной, глутаровой.
- •Вопрос 24.Стереоизомерия в ряду соединений с двойной связью: π-диастереомерия (цис- и транс- изомеры). Малеиновая и фумаровая кислоты, их медико-биологическое значение.
- •Вопрос 27.Желчные кислоты: холевая, гликохолевая, таурохолевая. Строение, биороль.
- •Вопрос 28.Угольная кислота и её производные (мочевина, уретаны, уреиды): строение, биороль и применение в медицине.
- •Вопрос 29. Лимонная кислота,-строение, свойства, значение, образование из щавелевоуксусной кислоты. Реакции разложения при нагревании.
- •Вопрос 32. Сложные жиры, производные фосфатидиловых: фосфолипиды. Строение, биороль. Гидролиз (полный и частичный).
- •Вопрос 33.Сфинголипиды: церамиды, сфингомиелины, их строение. Понятие о структурных компонентах. Значение.
- •Вопрос 34. Аминоспирты: коламин, холин, ацетилхолин. Аминофенолы: дофамин, адреналин, норадреналин. Строение, пути биосинтеза, биологическая роль.
- •Вопрос 35. Кефалины и лецитины-структурные компоненты клеточных мембран. Состав, строение, биороль. Бифильность сложных липидов
- •Вопрос 37. Многоатомные спирты. Строение и номенклатура. Химические свойства: кислотность, образование хелатных комплексов, образование простых и сложных эфиров, окисление.
- •Вопрос 39. Неомыляемые липиды. Стерины. Холестерин,-строение, роль в организме.
- •Вопрос 40. Гликолипиды: цереброзиды, ганглиозиды. Понятие о структурных компонентах. Бифильность сложных липидов. Значение.
- •Вопрос 41. Неомыляемые липиды. Классификация. Каротиноиды: β-каротин. Строение, значение.
- •Вопрос 42. Углеводы. Общая классификация. Моносахариды. Конформации пираноз. Образование и гидролиз о- и n-гликозидов.
- •Вопрос 45.Невосстанавливающие сахара: рафиноза. Строение, гидролиз, гликозидная связь.
- •Вопрос 46. Хондроитинсульфат и гиалуроновая кислота-гетерополисахариды. Строение, свойства, биороль.
- •Вопрос 49. Гомополисахариды: гликоген, целлюлоза. Строение, свойства, биороль. Гидролиз гликогена.
- •Вопрос 50. Явление таутомерии моносахаридов. Написать схему таутомерных превращений д-ксилозы в растворе. Мутаротация моносахоридов.
- •Вопрос 52. Гепарин, его состав, свойства, значение. Пектины: строение полигалактуроновой кислоты, биороль.
- •Вопрос 53. Пиразол, имидазол, тиазол, пиридин, пиримидин, пурин,-гетероциклы с несколькими гетероатомами: строение, значение. Кислотные и основные свойства этих гетероциклов.
- •Вопрос 55. Мочевина: строение, ферментативный и щелочной гидролиз, образование биурета (хелатного комплекса). Количественное определение мочевины. Гуанидин.
- •Вопрос 58. Гидрокси- и аминокислоты как гетерофункциональные соединения. Реакции α-аминокислот со щелочами, спиртами, формальдегидом, соляной кислотой, гидроксидом меди (ιι), дезаминирование.
- •61.Реакции α,- β-,γ-амино- и гидроксикислот, протекающие при нагревании. Формольное титрование, его значение. Качественные реакции на α-аминокислоты.
- •Вопрос 62. Образование α-аминокислот из α-кетокислот: восстановительное аминирование, транс-аминирование (переаминирование).
- •Вопрос 66. Биологическая роль пара-аминобензойной кислоты (пабк). Производные пабк: анестезин, новокаин,-строение, применение в медицине
- •Вопрос 68.Сульфаниловая кислота и её амид-стрептоцид (строение, получение из анилина). Применение в медицине и механизм действия сульфаниламидных препаратов.
- •Вопрос 72. Нуклеиновые кислоты: рнк и днк. Строение: нуклеотидный состав, сходство и различие в строении, функции. Минорные основания.
- •Вопрос 73. Комплементарность азотистых оснований. Образование водородных связей в комплементарных парах нуклеиновых оснований. Дезаминирование азотистых оснований.
- •Вопрос 74. Нуклеотиды (рибонуклеотиды и дезоксирибонуклеотиды): строение, номенклатура, частичный и полный гидролиз.
- •Вопрос 75. Нуклеозиды, их строение, значение, гидролиз.
- •Вопрос 76. Строение пиримидиновых оснований: урацила, тимина, цитозина и пуриновых оснований: аденина, гуанина. Лактим-лактамная и другие виды таутомерии. Значение.
- •Вопрос 77.Первичная структура нуклеиновых кислот. Рнк и днк, их нуклеотидный состав. Фосфодиэфирная и гликозидная связь. Гидролиз.
- •Вопрос 79. Первичная, вторичная, третичная и четвертичная структуры белков,-химические связи, обеспечивающие сохранение данной структуры. Денатурация и ренатурация белков.
- •Вопрос 80. Виды рнк и их функции. Вторичная структура днк. Роль водородных связей в формировании вторичной структуры. Роль нуклеиновых кислот в биоситезе белка.
- •Вопрос 82. Синтез пептидов с учетом защиты и активации.
- •Вопрос 83. Мутагенное действие азотистой кислоты на структуру нуклеиновых кислот. Нуклеозиды-антибиотики: кордицепин, арабинозид аденина, их строение, биороль.
- •Вопрос 84. Алкалоиды. Принципы классификации. Значение для медицины. Наркотики: морфин, кофеин, никотин: строение, действие на организм.
- •Вопрос 85. Алкалоиды, их характеристика и источники получения. Атропин, кокаин, героин: строение, использование в медицине.
Вопрос 40. Гликолипиды: цереброзиды, ганглиозиды. Понятие о структурных компонентах. Бифильность сложных липидов. Значение.
Гликолипиды. Как можно судить по названию, соединения этой группы включают углеводные остатки (чаще D-галактозы, реже D-глюкозы) и не содержат фосфорной кислоты и связанных с ней азотистых оснований. Типичные представители гликолипидов — цереброзиды и ганглиозиды — представляют собой сфингозинсодержащие липиды (их можно поэтому считать и сфинголипидами). В цереброзидах остаток церамида связан с D-галактозой или D-глюкозой бета-гликозидной связью. Цереброзиды (галактоцереброзиды, глюкоцереброзиды) входят в состав оболочек нервных клеток.
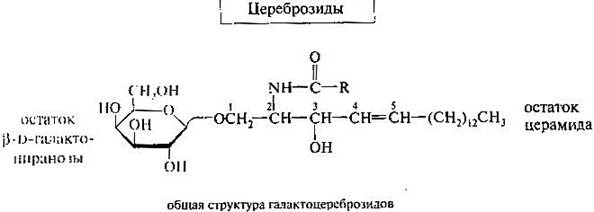
Впервые из серого вещества головного мозга были выделены ганглиозиды — богатые углеводами сложные липиды. В структурном отношении ганглиозиды сходны с цереброзидами, отличаясь тем, что вместо моносахарида они содержат сложный олигосахарид, в состав которого входит по крайней мере один остаток N-ацетилнейраминовой кислоты.
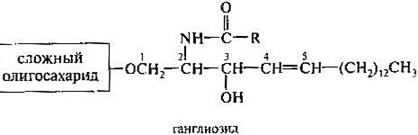
Характерной особенностью сложных липидов является их бифильность, обусловленная наличием неполярных гидрофобных и высокополярных ионизированных гидрофильных группировок. В фосфатидилхолинах например, углеводородные радикалы жирных кислот образуют два неполярных хвоста, а карбоксильная фосфатная и холиновая группы — полярную часть.
Вопрос 41. Неомыляемые липиды. Классификация. Каротиноиды: β-каротин. Строение, значение.
Липиды обладают способностью к гидролизу в кислой и щелочной среде. Поскольку в результате гидролиза в щелочной среде образуются соли высших карбоновых кислот, т. е. мыла, то сами липиды принято называть омыляемыми. Такое название часто встречается в биохимической литературе по той причине, что для группы негидролизующихся низкомолекулярных биорегуляторов продолжают использовать название неомыляемые липиды.
Неомыляемые липиды. К ним относятся стероидные гормоны, простаноиды, некоторые коферменты, жирорастворимые витамины, объединяемые одним названием — низкомолекулярные биорегуляторы.
Под этим названием объединяют ряд углеводородов и их кислородсодержащих производных, в состав которых входят гидроксильная, карбонильная группы, углеродный скелет которых построен из двух, трех и более звеньев изопрена. Сами углеводороды называют терпеновыми углеводородами, а их кислородсодержащие производные — терпеноидами. Терпенами богаты эфирные масла растений (герани, розы, лаванды, лимона, перечной мяты и др.), смола хвойных деревьев и каучуконосов. К терпенам относятся и различные растительные пигменты и жирорастворимые витамины. Группировка терпенового типа (изопреноидная цепь) включена в структуру многих биологически активных соединений. В большинстве терпенов изопреновые фрагменты соединены друг с другом по принципу «голова к хвосте — изопреновое правило (Л. Ружичка, 1921), как показано на примере мирцена.

Терпеновые углеводороды и терпеноиды. Общая формула большинства терпеновых углеводородов — (С5Н8)n. Они могут иметь ациклическое и бициклическое (би-, три- и полициклическое строение).
С учетом числа изопреновых группировок в молекуле различают
• монотерпены (две изопреновые группировки);
• сесквитерпены (три изопреновые группировки);
• дитерпены (четыре изопреновые группировки);
• тритерпены (шесть изопреновых группировок);
• тетратерпены (восемь изопреновых группировок).
Примерами ациклических терпенов служат упоминавшийся выше мирцен — монотерпен, содержащийся в эфирных масла хмеля и благородного лавра; родственный мирцену спирт гераниол входящий в состав эфирных масел герани и розы и при мягком окислении образующий альдегид — цитраль а.

Лимонен — представитель моноциклических терпенов. Он содержится в лимонном масле и скипидаре. Лимонен входит в состав масла тмина. Рацемическая форма лимонена (дипентен) может быть получена в результате реакции диенового синтеза из изопрена при нагревании.

При восстановлении оптически активного лимонена или дипентена получается ментан, а при полной их гидратации в кислой среде, протекающей в соответствии с правилом Марковникова образуется двухатомный спирт терпин. Терпин в виде гидрата применяется как отхаркивающее средство при хроническом бронхите.
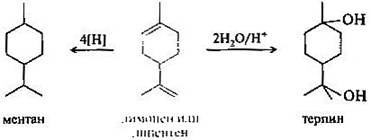
3амещенные дипентены (например, каннабидиол) — психоактивное начало гашиша (марихуаны). Ментол — имеет скелет ментана подобно лимонену. Ментол содержится в эфирном масле перечной мяты. Из приведенной конформации ментола видно, что все три заместителя в циклогексановом кольце занимают экваториальные положения.
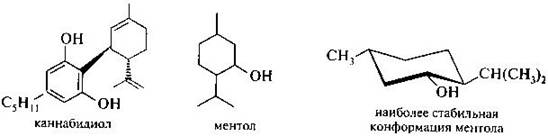
для получения рацемического ментола в промышленности м-крезола алкилируют изопропиловым спиртом в присутствии серной кислоты. При этом из изопропилового спирта первоначально генерируется изопропильный катион — электрофильная частица. При последующем восстановлении продукта алкилирования — тимола получается ментол.

Ментол оказывает антисептическое, успокаивающее и болеутоляющее (отвлекающее) действие, входит в состав валидола, а также мазей, применяемых при насморке. Альфа-пинен — бициклический монотерпен ряда пинана. Его левовращающий энантиомер — важная составная часть скипидара, получаемого из хвойных деревьев.
Камфора — бициклический кетон — редкий пример соединения, в котором шестичленный цикл имеет конформацию ванны. Камфора содержит два асимметрических атома углерода, и для нее следовало бы ожидать существования четырех оптически активных стереоизомеров. Их, однако, известно всего два, так как вследствие жесткости системы конфигурация обоих хиральных центров может измениться лишь одновременно (транс-расположение мостиковой группы -С(СН3)2- между узловыми асимметрическими атомами невозможно).
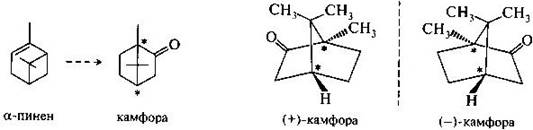
Камфора издавна применяется в медицине как стимулятор сердечной деятельности. Ее правовращающий стереоизомер выделяют из эфирного масла камфорного дерева. При действии брома на камфору замещается альфа-положение по отношению к карбонильной группе с образованием бромокамфоры.
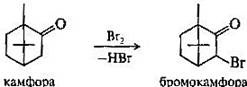
Бромокамфора улучшает деятельность сердца, оказывает успокаивающее действие на центральную нервную систему.
Особую группу терпенов составляют каротиноиды — растительные пигменты. Некоторые из них играют роль витаминов или предшественников витаминов, а также участвуют в фотосинтезе. Большинство каротиноидов относится к тетратерпенам. Их молекулы содержат значительное число сопряженных двойных связей, поэтому имеют желто-красную окраску. Для природных каротиноидов характерна транс-конфигурация двойных связей. Каротин — растительный пигмент цвета, в большом количестве содержавшийся в моркови, а также томатах и сливочном масле. Известны три его изомера, называемые альфа-, бета- и гамма-каротинами, различающиеся числом циклов и положением двойных связей. Все они являются предшественниками витаминов группы А. Молекула бета-каротина симметрична и состоит из двух одинаковых частей.

