
- •Глава IX. Карбоновые кислоты и их производные.
- •IX.1. Карбоновые кислоты
- •IX.1.1. Способы получения
- •Свойства карбоновых кислот
- •IX.1.3. Химические свойства
- •IX.1.3.1. Кислотные свойства.
- •IX.1.3.2. Нуклеофильные реакции карбонильной группы карбоновых кислот
- •3. Образование галогенангидридов (ацилгалогенидов).
- •IX.1.3.3. Реакции, сопровождающиеся потерей карбоксильной группы
- •IX.1.3.4. Реакции положения к карбоксильной группе
Глава IX. Карбоновые кислоты и их производные.
Карбоновые кислоты – соединения, содержащие функциональную группу
![]() СООН
– карбоксильную
группу,
своеобразный «гибрид» карбонильной и
гидроксильной групп:
СООН
– карбоксильную
группу,
своеобразный «гибрид» карбонильной и
гидроксильной групп:
Соединения, содержащие одну карбоксильную группу, – монокарбоновые (одноосновные) кислоты, две группы - дикарбоновые (двухосновные) и т.д. Общая формула простейших (монокарбоновых) кислот – R-CO-OH, где R может быть насыщенным, ненасыщенным, ациклическим, алициклическим или ароматическим радикалом. Карбоновые кислоты содержат фрагмент R-CO – ацил (ацильный радикал), и с этой точки зрения их можно рассматривать как ацилированную воду.
Карбоновые кислоты – родоначальники целого ряда родственных соединений, которые называют производными карбоновых кислот; эти соединения могут образовываться из карбоновых кислот (часто в одну стадию), превращаться обратно в карбоновые кислоты, а также во многих случаях переходить друг в друга.
Производные карбоновых кислот можно (в достаточной степени условно) разделить на четыре группы:
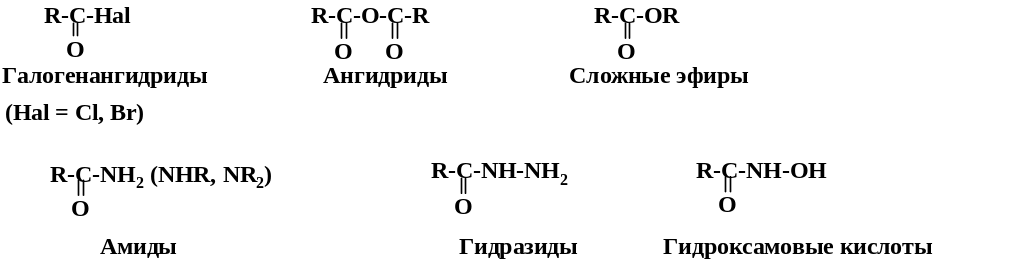 I.
Соединения общей формулы R-CO-X,
т.е. продукты формального замещения
карбоксильной гидроксигруппы:
I.
Соединения общей формулы R-CO-X,
т.е. продукты формального замещения
карбоксильной гидроксигруппы:
В о всех этих производных сохраняется ацильный фрагмент RСО; галогенангидриды (в большинстве случаев это хлорангидриды) можно рассматривать как ацилированные галогеноводороды, ангидриды – как ацилированные карбоновые кислоты, сложные эфиры, амиды, гидразиды, гидроксамовые кислоты – как ацилированные соответственно спирты, аммиак (первичные или вторичные амины), гидразин, гидроксиламин.
 II.
Соединения общей формулы R-CZ-X,
в которых замещены как гидроксигруппа,
так и «карбонильный» атом кислорода:
II.
Соединения общей формулы R-CZ-X,
в которых замещены как гидроксигруппа,
так и «карбонильный» атом кислорода:
III. Производные, которые можно рассматривать как ацетали на основе карбонильных групп сложных эфиров или амидов:
Нетрудно заметить сходство этих соединений с ацеталями карбонильных соединений - здесь вместо радикала (или водорода) стоит группа OR или NH2 (NHR, NR2).
![]() IV.
Продукты внутримолекулярной дегидратации
карбоновых кислот типа RСН2СООН
(кетены) и амидов RCONH2
(нитрилы):
IV.
Продукты внутримолекулярной дегидратации
карбоновых кислот типа RСН2СООН
(кетены) и амидов RCONH2
(нитрилы):
Наиболее широко используются производные первой группы и нитрилы; весьма перспективно использование в органическом синтезе ортоэфиров, ацеталей амидов, а также кетенов. Производные группы II пока используются в меньшей степени.
IX.1. Карбоновые кислоты
Из всех приведенных выше типов соединений карбоновые кислоты являются наиболее доступными; это одна из причин, почему именно они считаются основными (материнскими) соединениями в этом ряду. Другая причина – специфические свойства карбоксильной группы – единственной органической функциональной группы, обладающей достаточно сильными кислотными свойствами.
Простейшей монокарбоновой кислотой является муравьиная НСООН, ее ближайший гомолог – уксусная кислота СН3СООН; простейшая дикарбоновая кислота – щавелевая НООС-СООН, ее ближайший гомолог – малоновая кислота НООС-СН2-СООН; простейшая ароматическая кислота – бензойная С6Н5СООН. [Нетрудно заметить, что среди карбоновых кислот широко распространены тривиальные названия; причина в том, что карбоновые кислоты составляли значительную часть среди первых органических веществ, выделенных из природных источников, – помимо упомянутых муравьиной и щавелевой кислот это винная, лимонная, молочная и многие другие].
Помимо карбоксильной группы, карбоновые кислоты могут содержать и другие функциональные группы, в частности, гидроксильную (гидроксикислоты), карбонильную (оксокислоты), аминогруппу (аминокислоты) и другие.
Своеобразной карбоновой кислотой является угольная кислота НО-СО-ОН; сама она, как известно, неустойчива, но некоторые ее производные вполне стабильны.
